влияние на организм человека, действие
Как только человечество впервые открыло для себя состояние алкогольного опьянения, с той самой поры пошел отсчет смертям от различных отравлений, связанных со спиртосодержащими жидкостями. За время существования цивилизации, от некачественного алкоголя умерло достаточно людей, особенно за последние сто лет. И тем более непонятно, зачем в наши дни пить спиртное сомнительного качества, когда сегодня можно выбрать хороший алкогольный напиток, зная несколько необходимых условий. И уж совсем неясно стремление людей продолжать «глушить» спирт. А ведь этиловый и метиловый спирт на глаз не отличить. Поэтому нужно рассмотреть проблему: метиловый спирт, пагубное влияние на организм человека.
Как распознать метил
Не вдаваясь в дебри химического анализа, есть смысл подчеркнуть, что метиловый спирт пить нельзя, а вот этиловый можно. Последний тип, из перечисленных спиртов, является питьевым и легко усваивается в организме. С метанолом, все наоборот.
У этилового спирта и метилового есть особенности, благодаря которым их можно различить и сделать соответствующие выводы, пить или нет, но только при наличии:
- железной емкости;
- медной проволоки;
- горелки;
- другой посуды;
- градусника.
Пить и дегустировать не придется. Требуется налить в емкость подозрительную жидкость и нагреть над огнем. Этанол кипит при 78°C, метанол при 64°C. Другой способ. Накалить медную проволоку и окунуть в вещество. Этиловый спирт издает запах, похожий на аромат яблок, метиловый пахнет совершенно иначе – противно.
Влияние этилового спирта на организм человека не смертельно. Про него можно сказать еще и то, что он легче воды, быстро воспламеняется и служит в качестве антисептика. Пить антидот не потребуется, даже если присутствуют симптомы отравления организма. Все иначе с метилом. Употребление небольшого количества метилового спирта, до 30 грамм, приведет, в лучшем случае, к слепоте. Смертельная доза составляет 100 грамм и больше.
При крайних случаях, антидот или неотложная помощь, как правило, не помогают, организм гибнет. Главное помнить, что метиловый спирт является ядом для человека. Почему, и чем он так опасен? Метанол состоит из отходов нефтепереработки, природного газа и коксующегося угля. Формула вещества Ch4OH. Он быстро растворяется в воде, других спиртах, бензоле, ацетоне. Опытным путем был получен Жаном Батистом Дюма и Эженом Пелиго из продуктов сухой перегонки древесины.
Признаки отравления
Метанол опасен еще и тем, что он относится к нервно-сосудистым ядам и в частых случаях при отравлениях антидот, как правило, бесполезен из-за наступившего коллапса с развитием кислородной недостаточности и ацидоза. Пить его категорически нельзя, а если небольшое его количество попало в организм человека, можно говорить о сильнейшем отравлении.
Смертельная доза для всех разная, но опасность кроется в том, что даже после минимального количества употребления метанола, в большинстве примеров наступит слепота или даже летальный исход.
Высокотоксичный продукт используется в промышленности и непригоден для перорального применения. Часто организм человека травится этой гадостью по собственной небрежности, когда путаются: этиловый и метиловый спирты. Часто метиловый спирт используют подпольные мини-заводы по производству спиртных напитков. Если пить такую паленую водку, значит, можно смело говорить о серьезном отравлении.
Первые признаки, симптомы отравления можно констатировать спустя 8 часов после употребления ядовитой жидкости. В некоторых случаях до 72 часов. Ранние симптомы отравления – расширенные зрачки, нарушение зрения. Другие признаки.
- Показания свидетелей, что пострадавший употреблял какую-то жидкость.
- Наличие подозрительной емкости.
- Запах спиртного изо рта человека.
- За короткое время организм претерпевает резкие перепады настроения: возбуждение, сонливость.
- Состояние пострадавшего выражено сонливостью, которая перетекает в бессознательность.
- Тошнота, рвота, неустойчивая походка, боли в животе.
- Тахикардия, судороги, мигрени.
Кроме того, двоение в глазах, боль в глазных яблоках, потеря зрения вплоть до полной слепоты. Такие симптомы явно указывают на отравление человека продуктами метила. Если подобные признаки налицо, требуется неотложная помощь.
Немедленная госпитализация
Попадая в желудок, яд действует как сильное токсическое вещество. Поражаются все ткани и органы тела. Он нарушает метаболизм, разрушает клетки. Так как свыше 80% всей жидкости выводится через мочеполовую систему, деструктируется, в первую очередь, она. По существу, организм за короткий срок, подвергается сильнейшему отравлению.
Если выпита смертельная доза и случай тяжелый, симптомы будут следующими:
- кожная текстура отливаются синим цветом;
- беспокойство;
- сильные болевые ощущения в подложечной области;
- приступы страха;
- неясное сознание;
- ощущение сдавленности в груди.
В последнем случае, симптомы даже не наблюдаются – это, когда у пострадавшего отмечают потерю сознания вплоть до комы и летального исхода. В домашних условиях антидот от такого отравления подобрать невозможно. Только неотложная медицинская помощь может спасти несчастного.
Первым долгом медики постараются удалить метиловый спирт из организма, скорректируют работу сердца, почек, дыхательной системы, направят усилия на борьбу с ацидозом. Фактически в каждом подобном случае, пострадавшего кладут в стационар, так как только в стенах клиники можно подобрать соответствующий антидот. Неотложная терапия ведется в реанимационном или токсикологическом отделении.
В больнице сделают промывание ЖКТ, пропишут обильное питье, проведут лечение щелочами. Первая помощь при отравлении метиловым спиртом дома – это лишь употребление теплой воды в большом количестве и вызывание рвотных масс. Больше с больным ничего делать не рекомендуется.
Также в клинике дадут этанол – он считается противоядием. Он снизит окисление метила и образование токсичных продуктов. Принимают антидот каждые четыре часа в течение нескольких суток из расчета 0.5мл на килограмм веса. Могут назначить внутривенно по 5% раствора и глюкозы. Лечат пострадавшего и другими средствами: соевое слабительное через зонд, согревают организм. Можно использовать от отравления и соматические вещества: Реополиглюкин, гидрокарбонат натрия, глюкозу (внутривенно). Против судорог: Оксибутират натрия с Унитилолом, Пирацетам. Важно помнить, что метиловый спирт настолько опасен для человека, что даже после выздоровления, выжившие становятся инвалидами на всю жизнь.
Метиловый спирт (метанол). Формула, характеристики и применение
Метиловый спирт (формула CH3OH) – это прозрачное и бесцветное жидкое вещество с характерным для этой группы веществ «спиртовым» запахом и небольшим удельным весом (литр спирта весит примерно 800 г). Данная жидкость относится к числу легко воспламеняемых реактивов, и обладает токсичными свойствами. Доза от 30-ти до 50-ти миллилитров является очень опасной для человеческого организма, и гарантированно приводит к утрате человеком зрительной функции. А доза, равная 100 миллилитрам, принятая внутрь, является смертельной.
Своей токсичностью метанол (сокращенное название вещества) принципиально отличается от этилового спирта – следующего представителя группы одноатомных спиртов, являющегося компонентом многих алкогольных напитков и некоторых продуктов питания. Обе эти жидкости имеют одинаковый внешний вид, схожий запах и даже идентичный вкус – резкий жгучий с некоторым сладковатым оттенком. Но, тем не менее, отличить их всё-таки можно, даже без применения лабораторных методов, а с помощью подручных средств.
Как отличить метиловый спирт от этилового
Существует два метода — один с помощью раскалённой медной проволоки, другой – с помощью термометра с достаточно длинной шкалой (не менее 80°C). Первый способ основан на том, что раскалённую докрасна медную проволоку помещают в спирт и по запаху испарений делают вывод о том, какой это спирт – метиловый или этиловый. Второй способ основан на физических свойствах обоих веществ, и заключается в нагревании исследуемого вещества до температуры кипения. У метилового спирта она составляет 60°C, для сравнения, у этилового спирта температура кипения 80°C.
Однако эти методы имеют немало недостатков. Их эффективность может с определённой долей достоверности подтверждена только в тех случаях, если в исследуемом растворе, спирта содержится более половины в процентном отношении. Поэтому самый точный ответ на вопрос о том, как определить метиловый спирт в алкоголе, возможен только один: с помощью лабораторных исследований, и никак не иначе. Проще говоря: напитки сомнительного происхождения и качества без их тщательной проверки употреблять крайне нежелательно!
Метиловый спирт. Получение
Производят метанол в промышленных целях посредством взаимодействия угарного газа (СО) и водорода (Н). Данное химическое взаимодействие происходит при повышенном давлении (порядка 7 атм.) и при температуре более 250°C с участием в реакции различных катализаторов. Данный метод в нынешних условиях считается наиболее прогрессивным в противовес более старым методам: переработке метана и методу сухой перегонки древесины с лигнином.
Метиловый спирт. Применение
И при всей своей токсичности и пожароопасности этот химикат был, есть и остаётся важнейшим сырьём для многих производств промышленного масштаба. Одним из главных свойств этого вещества является его высокая эффективность в качестве растворителя для многих химических соединений и материалов.
Его редко используют в чистом виде в качестве растворителя, заметно чаще этот реактив оказывается основой или одним из компонентов более сложных растворяющих веществ. Такие растворители используются при работе со многими лакокрасочными средствами и другими химическими веществами.
Также метиловый спирт используется в химической индустрии. Его используют при синтезировании формальдегида, уксусной кислоты, некоторых разновидностей эфиров и прочих веществ. Применяется метанол также и в лабораторно-исследовательских работах в качестве реактива для самых разнообразных направлений деятельности.
Востребован химикат в газодобыче, как средство для нейтрализации гидратов. Часто используется в производстве топлива для двигателей внутреннего сгорания в качестве присадки, повышающей октановое число. Да и сам этанол в чистом виде в некоторых случаях может использоваться в этом качестве, как топливо для определённых разновидностей ДВС.
Может использоваться данное вещество и в парфюмерной отрасли, как денатурирующий компонент для этилового спирта, часто применяемого при изготовлении парфюмерной продукции.
Интернет-магазин ХимЭлемент, всем своим клиентам, предоставляет возможность метиловый спирт (метанол) купить в нашей торговой сети на самых выгодных для вас условиях, гарантированно получив при этом товар самого высокого качества, и воспользовавшись возможностью доставки в любой населённый пункт Украины.
свойства, получение и применение :: SYL.ru
Введение
Вы пришли вечером с работы, переоделись, затем, соблюдая свою привычку, сели в кресло перед телевизором и включили канал с новостями в эфире. Диктор сначала вещает что-то невразумительное, а потом выдает что-то вроде: «И, наконец, главная новость дня. В таком-то городе произошло массовое отравление метиловым спиртом. Погибло несколько десятков человек, еще столько же госпитализированы». Ваш слух моментально уловил название незнакомого вам вещества — «метиловый спирт». Большинство людей узнает о его существовании именно таким образом. Некоторые быстро забудут данное словосочетание, а некоторые захотят узнать о нем побольше. Вот для них в этой статье я и опишу все свойства метилового спирта.
Определение
Метиловый спирт (формула СН3ОН) является простейшим одноатомным спиртом, первым представляющим гомологический ряд последних.
Название
В разных источниках его могут называть по-разному: и гидроксидом метила, и метанолом, и древесным спиртом, и карбинолом, и метилгидратом.
Получение метилового спирта
До 60-х годов ХХ века для синтезирования метилового спирта использовали только цинкохромовые, однако, позже этот опыт стали проводить на медьсодержащих катализаторах. Но сегодня его получают посредством каталитического синтеза из оксида углерода (II) и водорода при температуре 250С, давлении 7 мегапаскалей и определенных катализаторах (оксиде цинка и оксиде меди). До этого метиловый спирт получали сухой перегонкой дерева. Но сегодня этот способ является второстепенным. Для этой цели могут также использовать отходы нефтепереработки и коксующиеся угли.
Свойства
Метанол является бесцветной жидкостью, имеющей запах этилового спирта. Вода, этанол и эфир могут смешиваться с ним в любых отношениях. Сжимается и разогревается, когда его смешивают с водой. Также он имеет репутацию сильного растворителя и нередко может заменить этиловый спирт. Если в безводном метаноле растворить медный купорос, он становится голубовато-зеленого цвета. Из-за этого такой безводный купорос нельзя использовать, чтобы открыть следы воды в метиловом спирте. Метанол не может образовывать азеотропную смесь с водой, из-за этого смеси воды и метилового спирта могут быть разделены с помощью ректификационной перегонки. Метанол соединяется со многими солями, образуя сольваты. При реакции с едкой щелочью может давать алкоголяты.
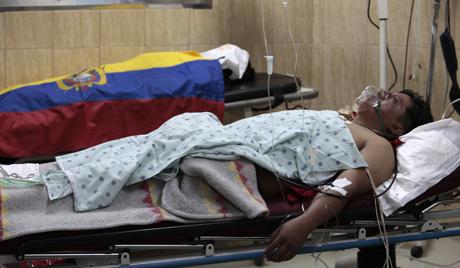 Метиловый спирт: отравление
Метиловый спирт: отравление
Метанол является сильнейшим ядом, его действию подвергаются нервная и сердечно-сосудистая системы. Отравление происходит из-за «летального синтеза» — метаболического окисления в организме, продуктом которого является очень ядовитый формальдегид. Тяжелое отравление наступает при попадании в организм 5-10 мл метилового спирта, а если это 30 или больше грамм — неизбежны слепота и/или летальный исход. Симптомы легкого отравления — это головная боль, общая слабость, недомогание, озноб, тошнота и рвота. Из-за этого опасными для жизни являются продукты даже с малейшей концентрацией метанола. Антидот при отравлении этим веществом — это этиловый спирт. Он вводится внутривенным или пероральным путями. Однако самим это делать не следует — при неправильных диагнозе и дозировке положение только ухудшится. Так что при подозрении на отравление метиловым спиртом необходимо срочно вызывать врача.
Применение
В газовой промышленности борьба с образованием гидратов не обходится без метилового спирта. С помощью него производят формальдегид, формалин, уксусную кислоту и целый ряд эфиров. Метанол используют при изготовлении растворителей для лаков. Он также может служить добавкой к жидким топливам для двигателей внутреннего сгорания и быть заправкой к мотоциклам и автомобилям. Из метилового спирта получают биодизель. Также в парфюмерии он — денатурирующая добавка к этанолу. Топливные элементы работают только благодаря окислению метанола в оксид углерода (IV) на катализаторе.
Заключение
Теперь вы знаете о метиловом спирте всё. И, как видите, несмотря на свою ядовитость, он может быть и очень полезным человеку, только при осторожном обращении с ним.
Метанол (метиловый спирт). Справка — РИА Новости, 01.06.2011
Метанол получают в промышленности восстановлением монооксида углерода при 400° С под давлением 20-30 МПа (мегапаскаль) в присутствии катализатора, состоящего из оксидов меди, хрома, и алюминия.
Метиловый спирт смешивается во всех соотношениях с водой, спиртами, ацетоном, бензолом; образует азеотропные смеси (смеси жидкостей, которые кипят при постоянной температуре и перегоняются без изменения состава) с ацетоном, бензолом, сероуглеродом, тетрахлорид углеродом и мн. др. соединениями.
До 1960-х гг. метиловый спирт синтезировали только на цинкхромовом катализаторе при 300-400°С и давлении 25-40 МПа. Впоследствии распространение получил синтез метилового спирта на медьсодержащих катализаторах (медьцинкалюмохромовом, медь‑цинкалюминиевом или др.) при 200-300°С и давлении 4-15 МПа.
Впервые метиловый спирт был выделен из продуктов сухой перегонки древесины Жаном Батистом Дюма и Эженом Пелиго, которые, сопоставив его свойства со свойствами винного спирта, дали первые представления о классе спиртов (1835). В 1857 г. французский химик Марселен Бертло синтезировал метиловый спирт омылением метилхлорида. Синтетический метиловый спирт начали получать с 1923 г.
Метанол используют как растворитель, а также в производстве формальдегида, применяемого для получения фенолформальдегидных смол. Большие объемы метанола используют при добыче и транспорте природного газа.
Его используют также для получения лекарственных веществ, как добавку к бензину и для получения бензина в целях экономии нефтяного сырья. Разрабатываются процессы получения из метилового спирта уксусного ангидрида, винилацетата, этанола, ацетальдегида, этиленгликоля и др. многотоннажных нефтехимических продуктов.
Метанол – наиболее токсичное соединение среди всех спиртов. Он окисляется в организме человека значительно медленнее, чем этиловый спирт, и в ходе его окисления образуются различные ядовитые вещества.
Метиловый спирт быстро всасывается в желудке и тонком кишечнике. Почти весь метанол (90%) метаболизируется в печени при помощи фермента алкогольдегидрогеназы, в результате чего образуются формальдегид и муравьиная кислота, обладающие высокой токсичностью. Метаболиты метанола удаляются почками, а меньшая часть (15%) в неизменном виде выделяется через легкие.
Метанол является сильным ядом преимущественно нервного и сердечно-сосудистого действия с выраженными кумулятивными свойствами. Токсическое действие метанола связано с угнетением центральной нервной системы, развитием тяжелого метаболического ацидоза (изменение кислотно-щелочного баланса организма), поражением сетчатки глаза и дистрофией зрительного нерва.
Острое отравление при вдыхании паров встречается редко. Опасен прием метанола внутрь: 5-10 мл могут вызвать тяжелые отравления и слепоту, а 30 мл — привести к смертельному исходу. Острое отравление характеризуется состоянием легкого опьянения, тошнотой, рвотой, сильной головной болью, резким ухудшением зрения вплоть до слепоты; при утяжелении состояния — цианоз (синюшная окраска кожи и слизистых оболочек), затрудненное дыхание, расширение зрачков, судороги и смерть от остановки дыхания.
Диагноз подтверждается обнаружением в моче муравьиной кислоты.
При очень больших дозах отравление может протекать в молниеносной форме, смерть наступает в течение 2-3 часов. Летальность при отравлении метиловым спиртом значительна.
Хронические отравления характеризуются головокружением, головной болью, бессонницей, повышенной утомляемостью, желудочно-кишечными расстройствами, болями в области сердца и печени, нарушением функции зрения, прежде всего цветного.
Материал подготовлен на основе информации открытых источников
алкоголя | Определение, формула и факты
Спирт , любой из класса органических соединений, характеризующихся одной или несколькими гидроксильными (OH) группами, присоединенными к атому углерода алкильной группы (углеводородной цепи). Спирты можно рассматривать как органические производные воды (H 2 O), в которых один из атомов водорода замещен алкильной группой, обычно представленной R в органических структурах. Например, в этаноле (или этиловом спирте) алкильная группа представляет собой этильную группу, ―CH 2 CH 3 .
Спирты относятся к наиболее распространенным органическим соединениям. Они используются в качестве подсластителей и в парфюмерии, являются ценными промежуточными продуктами в синтезе других соединений и являются одними из наиболее широко производимых органических химикатов в промышленности. Возможно, два самых известных спирта — это этанол и метанол (или метиловый спирт). Этанол используется в туалетных принадлежностях, фармацевтических препаратах и топливе, а также для стерилизации больничных инструментов. Кроме того, это алкоголь в спиртных напитках.Анестезирующий эфир также производится из этанола. Метанол используется как растворитель, сырье для производства формальдегида и специальных смол, в специальных топливах, в антифризах и для очистки металлов.
Спирты можно разделить на первичные, вторичные или третичные, в зависимости от того, какой углерод алкильной группы связан с гидроксильной группой. Большинство спиртов представляют собой бесцветные жидкости или твердые вещества при комнатной температуре. Спирты с низким молекулярным весом хорошо растворяются в воде; с увеличением молекулярной массы они становятся менее растворимыми в воде, и их температура кипения, давление пара, плотность и вязкость повышаются.
Получите эксклюзивный доступ к контенту нашего 1768 First Edition с подпиской. Подпишитесь сегодняВ этой статье рассматриваются структура и классификация, физические свойства, коммерческое значение, источники и реакции спиртов. Для получения дополнительной информации о близкородственных соединениях см. химическое соединение, фенол и эфир.
.Завод этанола, метанола, спирта, этанола, метанола, спирта OEM / ODM, производственная компания
Всего найдено 102 завода и компаний по производству этанола и метанола с 306 продуктами. Получите высококачественный этанол-метанол-спирт из нашего огромного набора надежных заводов по производству этанола-метанола. Золотой член| Тип бизнеса: | Торговая компания |
| Основные продукты: | Спирт , пропиленгликоль, глицерин, сложный эфир, диметилкарбонат |
| Mgmt.Сертификация: | ISO 9001, ISO 9000 |
| Собственность завода: | Общество с ограниченной ответственностью |
| Объем НИОКР: | OEM, ODM, собственный бренд |
| Расположение: | Тонглинг, Аньхой |
| Тип бизнеса: | Производитель / Factory |
| Основные продукты: | Ледяная уксусная кислота, серная кислота, метилэтилкетон, диметилформамид, безводный сульфат натрия |
| Mgmt.Сертификация: | ISO 9001 |
| Объем НИОКР: | OEM, ODM, собственный бренд |
| Расположение: | Циндао, Шаньдун |
| Производственные линии: | Больше 10 |
| Тип бизнеса: | Производитель / Factory |
| Основные продукты: | Нетканая маска, карбомер, карбопол, , этанол , перборат натрия |
| Mgmt.Сертификация: | ISO 9001 |
| Собственность завода: | Общество с ограниченной ответственностью |
| Объем НИОКР: | OEM, ODM, собственный бренд |
| Расположение: | Шицзячжуан, Хэбэй |
| Тип бизнеса: | Производитель / Factory , Торговая компания |
| Основные продукты: | Полипропиленовое волокно, ПВА для бетона, акриловая смола, полиамидная смола CPP для чернил, геосетка, геотекстиль, геоячейка, |
| Mgmt.Сертификация: | ISO 9001, GMP |
| Собственность завода: | Общество с ограниченной ответственностью |
| Объем НИОКР: | OEM, ODM |
| Расположение: | Хэфэй, Аньхой |
| Тип бизнеса: | Торговая компания |
| Основные продукты: | Органические химические вещества, неорганические химические вещества |
| Mgmt.Сертификация: | ISO 9001, ISO 9000, ISO 20000 |
| Собственность завода: | Общество с ограниченной ответственностью |
| Объем НИОКР: | OEM |
| Расположение: | Вэйфан, Шаньдун |
| Тип бизнеса: | Производитель / Factory |
| Основные продукты: | Фармацевтические промежуточные продукты, органические промежуточные продукты, ежедневные химикаты, Этанол , косметические материалы |
| Mgmt.Сертификация: | ISO 9001, ISO 9000, ISO 14001, ISO 14000, ISO 20000 … |
| Собственность завода: | Общество с ограниченной ответственностью |
| Объем НИОКР: | OEM, ODM, собственная торговая марка, Guanlang |
| Расположение: | Шицзячжуан, Хэбэй |
Метанол — Википедия
Метанол | ||
| Структурная формула и молекулярная модель | ||
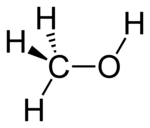 | ||
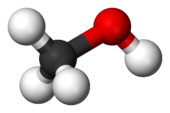 | ||
| Алгемин | ||
| Молекулярная формула | СН 3 ОН | |
| IUPAC-naam | метанол | |
| Имя Андере | метиловый спирт, хуталкоголь, марочный спирт, хутгест, гидроксиметан | |
| Молмасса | 32,04 г / моль | |
| УЛЫБКИ | CO | |
| ИнЧИ | 1 / Ch4OH / c1-2 / h3H, 1h4 | |
| Номер CAS | 67-56-1 | |
| Номер EG | 200-659-6 | |
| PubChem | 887 | |
| Beschrijving | Kleurloze giftige vloeistof | |
| Vergelijkbaar met | этанол, 1-пропанол | |
| Waarschuwingen en veiligheidsmaatregelen | ||
| Gevaar | ||
| H-zinnen | h325 — h401 — h411 — h431 — h470 | |
| EUH-zinnen | geen | |
| P-zinnen | P210 — P260 — P280 — P301 + P310 — P311 | |
| Омганг | Uitsluitend te gebruiken in een goed geventileerde ruimte, bij voorkeur een zuurkast.Бидж контакт встретил de huid afspoelen met veel water. Bij inslikken из контактов встретил de ogen onmiddellijk een arts waarschuwen. | |
| Опслаг | In een afgesloten fles in een goed geventileerde ruimte. Verwijderd houden van warmte en ontstekingsbronnen. | |
| LD 50 (ratten) | 5628 мг / кг | |
| LD 50 (konijnen) | 14200 мг / кг | |
| Fysische eigenschappen | ||
| Агрегатный стенд | vloeibaar | |
| Kleur | клеурлоос | |
| Дихтейд | 0,7914 г / см³ | |
| Smeltpunt | −93,9 ° С | |
| Кукпунт | 64,96 ° С | |
| Влампунт | 11 ° С | |
| Zelfontbrandings- temperatuur | 470 ° С | |
| Поехал оплосбаар в | вода | |
| Brekingsindex | 1,33 (589 нм, 20 ° C) | |
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K при 25 ° C, 1 бар). | ||
Метанол из метиловый спирт (в Бельгии около марочный спирт ) представляет собой гетероэнвудигстовый спирт в форме брутоформулы CH 4 O.
Метанол wordt vaak tot de primaire alcoholen gerekend, maar hoort daar volgens de strikte Definitie niet bij. Het kenmerk van primaire alcoholen — это то, что вам нужно, чтобы вода была прямо на вашем месте OH-groep zitten и bij methanol zijn dater drie.
Bijcoholische gisting van mengsels waarin zich pentosen (vijfwaardige suikers), zoals arabinose, bevinden kan methanol als bijproduct ontstaan (suikers zoals maltose en глюкоза zijn zeswaardig, oftewel hexosen). De vijfwaardige suiker xylose ontstaat bij afbraak van hemicellulose. Wanneer deze pentosen meegisten en er gisten aanwezig zijn die deze suikers kunnen omzetten (lang niet alle giststammen doen dit) ontstaat er (ook) метанол. De meeste ongelukken met methanol gebeuren echter door het consumer van spiritus, vaak omdat bij sommigen de mythe leeft dat men de methanol eruit kan filteren of door eenvoudige destillatie kan verwijderen.Filteren is niet mogelijk en voor zuivering door destillatie is een gefractioneerde destillatie met een aanzienlijk scheidend vermogen nodig, omdat de kookpunten van ethanol en methanol vrij dicht bij elkaar liggen.
Метанол представляет собой синтетический продукт, содержащий химические вещества, химические вещества и биомассу.
Метанол wordt tevens gemaakt uit aardgas (hoofdzakelijk methaan) en stoom en over een nikkel-katalysator geleid, waarbij stoom in overmaat aanwezig находится в een verhouding van 3: 1.
Aardgas wordt dan gekraakt bij ongeveer 840 ° C:
- Ch5 + h3O⟶CO + 3h3 {\ displaystyle {\ ce {Ch5 + h3O -> CO + 3 h3}}}
Een deel van het gevormde koolstofmonoxide reageert verder met de stoom:
- CO + h3O⟶CO2 + h3 {\ displaystyle {\ ce {CO + h3O -> CO2 + h3}}}
Deze reacties zijn hoofdzakelijk endotherm. Dit mengsel wordt vervolgens gecomprimeerd to 100 bar en over een koper-katalysator geleid. De hoge druk — это nodig om het evenwicht van de reacties te verschuiven naar rechts (principe van Le Chatelier).Hierdoor reageren koolstofmonoxide en waterstofgas met elkaar to methanol:
- CO + 2h3⟶Ch4OH {\ displaystyle {\ ce {CO + 2 h3 -> Ch4OH}}}
Альтернативная реакция — это смесь диоксида туссена с водой и газом. Deze kan gebruikt worden om CO 2 uit de atmosfeer te recycleren:
- CO2 + 3h3⟶Ch4OH + h3O {\ displaystyle {\ ce {CO2 + 3 h3 -> Ch4OH + h3O}}}
Deze reacties zijn hoofdzakelijk exotherm. De ontstane ruwe methanol wordt via destillatie gezuiverd, waarbij de nevenproducten water, alkanen en ethanol verwijderd word.
Sinds 2012 производит CRI в Гриндавике (Эйленд), метанол с CO 2 и вода для газа. Het waterstofgas wordt middels электролизирует электрическую дверь, используя ее nabijgelegen geothermische elektriciteitscentrale. De Beoogde jaarproductie составляет 50 000 литров на банку. Hoewel deze fabriek de naam draagt van nobelprijswinnaar Джордж Эндрю Олах, gebruikt deze niet het process waarvoor Олах самен встретился с Робертом Анисфельдом в 1994 году. [1]
Нобельпрайсвиннаар Джорджа Эндрю Олаха и Роберта Анисфельда ван де Университета Южной Калифорнии в 2008 году его производство на основе метанола в анфигелеиде, метанол, метанол, андерс, дан Люхт. [2] Meer bepaald zouden de koolstofdioxide en de waterdamp uit de lucht (als bron van waterstof) gebruikt kunnen worden voor de productie van метанол. Этот процесс превращается в жидкость. Dit process (Welke uiteraard ook een energiebron nodig heeft) wordt nog nergens toegepast.
Метанол производится в химической промышленности. Daarnaast kan het ook gebruikt worden als energiebron, op zichzelf of bijgemengd in brandstoffen.
Enkele chemische toepassingen van methanol zijn:
В het kader van de toenemende schaarste aan fossiele brandstoffen находится метанол een van de stoffen die zou kunnen worden gebruikt om energie chemisch op te slaan en te transporteren.Boven Waterstof здорового метанола het voordeel, что het veel gemakkelijker en veiliger op te slaan en te transporteren. Het zou zowel in verbrandingsmotoren als direct in elektrische brandstofcellen kunnen worden gebruikt. Компания Toshiba разработала в 2005 году фирменный стиль, связанный с использованием мобильного телефона, с использованием скрытого соединения, метанола и метанола. Метанол может быть использован как вода для воды для производства марок (bijvoorbeeld в автомобилях).De zo geproduceerde waterstof zou goedkoper zijn dan wanneer pure waterstof meegenomen wordt in speciale tank en het kan langer opgeslagen worden zonder verliezen. Метанол wordt gebruikt bij de productie van biodiesel.
Метанол представляет собой органический оплосмидный элюент.
Метанол — это подарок бижутерии: een van de gevolgen is blindheid en eventueel de dood. Дозировка составляет 25 грамм. Het wordt toegevoegd aan spiritus. Om die reden — это spiritus ondrinkbaar en hoeft er geen drankaccijns over te worden betaald.Bij ondeskundige bereiding vancohol ontstaat weleens methanol als bijproduct, waardoor een zeer gevaarlijke пил ontstaat.
De vergiftigingsverschijnselen van methanol lijken enigszins op dronkenschap door ethanol en zijn zelfs over het algemeen lichter dan die bij een soortgelijke hoeveelheid этанол. Na ongeveer 30 uur zal de ophoping van mierenzuur (hoofdzakelijk in de vorm van formiaationen) ten gevolge van de oxidatie van de methanol in het lichaam leiden to een giftige bloedspiegel.De geïntoxiceerde kan plotseling het gezichtsvermogen geheel of gedeeltelijk verliezen en sterft bij een voldoende hoge dosis aan ademstilstand.
Een extreem voorbeeld van het gevaar находится на 15 декабря 2011 года в Индии, в Менштаре Западной Бенгалии, 143 doden vielen als gevolg van het drinken van незаконный подарить алкоголь. [4] Op 19 декабря 2016 года на Русском стадионе Иркецк, 49 доден на хет-пью-ван-бэдолие с метанолом. [5] В феврале 2019 года overleden meer dan 130 mensen na het drinken van een пил метанол и метанол в Ассаме, Индия. [6]
,