Радиация вокруг нас: чего стоит бояться?
Підпис до фото,В этом году над 4-м энергоблоком обрушилась часть крыши, но выброса радиации не было
Накануне Дня Чернобыльской трагедии ВВС Украина выяснила, какие источники радиации существуют в быту, как уберечься от вредных последствий облучения и стоит ли сейчас бояться Чернобыля.
Нашими собеседниками стали Игорь Каденко, доктор физико-математических наук, заведующий кафедрой ядерной физики Университета Шевченко, и Александра Кравец, доктор биологических наук, старший научный сотрудник Института клеточной биологии и генетической инженерии НАНУ.
Что такое радиация?
Хотя в широком смысле радиацией называют любой вид электромагнитного излучения, например, видимый свет, обычно этим термином обозначают так называемое ионизирующее излучение.
Термин «ионизирующее» означает, что энергии излучения достаточно, чтобы превратить нейтральные атомы вещества в положительно или отрицательно заряженные ионы.
К ионизирующему излучению относят рентгеновские и гамма-лучи с малой длиной волны, а значит — высокой частотой, и потоки некоторых микрочастиц.
«Чем меньше длина волны, тем оно (излучение. — Ред.) более опасно с точки зрения возможности проникновения через какое-то препятствие или защиту», — объясняет доктор физико-математических наук Игорь Каденко.
Однако, говорит ученый, опасность для организмов составляют лишь значительные объемы такого излучения.
«Когда вы ходите по улице, на вас сверху падает куча разного излучения: нейтронов, гамма-квантов, других заряженных частиц, но мы же от этого никуда не денемся», — добавляет он.
Угрожает ли украинцам радиация из Чернобыля?
Сегодня уровень радиации с Чернобыльской станции украинцам практически не угрожает, поскольку вредное излучение ограничено укрытием над 4-м энергоблоком, говорит доктор биологических наук Александра Кравец.
С ней соглашается и Игорь Каденко, однако добавляет, что здание укрытия не плотное, и именно поэтому там строят новый конфайнмент.
«Потенциальная возможность утечки радиации есть — например, в результате обвала. И такой случай уже был, — добавляет ученый. — После того, как в феврале над 4-м энергоблоком частично обрушилась крыша, уровень радиации вокруг станции не повысился».
Кроме того, говорит доктор Кравец, теоретически через щели в укрытии наружу может выходить радиоактивная пыль.
Однако резкого выброса радиации с ЧАЭС ожидать не стоит, поскольку внутри разрушенного блока работают защитные системы, которые прибивают пыль и могут разбрызгивать вещества, которые остановят несанкционированный ядерный распад.
Підпис до фото,В Чернобыльской зоне есть как полностью чистые от радиации участки, так и частично загрязненные, говорят ученые
Какие существуют источники радиации в быту?
Вредный источник радиации в быту — это рентген-аппарат. Рентгеновские лучи имеют более низкую частоту, чем гамма-лучи, однако в больших дозах способны навредить организму.
Рентгеновские лучи имеют более низкую частоту, чем гамма-лучи, однако в больших дозах способны навредить организму.
Ученые советуют делать рентгенные снимки только в случаях, когда это действительно необходимо для здоровья.
Естественным источником радиации также является солнечный свет, однако в большинстве случаев он не представляет угрозы для здоровья.
Мобильные телефоны, Wi-Fi станции и другие устройства связи не являются источниками радиации, поскольку работают в микроволновом диапазоне, частота которого ниже, чем частота видимого света.
Однако в последние годы влияние мобильников на здоровье человека стало предметом многих научных исследований. В 2011 году Международное агентство по исследованию рака заявило, что мобильные телефоны, возможно, являются канцерогенными, однако для подтверждения этого нужно провести широкое обстоятельное исследование.
После такого заявления ВОЗ уточнила, что «на сегодня не установлено никаких неблагоприятных последствий для здоровья, вызванных использованием мобильных телефонов».
И все же г-жа Кравец предостерегает, что излучение от мобильного телефона может вредить здоровью. Она советует сразу после набора номера держать трубку подальше от уха, так как в этот момент интенсивность излучения от телефона высокая.
Как вредные дозы радиации влияют на организм?
Когда облучается живое существо, это повышает уровень активных форм кислорода в клетках тела, объясняет Александра Кравец.
Обычный кислород видоизменяется в формы, которые могут разрушать макромолекулы клеток — ДНК и белки.
Большинство негативных последствий связаны именно с повреждением ДНК, объясняет ученый.
Повреждения ДНК происходят в организме все время, но обычно их мало, и они могут устранять защитные системы клетки. Однако когда уровень повреждений превышает критический, это приводит к серьезным сбоям в работе клеток.
Некоторые повреждения ДНК могут передаваться по наследству, но это очень редкий процесс, и вероятность наследственных нарушений очень низкая, говорит доктор Кравец.
«Таких высоких доз облучения, которые привели бы к заметному росту наследственных заболеваний, не получили ни украинцы, ни японцы (после аварии на Фукусиме — Ред.)», — говорит Александра Кравец.
Как защитить организм от вредного влияния радиации?
Підпис до фото,Ежедневное употребление капусты поможет предотвратить нежелательные изменения в ДНК
«Я считаю, что независимо от того, угрожают ли украинцам последствия Чернобыля, нам всем нужно вести здоровый образ жизни», — говорит Кравец.
Под здоровым образом жизни она подразумевает занятия спортом, активное движение, контроль над весом тела и богатую минералами диету, в которой преобладают неочищенные крупы.
Доктор биологических наук, г-жа Кравец предлагает разработанную ею диету для защиты от радиации, которая состоит из трех шагов.
1. Сделать все для того, чтобы организм усваивал меньше радионуклидов. Для этого нужно обеспечить его всеми возможными биогенными минералами, прежде всего — калием и кальцием. Эти минералы есть в изобилии в овощах и неочищенных крупах и злаках, таких, как гречка, овсянка, коричневый рис. Ученая также советует есть хлеб из муки грубого помола. 2. Обеспечить ферменты, которые защищают организм от активных форм кислорода, необходимыми для них микроэлементами: цинком, медью, селеном, серой, марганцем и железом. Продукт «номер один» на этом этапе — подсолнечные и тыквенные семечки, богатые железом и магнием. Источником серы является чеснок, а меди, которой особенно не хватает в полесских почвах, — шпинат. Многие антиоксиданты содержатся также в моркови. Красное вино тоже обладает антиоксидантным свойством, говорит доктор Кравец, однако не слишком высоким. 3. Стимулировать восстановительные процессы ДНК. Для этого также нужны цинк, железо и магний, которые есть в семечках, неочищенных злаках и крупах. Предотвратить изменениям в ДНК помогают также все виды капусты: белокочанная, брокколи, брюссельская или цветная.
Эти минералы есть в изобилии в овощах и неочищенных крупах и злаках, таких, как гречка, овсянка, коричневый рис. Ученая также советует есть хлеб из муки грубого помола. 2. Обеспечить ферменты, которые защищают организм от активных форм кислорода, необходимыми для них микроэлементами: цинком, медью, селеном, серой, марганцем и железом. Продукт «номер один» на этом этапе — подсолнечные и тыквенные семечки, богатые железом и магнием. Источником серы является чеснок, а меди, которой особенно не хватает в полесских почвах, — шпинат. Многие антиоксиданты содержатся также в моркови. Красное вино тоже обладает антиоксидантным свойством, говорит доктор Кравец, однако не слишком высоким. 3. Стимулировать восстановительные процессы ДНК. Для этого также нужны цинк, железо и магний, которые есть в семечках, неочищенных злаках и крупах. Предотвратить изменениям в ДНК помогают также все виды капусты: белокочанная, брокколи, брюссельская или цветная.
«Нужно употреблять как можно более простые продукты», — заключает доктор Кравец.
Стоит ли бояться радиации?
«Мое персональное впечатление, что радиация безопасна в пределах установленных норм. Я бы никому не хотел пожелать, чтобы люди ее боялись. Поэтому мое персональное впечатление, что именно страх может вызвать проблемы. Не радиация, а именно страх», — говорит доктор Каденко , заведующий кафедрой ядерной физики в украинском университете.
Кафедру создали в 1945 году, рассчитывая, что она поможет в развитии программы ядерных вооружений СССР. Естественно, что в таком месте сосредоточено много приборов, работа которых связана с радиоактивным излучением.
Через кафедру, рассказывает ученый, прошло много людей, которые всю свою жизнь работали там и оставались здоровыми.
«У меня работает сотрудник, который участвовал в Великой Отечественной войне, летал на самолете и бомбил Кенигсберг. Ему сейчас 87 лет. Человек ходит на работу, он очень активный, я не знаю, что бы я делал без него», — рассказывает Игорь Каденко.
При этом завкафедрой говорит, что ни один из его коллег не превышает разрешенных 20 миллизивертов облучения в год.
«Никогда, это абсолютно исключено. Это очень жестко, и за несоблюдение соответствующих норм есть уголовная ответственность», — говорит он.
Как питаться на загрязненных радиацией территориях
Воздействие радиации на организм
Санэпидслужба на пострадавших территориях систематически проводит контроль продуктов питания, воды, почвы на содержание радионуклидов, исключает из реализации через торговые сети те продукты, которые содержат радионуклиды в количествах, превышающих предельно допустимые уровни. Однако далеко не все продукты можно проверить. И, к сожалению, все люди следуют советам врачей. Многие продолжают есть грибы, рыбу, дичь, овощи, фрукты без какого-либо контроля, тем самым увеличивая риск проникновения в организм радиоактивных веществ.
Поэтому первый и самый основной совет, касающийся особенностей питания людей, проживающих на загрязненных территориях: не используйте в пищу продукты, которые не прошли должного контроля!
Как быть, если человек постоянно находится в условиях действия малых и предельно допустимых доз радиации? Можно ли как-то уменьшить или исключить вредные последствия?
И сразу же небольшая оговорка: в медицине до сих пор нет единых представлений о вредном влиянии на здоровье малых доз радиации.
Отсюда второй совет тем, кто живет в загрязненных радионуклидами зонах: постарайтесь увеличить в своем рационе долю продуктов и пищевых веществ, повышающих антиокислительную (антиоксидантную) защиту организма.
Какие продукты есть
Это прежде всего витамины С, А, Е, бетакаротин. Исследования также выявили, что и при достаточном потреблении витаминов с пищей их дефицит у различных групп населения в зоне загрязнения достаточно выражен. У 91% обследованных, к примеру, обнаружено недостаточное обеспечение организма витамином С, почти у каждого пятого — бетакаротином, а у каждого десятого — витамином Е.
У 91% обследованных, к примеру, обнаружено недостаточное обеспечение организма витамином С, почти у каждого пятого — бетакаротином, а у каждого десятого — витамином Е.
Повышена потребность населения радиоактивных зон и в витаминах группы В: В2, В6 уменьшающих чувствительность организма к ионизирующему облучению. Поэтому всем постоянно проживающим на загрязненных территориях необходимо принимать поливитаминные препараты — ежедневно 2–3 драже. Это активизирует противолучевую сопротивляемость организма.
Другие пищевые вещества, оказывающие радиозащитное действие, — аминокислоты, содержащие серу. Это цистин, цистеин, метионин. Наиболее богаты ими белок яйца, творог, сыр, рыба, мясо, бобовые. Было бы хорошо эти продукты в разных сочетаниях ежедневно включать в рацион.
И третий совет: организм должен постоянно и в достаточных количествах получать пищевые волокна.
Пищевые волокна содержатся во всех растительных продуктах. Но особенно много таких волокон в отрубях, овсяной, гречневой крупе, моркови, свекле, яблоках, сухофруктах, морской капусте, орехах. Пищевые волокна прочно связывают радионуклиды и выводят их из организма. Исследования показали, что ежедневное потребление оптимального количества (до 30–35 граммов) пищевых волокон способствует снижению общей радиоактивности организма на 10–15% в течение месяца.
Пищевые волокна прочно связывают радионуклиды и выводят их из организма. Исследования показали, что ежедневное потребление оптимального количества (до 30–35 граммов) пищевых волокон способствует снижению общей радиоактивности организма на 10–15% в течение месяца.
Выведение радионуклидов стронция и цезия усиливают минеральные вещества, особенно кальций и калий. Кальция много во всех молочных продуктах (кроме сливочного масла, сметаны, сливок), а калия — в картофеле, капусте, тыкве, кабачках, абрикосах, персиках, сухофруктах (курага, изюм, чернослив). Минеральные щелочные воды — неплохие источники необходимых минеральных веществ.
Самые ранние симптомы воздействия радиации на организм проявляются обычно нарушениями системы кроветворения. Для их профилактики рекомендуется систематически включать в рацион источники гемового железа (мясо, печень, рыбу, креветки), а также петрушку, укроп, сельдерей, салат. Содержащаяся в зеленных культурах фолиевая кислота принимает участие в процессе кроветворения.
Особым радиозащитным эффектом обладает микроэлемент селен. В виде фармпрепарата он продается в аптеках. После совета с лечащим врачом его можно принимать как дополнительное лечебно-профилактическое средство для повышения радиопротекторных возможностей организма.
На ряде территорий, подвергшихся радиационному загрязнению, в почве содержится мало йода. Для восполнения этого хронического дефицита специалисты советуют не пренебрегать продуктами, богатыми йодом: разнообразными дарами моря, особенно морской капустой в натуральном, консервированном или сушеном виде, а также йодированной солью.
Как готовить пищу
Важно знать, что лечебно-профилактическое действие продуктов во многом зависит от их кулинарной обработки и правильного режима питания, особенно если нет уверенности в экологической чистоте овощей, грибов, рыбы, мяса… Предпочтительный способ приготовления еды — варка. При такой более щадящей термической обработке продуктов (в сравнении с жаркой, копчением) в меньшей мере теряются биологически активные вещества.
Еще одна тонкость: если варить, допустим, картофель в предварительно посоленной воде и без кожуры, в несколько раз увеличивается выведение из него радионуклидов. То же и с другими овощами. При жарке, копчении радионуклиды в продуктах сохраняются.
Режим питания
Лучше есть 4–5 раз в день, так, чтобы большая часть калорийности рациона приходилась на первую половину дня. Избегайте чересчур горячих блюд, обжигающих слизистую рта, пищевода, желудка. Жиры добавляйте в готовые блюда.
Итог: как питаться на зараженных радиацией территориях
Пищевой рацион живущих в зоне загрязнения должен включать всевозможные источники животного белка (мясо, рыбу, яйца, сыр, творог, кисломолочные продукты, говяжью печень, кальмары, креветки) в разных сочетаниях — 3–4 разных продукта в течение дня; хлебобулочные изделия из муки грубого помола; крупы и овощи с высоким содержанием пищевых волокон, солей калия, витаминов группы В — овсяную, гречневую каши, морковь, свеклу, тыкву, кабачки, помидоры, огурцы, картофель, морскую капусту, зелень, пищевые пшеничные отруби в разных сочетаниях — 3–4 блюда в день; фрукты, сухофрукты, ягоды, фруктовые и овощные соки, минеральные воды — в разных сочетаниях 1 —2 раза в день.
Профилактика рака: Воздействие радиации
Воздействие радиации на рабочем месте
Первая злокачественная опухоль – рак кожи, вызванная радиацией, была диагностирована в 1902 г. у рентгенологов. Далее было показано, что у радиологов повышен риск лейкозов, миеломной, а также большинства солидных опухолей. Однако принятие защитных мер значительно снизило риск опухолей среди представителей этой профессии.
Риск развития рака легкого у шахтеров, связанный с высокой концентрацией в шахтах радиоактивного газа радона, изучался в ряде работ, проведенных в Чехословакии, США, Швеции, Китае. Во всех этих исследованиях показано значительное повышение риска смерти от рака легкого. Кривая доза-эффект имела строго линейный характер.
Данные о повышенном риске развития злокачественных опухолей среди работников различных ядерных установок противоречивы. Большинство эпидемиологических исследований, основанных на наблюдении за этими контингентами, не выявили повышения заболеваемости, а в ряде из них выявлен «дефицит» заболевания раком, что можно объяснить т.н. эффектом
Результаты последних исследований, в которые были включены первичные данные работников различных ядерных предприятий США и Канады, говорят, скорее, о снижении риска рака в результате эффекта «здорового рабочего», чем о его повышении. Нужно подчеркнуть, что доза радиации, полученная работниками на этих предприятиях, не превышала 5 сГр (0,05 Гр). Кооперативное исследование, в которое были включены американские и английские данные по 76 тыс. работникам ядерных установок, показало, что только 9 из 3976 случаев злокачественных опухолей можно связать с радиацией.
работникам ядерных установок, показало, что только 9 из 3976 случаев злокачественных опухолей можно связать с радиацией.
Риск злокачественных опухолей у населения, проживающего вблизи ядерных установок
Рост заболеваемости и смертности предприятия «Маяк», как известно, связан с загрязнением реки Течи радиоактивными выбросами этого предприятия. К сожалению, оценить количественно степень канцерогенного риска, которому подверглось это население, скорее всего, уже невозможно. В то же время мы располагаем результатами исследований, которые проводились в разных странах вокруг ядерных предприятий. В большинстве этих работ не удалось выявить повышения заболеваемости и смертности от рака. В некоторых исследованиях было выявлено небольшое повышение заболеваемости злокачественными опухолями среди детей. Однако в большинстве случаев эти находки не подтвердились.
На основании исследований, проведенных в Англии, было высказано предположение, что у детей, проживающих по соседству с ядерным предприятием в городке Селлафильд, повышена заболеваемость лейкозом.
Применение ионизирующей радиации в медицине
Первые данные о канцерогенности ионизирующей радиации получены в результате наблюдения за больными, которые часто подвергались воздействию радиации. Наблюдение за когортой женщин, больных туберкулезом, показало, что частое флюорографическое обследование, применявшееся для контроля над пневмотораксом, одним из методов лечения туберкулеза, приводило через 10–15 лет после начала лечения к повышению риска рака молочной железы. Наиболее высокие показатели риска были зафиксированы у женщин, которым частое флюорографическое обследование производилось в подростковом и детском возрасте. Рост ОР в зависимости от дозы облучения носил линейный характер. Показано, что облучение молочной железы дозой в 1 Гр увеличивает риск рака этого органа на 60%. Необходимо отметить, что молочная железа – один из наиболее радиочувствительных органов, степень которой зависит от возраста. Так, в период роста и развития радиочувствительность молочной железы выше, чем после 50 лет.
Наблюдение за когортой женщин, больных туберкулезом, показало, что частое флюорографическое обследование, применявшееся для контроля над пневмотораксом, одним из методов лечения туберкулеза, приводило через 10–15 лет после начала лечения к повышению риска рака молочной железы. Наиболее высокие показатели риска были зафиксированы у женщин, которым частое флюорографическое обследование производилось в подростковом и детском возрасте. Рост ОР в зависимости от дозы облучения носил линейный характер. Показано, что облучение молочной железы дозой в 1 Гр увеличивает риск рака этого органа на 60%. Необходимо отметить, что молочная железа – один из наиболее радиочувствительных органов, степень которой зависит от возраста. Так, в период роста и развития радиочувствительность молочной железы выше, чем после 50 лет.
Данные о канцерогенном риске, связанном с маммографией, указывают на то, что, несмотря на возможное небольшое повышения риска развития рака молочной железы, в результате облучения (поглощенная железой доза обычно равна 3 мГр) в конечном счете этот тип обследования снижает смертность от рака этого органа. Расчеты, проведенные в Швеции, показали, что маммографический скрининг 100 тыс. женщин в возрасте 50-69 лет в результате облучения может привести к смерти от рака молочной железы от 1 до 5 женщин. В то же время в результате скрининга смертность от рака молочной железы снизилась на 25%, т.е. в результате скрининга были сохранены жизни 560 женщин.
Расчеты, проведенные в Швеции, показали, что маммографический скрининг 100 тыс. женщин в возрасте 50-69 лет в результате облучения может привести к смерти от рака молочной железы от 1 до 5 женщин. В то же время в результате скрининга смертность от рака молочной железы снизилась на 25%, т.е. в результате скрининга были сохранены жизни 560 женщин.
При скрининге рака легкого с использованием низкодозовой спиральной КТ эффективная доза составляет 0,2-1 МэВ, которая может привести к развитию 1-5 случаев смерти от рака на 100 тыс. обследуемых.
Дозы облучения при других методах лучевой диагностики, в частности, флюорографии, выше. Поэтому принятие решения о каждой дополнительной лучевой диагностической процедуре должно быть обосновано.
Лучевая терапия повышает риск возникновения второй злокачественной опухоли у онкологических больных. Повышение риска лейкоза и лимфомы отмечено у больных, получивших радиотерапию по поводу рака шейки и тела матки и лимфогранулематоза. Лучевая терапия рака молочной железы также повышает риск рака легкого. По-видимому, эта же причина в определенной мере способствует и частому развитию рака второй молочной железы. На основании тщательного анализа роли лучевой терапии в возникновении вторых опухолей было сделано заключение, что радиотерапия ответственна за 5-10% всех вторых опухолей. Роль же других факторов, в т.ч. химиотерапии, гормонального статуса, а в большей степени факторов образа жизни, которые причинно были связаны и с первыми опухолями, а именно курение, потребление алкоголя, питание, представляется более значимой.
Лучевая терапия рака молочной железы также повышает риск рака легкого. По-видимому, эта же причина в определенной мере способствует и частому развитию рака второй молочной железы. На основании тщательного анализа роли лучевой терапии в возникновении вторых опухолей было сделано заключение, что радиотерапия ответственна за 5-10% всех вторых опухолей. Роль же других факторов, в т.ч. химиотерапии, гормонального статуса, а в большей степени факторов образа жизни, которые причинно были связаны и с первыми опухолями, а именно курение, потребление алкоголя, питание, представляется более значимой.
Наблюдение за детьми, облученными по поводу ретинобластомы, выявило значительное повышение у них риска опухолей костей, мягких тканей, ЦНС и меланомы. Как известно, ретинобластома часто сочетается с вышеперечисленными опухолями, однако радиация еще больше повышает риск их развития.
Риск злокачественных опухолей, связанный с воздействием радона в помещениях
Радон-222 является источником половины всей дозы ионизирующего излучения, получаемого человеком из естественных источников, и составляет в среднем 1,15 мЗв/г. Однако уровень экспозиции радону значительно варьирует и может превышать средний в десять и более раз. Как известно, у шахтеров в результате воздействия радона значительно повышен риск рака легкого. Однако уровень радона в жилых помещениях значительно ниже, чем в шахтах, и поэтому изучение канцерогенного воздействия радона в помещениях крайне трудно.
Однако уровень экспозиции радону значительно варьирует и может превышать средний в десять и более раз. Как известно, у шахтеров в результате воздействия радона значительно повышен риск рака легкого. Однако уровень радона в жилых помещениях значительно ниже, чем в шахтах, и поэтому изучение канцерогенного воздействия радона в помещениях крайне трудно.
Метаанализ эпидемиологических исследований, проведенных в разных странах, показал, что ОР рака легкого, связанный с воздействием радона в жилых помещениях, равен 1,2, а процент рака легкого, который этиологически связан с этим фактором, не превышает 2%. Необходимо подчеркнуть, что высокие уровни радона характерны для Домов из камня и особенно гранита, а также для первых этажей домов, построенных в скалистой местности.
Отдаленные последствия аварии на Чернобыльской АЭС
Эпидемиологические исследования отдаленных последствий аварии на ЧАЭС выявили достоверное повышение риска рака щитовидной железы среди детей. Это повышение частично может быть объяснено эффектом скрининга. Однако большая часть этих случаев, несомненно, связана с радиацией. Количество детей в Белоруссии, России и на Украине, которым в 1986-2000 гг. был поставлен диагноз, рак щитовидной железы, составило 1800. Рост заболеваемости раком щитовидной железы был наиболее выражен в Гомельской области — в регионе, жители которого получили наиболее высокие дозы радиации, в частности, радиоактивного йода (131I), экспозиция которому предшествовала экспозиции другим радиоактивным веществам, в частности, изотопам цезия. Заболеваемость раком щитовидной железы выросла и среди детей, проживавших в наиболее загрязненных районах России и Украины. Подтверждением причинной связи между аварией на ЧАЭС и ростом заболеваемости раком щитовидной железы у детей является исследование методом «случай-контроль», проведенное в Белоруссии, в которое были включены 107 детей, больных раком щитовидной железы, 107 детей, представляющих популяционную контрольную группу, и 107 детей, которые участвовали в популяционном скрининге и у которых не было выявлено патологии щитовидной железы.
Это повышение частично может быть объяснено эффектом скрининга. Однако большая часть этих случаев, несомненно, связана с радиацией. Количество детей в Белоруссии, России и на Украине, которым в 1986-2000 гг. был поставлен диагноз, рак щитовидной железы, составило 1800. Рост заболеваемости раком щитовидной железы был наиболее выражен в Гомельской области — в регионе, жители которого получили наиболее высокие дозы радиации, в частности, радиоактивного йода (131I), экспозиция которому предшествовала экспозиции другим радиоактивным веществам, в частности, изотопам цезия. Заболеваемость раком щитовидной железы выросла и среди детей, проживавших в наиболее загрязненных районах России и Украины. Подтверждением причинной связи между аварией на ЧАЭС и ростом заболеваемости раком щитовидной железы у детей является исследование методом «случай-контроль», проведенное в Белоруссии, в которое были включены 107 детей, больных раком щитовидной железы, 107 детей, представляющих популяционную контрольную группу, и 107 детей, которые участвовали в популяционном скрининге и у которых не было выявлено патологии щитовидной железы. ОР рака щитовидной железы был в шесть раз выше у детей, которые получили дозу радиации более 1 Гр, по сравнению с получившими дозу менее 0,3 Гр, и эта разница была статистически достоверна. Исследователи отмечают, что рак щитовидной железы у детей, связанный с аварией на ЧАЭС, почти исключительно имеет папиллярное гистологическое строение, опухоли чаще возникают у детей, которые подверглись воздействию радиации до 5 лет, и что латентный период между воздействием радиации и развитием рака необычайно короток.
ОР рака щитовидной железы был в шесть раз выше у детей, которые получили дозу радиации более 1 Гр, по сравнению с получившими дозу менее 0,3 Гр, и эта разница была статистически достоверна. Исследователи отмечают, что рак щитовидной железы у детей, связанный с аварией на ЧАЭС, почти исключительно имеет папиллярное гистологическое строение, опухоли чаще возникают у детей, которые подверглись воздействию радиации до 5 лет, и что латентный период между воздействием радиации и развитием рака необычайно короток.
Результаты эпидемиологических исследований, в которых изучалась связь межу аварией на ЧАЭС и раком щитовидной железы у взрослых, менее убедительны. Тем не менее, в двух когортах ликвидаторов, которые наблюдались в Эстонии и России, выявлено повышение заболеваемости раком щитовидной железы по сравнению с ожидаемой заболеваемостью, основанной на статистике рака щитовидной железы в Эстонии и России. Необходимо отметить, что подобное сравнение правомочно, однако, учитывая проблемы популяционной статистики вообще и особенно в России, где, несомненно, имеется недоучет больных злокачественными опухолями и особенно опухолями щитовидной железы, результаты такого сравнения a priori должны быть положительными.
Данные эпидемиологических исследований не указывают на связь между аварией на ЧАЭС и заболеваемостью лейкозом у детей. Эпидемиологическое исследование, в котором изучалась динамика заболеваемости лейкозами и лимфомами детей в 23 странах, не выявило связи между небольшим ростом заболеваемости лейкозом, который был отмечен исследователями, и радиацией. Аналогичные исследования на Украине, в Белоруссии, Финляндии не выявили роста заболеваемости детским лейкозом. Исследования динамики заболеваемости лейкозом взрослого населения в наиболее загрязненных регионах Украины и Белоруссии не выявили роста заболеваемости, которую можно было бы объяснить воздействием радиации. Однако повышение риска острого лейкоза было отмечено среди ликвидаторов, получивших наибольшие дозы радиации.
Риск злокачественных опухолей, связанный с космической радиацией
Эта проблема привлекла внимание исследователей относительно недавно. Риску, связанному с этим источником радиации, в большей степени подвергаются экипажи реактивных самолетов. Экипажи, выполняющие пассажирские рейсы, получают в год в среднем 3-6 мЗв, а военные летчики – около 9 мЗв. Эпидемиологические исследования этих контингентов выявили увеличения риска рака кожи и меланомы, злокачественных опухолей, которые могут быть связаны и с повышенной экспозицией солнечным лучам в нерабочее время. Кроме того, у женщин – членов экипажей реактивных самолетов – выявлено повышение риска рака молочной железы, которое также можно объяснить особенностями репродуктивного анамнеза стюардесс, в частности, поздними первыми родами и отсутствием детей. В одной работе, проведенной в Дании, показано повышение риска смерти от лейкоза.
Экипажи, выполняющие пассажирские рейсы, получают в год в среднем 3-6 мЗв, а военные летчики – около 9 мЗв. Эпидемиологические исследования этих контингентов выявили увеличения риска рака кожи и меланомы, злокачественных опухолей, которые могут быть связаны и с повышенной экспозицией солнечным лучам в нерабочее время. Кроме того, у женщин – членов экипажей реактивных самолетов – выявлено повышение риска рака молочной железы, которое также можно объяснить особенностями репродуктивного анамнеза стюардесс, в частности, поздними первыми родами и отсутствием детей. В одной работе, проведенной в Дании, показано повышение риска смерти от лейкоза.
Существующие гигиенические нормы допустимых уровней радиации вполне удовлетворительны с точки зрения современных знаний о канцерогенном эффекте ионизирующей радиации. Сказанное не исключает необходимости систематического мониторирования радиоактивности в окружающей среде и, в первую очередь, на территориях, прилегающих к АЭС и другим атомным предприятиям.
«Линия Сталина»: смертельная радиация ДОТов Карельского укрепрайона
ДОТ №26. Фото: Виктор Терешкин
Зона
В нее нас ведет сталкер. Его зовут Антон Коломицын. Ему 40 лет, он худой, поджарый и может спать на снегу, без костра. В минус 30. В поисках приключений он побывал в 26 регионах России. Это его образ жизни. На адреналине. Он идет так быстро, что мы с экспертом по атомным проектам Экологического правозащитного центра «Беллона» Алексеем Щукиным то и дело отстаем. Антон легко ныряет под наклонившиеся деревья и на ходу рассказывает.
– В укрепрайоне 230 ДОТов. Он протянулся по старой финско-советской границе от Финского залива до Ладоги. Входил в «Линию Сталина». В 1993 году военные отсюда ушли и бросили все оборонительные сооружения на произвол судьбы. А внутри ДОТов, капониров осталось до фига самого разного железа. В них постоянно бывает много людей – дети с окрестных садоводств, «геокэшеры», поисковики, грибники, «фортификаторы», «металлисты». «Металлисты» спиливают все, что могут там, куда можно подъехать на машине. Очень часто лазал по ДОТам и я. Много лет. И только 22 января догадался замерить уровни радиации. Мой дозиметр ИРД-02 способен регистрировать не только гамма-, но так же альфа- и бетта-излучение. Когда я увидел, что при замере радиационного фона, он зашкаливает за пределы измерения по альфа-излучению, решил срочно написать в «Беллону». Ведь нужно бить тревогу!
«Металлисты» спиливают все, что могут там, куда можно подъехать на машине. Очень часто лазал по ДОТам и я. Много лет. И только 22 января догадался замерить уровни радиации. Мой дозиметр ИРД-02 способен регистрировать не только гамма-, но так же альфа- и бетта-излучение. Когда я увидел, что при замере радиационного фона, он зашкаливает за пределы измерения по альфа-излучению, решил срочно написать в «Беллону». Ведь нужно бить тревогу!
«Кубок экстремальных условий». Фото: Виктор Терешкин
Щукин держит включенным профессиональный дозиметр-радиометр МКС-01 СА1М. Прибор мерно пощелкивает. Если он уловит скачок гамма-фона – щелчки участятся. И тут же приятный женский голос предупредит «Внимание!» – если гамма-фон будет от 60 до 120 микрорентген в час (мкР/час). А уж если голос скажет: «Опасно!», значит гамма-излучение уже выше, чем 120 микрорентген в час. И на экране выскочат соответствующие цифры.
Замечаю, что мы идем по тропе, занесенной снегом. Что вдоль тропы на елях есть полоски красного полиэтилена. Подходим к ДОТу №26 – так он обозначен на карте укрепрайона. Рядом с садоводством «Перемяки». Вижу, что прямо за ДОТом на ели висит какое-то объявление. Прошу коллег подождать, лезу по снегу, читаю – «Кубок экстремальных условий». Мда, нашли себе кубок на собственную… голову. Вечером этого дня прочитаю в Интернете на информационном портале об активном отдыхе креативчик: «Кубок экстремальных условий – невозможно устоять на ногах!».
Что вдоль тропы на елях есть полоски красного полиэтилена. Подходим к ДОТу №26 – так он обозначен на карте укрепрайона. Рядом с садоводством «Перемяки». Вижу, что прямо за ДОТом на ели висит какое-то объявление. Прошу коллег подождать, лезу по снегу, читаю – «Кубок экстремальных условий». Мда, нашли себе кубок на собственную… голову. Вечером этого дня прочитаю в Интернете на информационном портале об активном отдыхе креативчик: «Кубок экстремальных условий – невозможно устоять на ногах!».
Сталкер и Щукин стоят у входа в ДОТ. У Щукина встревоженное лицо – дозиметр уже не мерно щелкает, он заходится от щелчков. Мы еще не вошли внутрь, а гамма-фон уже повышен. Что же будет внутри? По спине бежит холодок. Включаем налобные фонарики. Я дополнительно включаю мощный охотничий. Заходим в тесный ДОТ. Дозиметр стрекочет как оглашенный. Проходит минута и приятный женский голос сообщает:
– Два и три десятых миллирентген в час. Опасно!
Алексей встревожено:
– Мужики, работаем быстро. И быстро уходим. Тут худо. Нормальный фон – 15-20 микрорентген в час.
И быстро уходим. Тут худо. Нормальный фон – 15-20 микрорентген в час.
Переключает прибор в режим замера альфа-излучения. Подносит его станку, где стоял пулемет «Максим». Над ржавыми железками полукруглый бетонный выступ. На нем металлическая пластина. С нее лохмотьями свисает светосостав постоянного действия. Дозиметр сходит с ума. Свечу фонариком на пол. Прямо под пластиной пол усыпан ошметками светомассы. Дозиметр показывает – 30 000 альфа-частиц в минуту с квадратного сантиметра.
– Это предел его измерения альфа-частиц – быстро говорит наш эксперт. – Всё, валим!
Выскакиваем из опасной зоны, отходим метров на двадцать. Жадно закуриваем.
Эксперт Алексей Щукин и Антон Коломицын спешат от фонящего ДОТа. Фото: Виктор Терешкин
– В этих ДОТах практически все «светит», – предупреждает сталкер. – Ничего нельзя касаться. Я вчера был в ДОТе на Лемболовских высотах, рядом с комплексом «Лемболовская твердыня». Случайно схватился за металлическую ручку на пулеметном станке. Потом замерил перчатку – 1500 альфа-частиц.
Потом замерил перчатку – 1500 альфа-частиц.
– А зачем воякам этот опаснейший СПД понадобился в ДОТах? – спрашиваю я. – Ведь от часов со светящимися точками рядом с каждой цифирькой, лупит около шести тысяч микрорентген в час. А тут пластины шириной сантиметров в сорок и длиной в метр. Да еще СПД не пожалели – ведь миллиметра в два толщиной намазюкали.
– Да кто ж теперь скажет, – тянет Антон, дымя как паровоз. – Я наводил справки, говорят – какие-то опыты вели. Было это в начале 60-ых. При модернизации ДОТов. Как версия – на эту металлическую пластину прикрепляли тонкую бумагу, на которой были нанесены цели, с указанием расстояния. Чтоб пулеметчик быстрее мог начать стрельбу. Свет в ДОТы давали по кабелям от подземной электростанции. А в тех, куда кабель дотянуть не смогли, СПД использовали как подсветку. Но это – версия. Вся информация по укрепрайону до сих пор засекречена. Сколько из 230 ДОТов в «грязи» еще предстоит узнать.
Из досье «Беллоны.ру»: До 1970-х годов на шкалы различных приборов наносился светосостав постоянного действия (СПД), содержащий соли Радия-226. В отличие от фосфора такой состав светился десятилетиями, постепенно теряя яркость. Область применения была разнообразна: часы, компасы, авиаприборы, вольтметры, амперметры, манометры, тумблеры, прицельные приспособления, шкалы в военных установках, новогодние игрушки, настенные картины и др.
В отличие от фосфора такой состав светился десятилетиями, постепенно теряя яркость. Область применения была разнообразна: часы, компасы, авиаприборы, вольтметры, амперметры, манометры, тумблеры, прицельные приспособления, шкалы в военных установках, новогодние игрушки, настенные картины и др.
Поскольку по химическим свойствам Радий-226 похож на кальций, то, попадая в организм, он накапливается в костных тканях, вызывая рак костей. Это долгоживущий элемент (его период полураспада составляет 1600 лет). Кроме рака костей, радий вызывает такое заболевание, как анемия, поскольку он воздействует на костный мозг.
ДОТ № 66 у ручья Ядки. Фото: Виктор Терешкин
СПД может иметь разные оттенки, но чаще всего преобладают желтые. В полнейшей темноте приборы с покрытием СПД 60-х годов выпуска все еще продолжают светиться.
«Фонят» сильнее всего те приборы, где СПД нанесено больше всего. Как видим, это шкалы измерительных приборов (выдают более 6000 мкР/ч). На расстоянии в полтора метра фон уже практически в норме.
На расстоянии в полтора метра фон уже практически в норме.
Следует отметить, что при распаде Радий-226 выделяет радиоактивный газ Радон-222, который легко попадает в легкие.
ДОТ у ручья Ядки
Вчера вместе со сталкером Антоном и экспертом Щукиным мы вновь поехали в Зону. Дот №66 стоит на склоне у ручья Ядки. Его пулеметы должны были простреливать всю долину ручья, грунтовую дорогу, мост на ней и шоссе. Метрах в пятидесяти от долговременной огневой точки расположено садоводство «Марс». И ясно, что летом мальчишки и девчонки садоводства днюют и ночуют в этом притягивающим как магнит месте. Хороший знакомый Антона, узнав от него, что в ДОТе бешеные уровни радиации, схватился за голову: я же туда не раз детей водил.
ДОТ № 66. Февраль 2017 года. Альфа-частиц 30 000. Предел измерений для дозиметра. Фото: Виктор Терешкин
Наш эксперт Алексей Щукин на этот раз экипировался, как положено, – на нем респиратор. Мы со сталкером полезли в опасный ДОТ без них. Ну, конченые идиоты. Здесь СПД с металлической пластины и не думал падать. Замеры показали, что гамма-фон внутри долговременной огневой точки – 23 миллирентгена в час. При замере альфа частиц дозиметр дошел до предела измерения – 30 000. Страшно представить, какая катастрофа разразится, если какой-нибудь пацан решит эту пластину содрать и привезет домой, в Питер. И сам получит смертельную дозу и всех друзей, которым похвастается – «во какая военная штука, должна светиться», переоблучит. И квартира вся «засветит». Ручей оправдает свое название.
Мы со сталкером полезли в опасный ДОТ без них. Ну, конченые идиоты. Здесь СПД с металлической пластины и не думал падать. Замеры показали, что гамма-фон внутри долговременной огневой точки – 23 миллирентгена в час. При замере альфа частиц дозиметр дошел до предела измерения – 30 000. Страшно представить, какая катастрофа разразится, если какой-нибудь пацан решит эту пластину содрать и привезет домой, в Питер. И сам получит смертельную дозу и всех друзей, которым похвастается – «во какая военная штука, должна светиться», переоблучит. И квартира вся «засветит». Ручей оправдает свое название.
Выскочили мы из ДОТа очень быстро. Отошли на безопасное расстояние, и я попросил Алексея Щукина прокомментировать уровни радиоактивного загрязнения.
Дозиметр считает гамма-излучение. Светосостав практически цел. Фото: Виктор Терешкин
– 23 мР/час – в 1000 раз больше естественного фона. По альфа частицам – зашкал прибора – более 30 000 частиц/кв см*мин. Опасно для всего живого.
Опасно для всего живого.
В этот же день мы обследовали еще один ДОТ. Его номер 61. Он находится рядом с домом по улице 16 аллея СНТ «Аист». Владельцы дома используют долговременную огневую точку как погреб. Алексей Щукин и сталкер Антон провели замеры.
– Тут все чисто, – сказал Алексей Щукин. – Все объясняется просто. В ДОТ был подведен кабель. Я видел довоенные плафоны.
– Слава Богу, – сказал хозяйка дома Людмила Абакумова. – А вам, ребята, спасибо большое. Успокоили.
«Эти уровни смертельно опасны!»
В этом уверен Юрий Щукин. Много лет он возглавлял Комиссию радиационного контроля. Комиссия радиационного контроля Ленгороблисполкомов (КРК) закрыла регион от поступления чернобыльской «грязи».
– На ваш взгляд, те уровни, которые мы сегодня замерили, 23 миллирентгена в час, и 30 000 альфа-частиц, а дальше дозиметр уже измерять не может, они…
– Они смертельно опасны! В Нормах Радиационной Безопасности (НРБ 99/10) прописано, что даже на поверхности в рабочих помещениях, где профессионалы и те пребывают временно, должно быть не больше сотни частиц, а тут 30 тысяч, а раз прибор больше не может замерить – там больше. Намного. Но это внешнее излучение, вся проблема в том, насколько СПД сыпется, самое главное – составляющая аэрозолей, не фон альфа-частиц. Для того чтобы понять, насколько велика опасность, надо было взять мазок с поверхности пола, механизмов в ДОТе. Слегка намочить ватку и провести по поверхности, потом провести замер. Ту цифру, которую покажет прибор, специалисты называют «снимаемое загрязнение». Вот оно – самое страшное. Каждый, кто к механизмам прикасался, перенес это загрязнение на кожу ладоней. И если это попадет в желудок, вот тут начнутся большие проблемы со здоровьем.
Намного. Но это внешнее излучение, вся проблема в том, насколько СПД сыпется, самое главное – составляющая аэрозолей, не фон альфа-частиц. Для того чтобы понять, насколько велика опасность, надо было взять мазок с поверхности пола, механизмов в ДОТе. Слегка намочить ватку и провести по поверхности, потом провести замер. Ту цифру, которую покажет прибор, специалисты называют «снимаемое загрязнение». Вот оно – самое страшное. Каждый, кто к механизмам прикасался, перенес это загрязнение на кожу ладоней. И если это попадет в желудок, вот тут начнутся большие проблемы со здоровьем.
– Рядом с этим ДОТом, буквально в 50 метрах стоят дома садоводства, поэтому в ДОТе часто бывают дети, ну как же – такое приключение, старый ДОТ, железяки, которые можно покрутить. Сталкер Антон крутил при мне рукоятки принудительной вентиляции ДОТа. Она гудела. Рукоятки были ржавые. Какой соблазн для пацанов.
– Я про это и говорю – если это загрязнение снимаемое, если СПД уже разрушилось, специалисты называют это – радий поплыл, вот это уже страшно. Гамма-фон 23 миллирентгена – это очень нехорошо, но это не смертельно.
Гамма-фон 23 миллирентгена – это очень нехорошо, но это не смертельно.
Юрий Щукин. Фото: Виктор Терешкин
– Вы говорили, что было постановление правительства СССР об изъятии приборов с СПД. В том числе и в министерстве обороны. Это было в 70-ые годы, я брал у Вас интервью в 1989 году, и Вы говорили, что военные выполнили требование постановления чрезвычайно небрежно.
– Это было в 70-ые годы. КРК пришлось проводить спецоперацию на Балтийском военном флоте, на нем вспомогательные суда все были старые, в машинных отделениях у них было много приборов с СПД. И КРК занималась их изъятием. Эта большая операция длилась три года. И все офицеры прекрасно понимали опасность СПД. Прекрасно все знали. И администрация города высказала командованию БФ своё «фэ». После выхода постановления правительства офицеры министерства обороны стали приборы изымать, но так халатно, что тысячи приборов попало на свалки. Так образовались мощные пятна радиоактивной грязи. Мы изымали эти приборы по школам, Дворцам пионеров, кружкам юных моряков.
Мы изымали эти приборы по школам, Дворцам пионеров, кружкам юных моряков.
– Как вы расцениваете то, что в 1993 году военные уходили из Карельского укрепрайона и не сняли металлические пластины с СПД? В этом есть признаки халатности? Служебной недобросовестности?
– Конечно, есть.
– А если ребенок побывал в таком брошенном ДОТе. Да не раз, не два, не три – как это может сказаться на его здоровье?
– Это будут страшные последствия. Военные должны проводить тотальную проверку всех, кто живет рядом с такими ДОТами, вычислять, кто мог попасть в них, но не живет в садоводствах. Зоны вокруг радиоактивных ДОТов должны закрываться, и нужно проводить дозиметрическое обследование всех и вся. Мы в свое время на полтора года задержали открытие нового корпуса военного училища на улице, параллельной Московском проспекту. В корпусе старого училища были пятна «грязи» от приборов с СПД, стекол на них не было, светосостав стал осыпаться, курсанты на подошвах растащили эту «грязь» по коридорам старого училища, а потом и нового. И мы потом эту «грязь» отмывали. Очень тяжелая, муторная работа. И здесь будет такая же. Ведь «грязь» могли растащить по дачам, домам, квартирам в Петербурге.
И мы потом эту «грязь» отмывали. Очень тяжелая, муторная работа. И здесь будет такая же. Ведь «грязь» могли растащить по дачам, домам, квартирам в Петербурге.
Чтобы ядерная энергетика процветала, нам нужно изменить образ мыслей о радиации
Ядерная энергетика должна расти — и расти быстро, — если страны мира хотят иметь хоть какую-то надежду на ограничение роста выбросов углекислого газа.
Но рост ядерной энергетики сдерживается рядом факторов, включая стоимость и длительные сроки лицензирования и строительства новых реакторов. Эти высокие затраты и длительные сроки могут быть в значительной степени связаны с одной проблемой: чрезмерным страхом людей перед радиацией. Этот чрезмерный страх перед радиацией препятствует масштабному развертыванию ядерной энергетики во всем мире, и при этом он мешает как богатым, так и бедным странам извлекать выгоду из единственного лучшего источника дешевой, безуглеродной энергии с высокой плотностью мощности, известного науке.
Несмотря на этот страх — и ошибочное убеждение, что любая радиация опасна, — истина заключается в том, что мы постоянно подвергаемся воздействию радиации из нашего окружения. На самом деле радиация, которую мы получаем от полетов на реактивных лайнерах или компьютерной томографии, так же велика, или даже больше, чем радиация, поглощаемая людьми, живущими вблизи Чернобыля или Фукусимы.
Джеральдин Томас читает лекцию в Аделаиде, Южная Австралия, в 2016 годуЭто те моменты, которые доктор Джеральдин Томас, директор Чернобыльского Банка тканей, рассказывает в течение многих лет. Джерри, как она предпочитает, чтобы ее называли, имеет докторскую степень в области патологии и является членом факультета в Имперском колледже Лондона. С начала 1990-х годов она руководила сбором и хранением образцов тканей людей, перенесших операцию после облучения в зоне радиоактивных осадков вблизи Чернобыльской АЭС на севере Украины. Ее работа в Чернобыле и Фукусиме дает ей уникальную квалификацию для оценки рисков, связанных с радиацией. В 2011 году она написала статью в газете Guardian о том, что после аварии на АЭС «Фукусима» люди стали бояться радиации.
В 2011 году она написала статью в газете Guardian о том, что после аварии на АЭС «Фукусима» люди стали бояться радиации.
«Недавнее безумие, последовавшее за событиями в Японии, говорит о том, что средства массовой информации стремятся подпитывать наши ядерные страхи сосредоточение внимания на воздействии радиации, которое крайне маловероятно приведет к одной смерти, по сравнению с природной катастрофой, в результате которой погибло по меньшей мере 20 000 человек и было перемещено более 100 000 человек».
«Радиационный риск должен быть поставлен в контекст. Последствиями для наиболее уязвимой группы выживших после атомной бомбардировки стала средняя продолжительность жизни, значительно меньшая, чем потеря в результате ожирения или курения».
Во время недавнего выпуска подкаста Power Hungry Томас сказала, что большинству людей трудно понять дозировку радиации и то, что составляет опасную дозу. Количество радиации, которое человек получает от компьютерной томографии всего тела, составляет около 10 миллизивертов, что, по ее словам, примерно такая же доза, которую получают люди, живущие вблизи Чернобыля, но она «распределяется на протяжении 20 с лишним лет».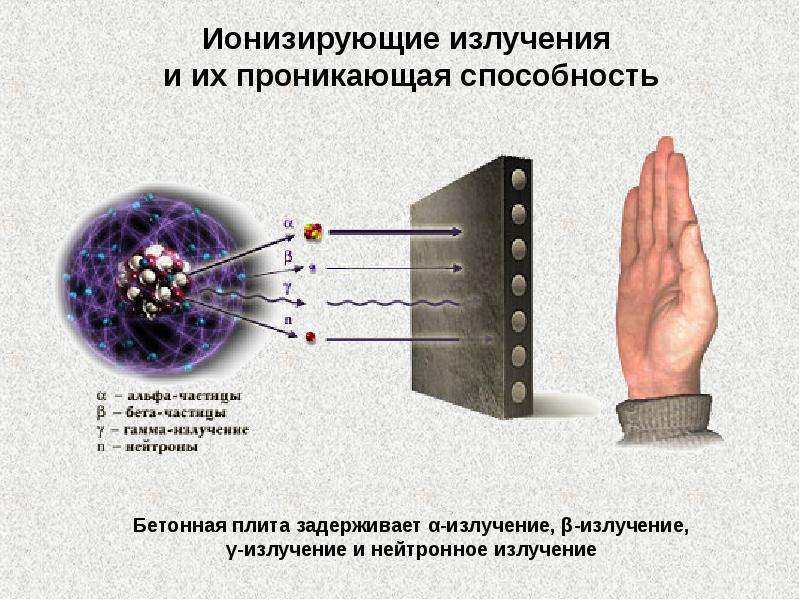
Почему мы так боимся радиации?
«Ты не можешь почувствовать ее вкус, ты не можешь почувствовать ее запах, ты не можешь увидеть ее», — говорит Джеральдин. «И ее нельзя обнаружить, если у вас нет дозиметра. Добавьте сюда десятилетия нагнетания страха различными источниками и слияние ядерной энергии с ядерным оружием, и легко понять, почему люди боятся».
Томас считает, что наш страх перед радиацией — «это запрограммированный страх»… Есть что-то в глубине вашего сознания, что говорит: «Ты уверен?», потому что нас столько лет заставляли бояться даже самой маленькой дозы радиации, что на самом деле требуется полный разворот мышления, чтобы понять это.
Томас говорит, что ленивая журналистика — это одна из причин, почему публика стала так бояться радиации. До аварий на Чернобыльской АЭС и Фукусиме она говорила, что медицинские эксперты по радиации «никогда не приблизятся к журналисту, потому что им нельзя доверять». Понимание радиации требует понимания «сложностей воздействия на здоровье». А как насчет экологических групп, таких как Greenpeace и Sierra Club, которые являются категорически антиядерными? (На своем веб-сайте Sierra Club сообщает, что во время добычи и переработки урана «радиоактивность выбрасывается по всему пути».) Насколько они виновны?
А как насчет экологических групп, таких как Greenpeace и Sierra Club, которые являются категорически антиядерными? (На своем веб-сайте Sierra Club сообщает, что во время добычи и переработки урана «радиоактивность выбрасывается по всему пути».) Насколько они виновны?
Томас тактично отвечает: «Я не люблю сбивать с толку зеленых защитников окружающей среды. Но я бы хотел, чтобы они посмотрели на науку».
Десятилетия шумихи вокруг возможной опасности радиации привели к созданию протоколов безопасности, которые резко увеличили стоимость проектирования, лицензирования и строительства новых атомных станций. Тот же самый страх привел к десятилетиям споров по поводу хранения и утилизации отработавших топливных стержней и других радиоактивных материалов, производимых атомными электростанциями.
Томас непреклонно выступает за ядерную энергию.
«Я не думаю, что у нас есть большой выбор, если мы хотим декарбонизировать должным образом», — сказала она.
— «Есть несколько причин, по которым вам понадобится ядерная энергия. Первое: она не прерывистая. Другое дело, что это производит большое количество энергии, которую вы могли бы использовать для электролиза и получения водорода».
Этот водород можно было бы затем использовать для транспортировки и в промышленности. Но будущее таких проектов, как Sizewell C, а также развертывание небольших модульных реакторов, зависит от того, чтобы убедить общественность в ее чрезмерном страхе перед радиацией. Как говорит Томас, это потребует «изменения менталитета» среди общественности и политиков. Но если мы собираемся добиться прогресса в развертывании ядерной энергетики в масштабе тераватт — и, следовательно, в сокращении выбросов парниковых газов, — то этот поворот мышления должен произойти, и очень скоро.
Кафедра рентгенологии и радиационной медицины
Заведующий кафедрой
доктор медицинских наук, профессор Амосов Виктор Иванович
Контактная информация
Тел. : (812) 338 6303, 338 6308
: (812) 338 6303, 338 6308
Ответственные:
- за учебную работу: Кишковская Елена Альбертовна тел.: (812) 338 6301
- за научную работу: Лукина Ольга Васильевна тел.: (812) 338 6301
Кафедра расположена в 58 корпусе, на 2 этаже
Лечебно-диагностические отделения:
Отделение рентгеновской компьютерной томографии №1:
Руководитель отделения — к.м.н. Бобров Евгений Игоревич
Заведующий отделением — Морозов Алексей Николаевич
Отделение рентгеновской компьютерной томографии №2:
Руководитель отделения — д.м.н. Лукина Ольга Васильевна
Заведующий отделением — Сорочинский Сергей Петрович
Отделение рентгеновской компьютерной томографии №3:
Заведующая отделением — Соловьева Елена Николаевна
Отделение совмещенной позитронно-эмиссионной и компьютерной томографии:
Заведующий отделением — Христолюбов Александр Владимирович
Радиологическое отделение:
Заведующий отделением — Литвинов Андрей Петрович
История кафедры
Кафедра рентгенологии и радиационной медицины основана в 1945 году на базе доцентских курсов, которыми руководили профессор М. И.Неменов и профессор Г.А. Зедгенидзе. Читать далее
И.Неменов и профессор Г.А. Зедгенидзе. Читать далее
Содержание дисциплины, учебные программы
Балльно-рейтинговая оценка усвоения дисциплины «Лучевая диагностика» на лечебном факультете
Домашнее задание к практическим занятиям по лучевой диагностике для студентов лечебного факультета
План практических занятий по лучевой диагностике для студентов 3 курса лечебного факультета
Последипломная подготовка
Циклы повышения квалификации и профессиональной переподготовки:
Повышение квалификации по специальности «Рентгенология»: «Мультиспиральная компьютерная томография в многопрофильной клинике» — 144 часа.
Повышение квалификации в рамках непрерывного медицинского образования по специальности «Рентгенология», «Радиология», «Терапия», «Пульмонология», «Торакальная хирургия», «Хирургия», «Общая врачебная практика(семейная медицина»: «Мультиспиральная компьютерная томография в пульмонологии» — 36 часов.
Научная деятельность
Научно- исследовательская деятельность кафедры проходит под руководством заведующего кафедрой профессора, д.м.н. Амосова В.И. Сотрудниками кафедры, в тесном сотрудничестве с другими подразделениями Университета, разрабатываются следующие основные темы:
Основными темами научной работы кафедры в период с 2008 по 2013 годы являются:
- Лучевая диагностика заболеваний органов дыхания.
- Лучевая диагностика заболеваний опорно- двигательного аппарата.
- Лучевая диагностика заболеваний челюстно — лицевой области и зубо-челюстных деформаций.
- Лучевая диагностика заболеваний ЛОР-органов.
- Возможности МСКТ – ангиографии в диагностике заболеваний различных органов и систем в условиях многопрофильной клинике.
- Возможности применения современных гибридных технологий (ПЭТ-КТ, ОФЭКТ –КТ)
Согласно вышеперечисленным темам разрабатываются программы научных семинаров и проводятся научно- практические конференции с участием сотрудников кафедры, рентегенологического, радиологического отделений и отделения рентгеновской и магнитно- резонансной хирургии.
На кафедре рентгенологии и радиационной медицины утверждена программа подготовки очных и заочных аспирантов по специальности 14.01.13 – лучевая диагностика, лучевая терапия.
Основными подразделениями на базе которых выполняются названные выше темы научной работы являются – радиологическое отделение, отделение магнитно-резонансной и компьютерной томографии, отделение кабинеты клиник университета. Необходимо подчеркнуть, что научные исследования проводятся в тесной интеграции с другими клиническими кафедрами и научно-исследовательскими институтами Университета. Внедрение в практику современных методик лучевой диагностики позволило начать разработку новых научно-исследовательских тем совместно с кафедрами акушерства и гинекологии, госпитальной хирургии №1, госпитальной хирургии №2, факультетской хирургии, общей хирургии, госпитальной терапии, факультетской терапии, рентгенорадиологии факультета постдипломного обучения, офтальмологии, оториноларингологии, патофизиологии, неврологии и нейрохирургии, хирургической стоматологии.
Дополнительная информация
Анкета интерна
Расписание прохождения практики в качестве рентгенлаборанта
Распределение интернов по кабинетам
Штат кафедры
Заведующий кафедрой: д.м.н., профессор Амосов Виктор Иванович
Профессор:
д.м.н. Сперанская Александра Анатольевна
Доценты:
к.м.н Кишковская Елена Альбертовна,
к.м.н. Бобров Евгений Игоревич,
д.м.н. Лукина Ольга Васильевна.
Ассистенты:
Христолюбов Александр Владимирович,
Литвинов Андрей Петрович,
Осипов Николай Петрович,
Малкова Мария Юрьевна,
к.м.н. Брызгалова Светлана Владимировна,
к.м.н. Бубнова Евгения Викторовна
МАТЕРИАЛЫ КОНГРЕССОВ И КОНФЕРЕНЦИЙ: IV РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
IV РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
ЧТО НУЖНО ЗНАТЬ ПАЦИЕНТУ ПРИ ПРОВЕДЕНИИ ЛУЧЕВОЙ ТЕРАПИИ
Л. Б. Ефимова
Б. Ефимова
Медицинский радиологический научный центр РАМН, Обнинск
В докладе будет дана примерная схема основных вопросов, которые задают себе, врачу и медицинским сестрам больные с онкологическими заболеваниями, которым назначают лучевое лечение. Любой больной, а тем более онкологический, потрясен свалившейся на него бедой, он боится и не знает, как себя дальше вести, в чем искать опору. В этой ситуации кроме лечащего врача такую поддержку больные могут найти только у сестры, поскольку большую часть времени они общаются именно с нами. Найти нужные слова и правильно подготовить больного к процессу лечения, ответить на интересующие его вопросы — наш долг и обязанность, но еще это должно идти от сердца, от сострадания.
Ниже дается перечень вопросов, ответы на которые должны, на наш взгляд, знать сестры, чтобы помочь больному успешно пройти лечение.
Что такое лучевая терапия?
Лучевая терапия — это направленное использование радиации для лечения новообразований и ряда неопухолевых заболеваний. Это излучение создается с помощью специальных аппаратов или возникает в результате распада радиоактивных веществ.
Это излучение создается с помощью специальных аппаратов или возникает в результате распада радиоактивных веществ.
Каков механизм лучевого лечения? При облучении происходит гибель больных клеток, что останавливает развитие болезни. Если не проводить лечение, больные клетки могут непрерывно расти, разрушая при этом здоровые клетки и распространясь по всему организму.
Каковы успехи лучевой терапии? Облучение используется для лечения многих типов опухоли, и для многих пациентов оно является единственным методом лечения, который им необходим. Успехом лучевой терапии необходимо считать излечение от болезни. Кроме того, лучевая терапия может приносить уменьшение болей, симптомов сдавления здоровых органов, прекращать кровотечение.
Каков риск лучевой терапии? Как при большинстве методов лечения, имеется некоторый риск для больных, которым проводится лучевое лечение. Излучение, убивая больные клетки, может также повреждать и прилежащие к ним нормальные ткани, что приводит к развитию побочных эффектов. Однако риск отрицательного воздействия намного меньше, чем последствия неизлечимой болезни.
Однако риск отрицательного воздействия намного меньше, чем последствия неизлечимой болезни.
Что Вы можете ожидать от лучевой терапии?
Как проводится лучевое лечение? Источник излучения можно подводить к больному участку несколькими способами, если источник:
- находится на расстоянии от тела пациента — облучение называется дистанционным;
- помещают в какую-либо полость — внутриполостное;
- вводят непосредственно в больной участок в виде жидкости, проволоки, игл, зондов, а также в виде жидкости через рот, в сосуды и полости, такой вид облучения называется внутритканевым.
Что можно ожидать при получении дистанционной лучевой терапии? Перед началом лучевой терапии врач-радиолог изучит все Ваши документы (историю болезни, снимки, анализы и др.) и выберет нужный метод лучевой терапии. После этого Вам будет дана информация о методе, побочных эффектах, риске и прогнозе результатов лечения. При следующем посещении Вы пройдете специальную процедуру маркировки, называемую разметкой. Вам сделают рентгеновские снимки области, которая будет облучаться. Эти рентгеновские снимки будут использованы вашим врачом при решении вопроса о том, как направить излучение, чтобы воздействовать на очаг заболевания и сохранить здоровые ткани. На Вашу кожу будут нанесены метки краской (фуксином), которые необходимо сохранять в период проведения терапии. При необходимости будут изготовлены специальные приспособления, которые позволят соблюдать точное положение тела при каждом сеансе облучения. Число сеансов лечения определяет Ваш врач.
При следующем посещении Вы пройдете специальную процедуру маркировки, называемую разметкой. Вам сделают рентгеновские снимки области, которая будет облучаться. Эти рентгеновские снимки будут использованы вашим врачом при решении вопроса о том, как направить излучение, чтобы воздействовать на очаг заболевания и сохранить здоровые ткани. На Вашу кожу будут нанесены метки краской (фуксином), которые необходимо сохранять в период проведения терапии. При необходимости будут изготовлены специальные приспособления, которые позволят соблюдать точное положение тела при каждом сеансе облучения. Число сеансов лечения определяет Ваш врач.
Что происходит в течение каждого сеанса облучения? В процедурной комнате врач и медицинская сестра (технолог) помогут Вам занять позицию для лечения, которая была выбрана во время разметки. Вам еще раз напомнят, что имеющиеся на коже метки необходимо тщательно сохранять в течение всего курса лучевой терапии. Это будет легко делать, если Вы носите одежду, которая легко снимается. В процедурной комнате Вы будете ежедневно находиться в течение нескольких минут, время облучения составит 1-5 минут из общего времени. Для осуществления лечения врач поместит нужные блоки или защиту, как это разработано по программе. При погашенном свете врач уточняет Ваши метки перед каждым сеансом облучения. После ухода медицинского персонала Вы должны оставаться неподвижным, чтобы получить радиацию только в область, где это необходимо. Вы должны спокойно дышать во время сеанса облучения. Врач и медицинская сестра (технолог) управляют аппаратом в специальной комнате и наблюдают за Вами с помощью монитора. Они видят и слышат Вас. Вы, скорее всего, не будете чувствовать что-либо во время сеанса лечения, но можете услышать шумы, обусловленные работой аппарата. Не пугайтесь, большие машины производят значительный шум.
В процедурной комнате Вы будете ежедневно находиться в течение нескольких минут, время облучения составит 1-5 минут из общего времени. Для осуществления лечения врач поместит нужные блоки или защиту, как это разработано по программе. При погашенном свете врач уточняет Ваши метки перед каждым сеансом облучения. После ухода медицинского персонала Вы должны оставаться неподвижным, чтобы получить радиацию только в область, где это необходимо. Вы должны спокойно дышать во время сеанса облучения. Врач и медицинская сестра (технолог) управляют аппаратом в специальной комнате и наблюдают за Вами с помощью монитора. Они видят и слышат Вас. Вы, скорее всего, не будете чувствовать что-либо во время сеанса лечения, но можете услышать шумы, обусловленные работой аппарата. Не пугайтесь, большие машины производят значительный шум.
Побочные эффекты (реакции). Во время лечения у Вас могут развиться побочные эффекты, которые обусловлены излучением. Все люди по-разному переносят лучевую терапию. Чаще всего реакции развиваются через 2-3 недели после окончания лучевой терапии. Ваш врач даст рекомендации по лекарственному лечению и предупреждению их во время всего курса терапии. Он также даст Вам рекомендации по диетпитанию, которое может способствовать снижению побочных эффектов. Можно указать на некоторые реакции нормальных тканей и органов, которые могут появиться у Вас во время лучевого лечения и в ближайшие сроки по его завершению.
Чаще всего реакции развиваются через 2-3 недели после окончания лучевой терапии. Ваш врач даст рекомендации по лекарственному лечению и предупреждению их во время всего курса терапии. Он также даст Вам рекомендации по диетпитанию, которое может способствовать снижению побочных эффектов. Можно указать на некоторые реакции нормальных тканей и органов, которые могут появиться у Вас во время лучевого лечения и в ближайшие сроки по его завершению.
1. Изменения (реакции) кожи: сухость, шелушение, зуд, краснота, появление пузырьков. Для предупреждения и лечения этих реакций используются различные виды мазей, масло Витаон, крем «Детский», «Люкс».
2. Изменения (реакции), возникающие при лечении головы (черепа): выпадение волос, нарушения слуха из-за отека слухового канала, ощущение тяжести в голове.
3. Побочные эффекты, которые могут наблюдаться при лечении лица и шеи: сухость во рту, першение, боли при приеме пищи или постоянные, спазм, осиплость голоса, потеря аппетита, обо всем нужно рассказывать лечащему врачу. Необходима щадящая диета (исключить все острое, крепкое, соленое, кислое, грубую пищу). Используйте пищу, приготовленную на пару, вареную, хорошо измельченную. Питайтесь чаще, небольшими порциями, во время еды используйте растительное или сливочное масло. Употребляйте больше жидкости, свежеприготовленные овощные и фруктовые соки, отвар шиповника, некислый клюквенный морс и др. Для уменьшения сухости, першения, болей используйте полоскания отварами трав (ромашка, календула, мята), можно принимать натощак масло облепихи с подсолнечным растительным маслом в соотношении 1:2, закапывать эту смесь по полной пипетке в нос, особенно на ночь. Зубы можно обрабатывать ежедневно 1% фтористым гелем.
Необходима щадящая диета (исключить все острое, крепкое, соленое, кислое, грубую пищу). Используйте пищу, приготовленную на пару, вареную, хорошо измельченную. Питайтесь чаще, небольшими порциями, во время еды используйте растительное или сливочное масло. Употребляйте больше жидкости, свежеприготовленные овощные и фруктовые соки, отвар шиповника, некислый клюквенный морс и др. Для уменьшения сухости, першения, болей используйте полоскания отварами трав (ромашка, календула, мята), можно принимать натощак масло облепихи с подсолнечным растительным маслом в соотношении 1:2, закапывать эту смесь по полной пипетке в нос, особенно на ночь. Зубы можно обрабатывать ежедневно 1% фтористым гелем.
4. Побочные эффекты, которые могут встречаться при лучевой терапии на органы грудной клетки: затруднение, боли при глотании слюны, жидкости, пищи; сухой кашель, одышка, болезненность мышц.
5. Побочные эффекты, которые могут встречаться при лечении молочной железы: болезненность мышц, припухлость и болезненность молочной железы, реакции кожи областей облучения, воспалительные явления со стороны горла, редко кашель. Мероприятия по лечению реакций такие же, как в пунктах 1, 3.
Мероприятия по лечению реакций такие же, как в пунктах 1, 3.
6. Побочные эффекты, которые могут встречаться при облучении органов брюшной полости: потеря аппетита, похудание, тошнота, рвота, понос, боли в брюшной полости.
7. Реакции, развивающиеся при лечении тазовой области: тошнота, потеря аппетита, понос, нарушение мочеиспускания (часто, непроизвольное) с чувством жжения, боли в прямой кишке, сухость влагалища, выделения из него. При облучении брюшной полости или тазовой зоны необходимо проводить определенные диетические мероприятия. В течение первой недели необходимо перейти на диетическое питание (стол 4-5). Пищу принимать чаще, небольшими порциями, до 4-5 раз в день. Она должна быть отварной или приготовлена на пару, протертая. Необходимо исключить жареное, соленое, острое, кислое. При появлении вздутия живота, поноса исключить молочные продукты. Можно принимать вегетарианские супы на слабом мясном или рыбном бульоне, протертые каши, кисели, паровые блюда из нежирных сортов мяса в виде кнелей, суфле, фрикаделек, котлет, пюре, нежирную отварную рыбу, пшеничный хлеб из высших сортов муки, лучше в виде сухарей, свежеприготовленный творог. Разрешаются отвары черники, черемухи, шиповника, спелых груш, гранатов, некислых яблок, крепкий чай, какао на воде, кофе черный, из вин — кагор. Большинство пациентов хорошо переносят 2-3 яйца всмятку и в виде паровых омлетов. Рекомендуется ограничить прием сахара, а сливочное масло класть в готовые блюда.
Разрешаются отвары черники, черемухи, шиповника, спелых груш, гранатов, некислых яблок, крепкий чай, какао на воде, кофе черный, из вин — кагор. Большинство пациентов хорошо переносят 2-3 яйца всмятку и в виде паровых омлетов. Рекомендуется ограничить прием сахара, а сливочное масло класть в готовые блюда.
8. Побочные эффекты, которые могут встречаться при облучении костей конечностей, позвоночника, костей таза и других зон скелета: хрупкость (ломкость) кости (в основном для костей конечностей), уменьшение показателей крови, болезненность мышц. Бывают реакции слизистых оболочек пищевода, кишечника в зависимости от того, в какой части тела облучаются кости. Возможны реакции кожи в зонах облучения.
Наблюдение после окончания лечения
Когда Вы закончили курс лучевой терапии, Ваш врач укажет Вам время контрольных исследований. Во время этих посещений врач осмотрит Вас и назначит необходимые дополнительные исследования. Это нужно делать, чтобы выявить побочные эффекты, связанные с лучевым лечением, а также контролировать процесс заболевания.
Способы облегчения своей жизни во время лучевой терапии. Позаботьтесь о себе в течение лучевой терапии. Все пациенты, получающие лучевую терапию, должны заботиться о себе, чтобы защитить свое здоровье и помочь врачу в достижении успехов лечения. С помощью определенных мероприятий Вы можете это сделать. Больше отдыхайте. Спите столько, сколько Вам необходимо. Ваше тело будет нуждаться в дополнительной энергии во время курса лечения, и Вы можете чувствовать себя утомленным. Просите о помощи, когда Вы нуждаетесь в этом. Ешьте хорошую пищу. Вашему организму необходимо успешно перенести лечение. Сбалансированная диета предотвратит потерю в весе.
Избегайте носить стягивающую одежду, особенно в области облучения. Нательное белье должно быть мягким, изо льна или хлопка. Используйте умеренно теплую воду для купания. Защищайте область облучения от солнца, закрывая ее одеждой, шляпой или шарфом.
Старайтесь быть спокойным. Помните, что лучевая терапия помогает Вам бороться с Вашим заболеванием.
Задавайте все вопросы относительно лучевой терапии. Вы не будете бояться, если знаете, что Вас ожидает.
Заботьтесь о себе — так Вы будете чувствовать, что управляете своей жизнью снова.
Что такое радиация? | UCSF Radiology
Все мы ежедневно подвергаемся радиационному воздействию, в основном от солнца и почвы. Другие источники радиации созданы человеком и включают потребительские товары, а также диагностические методы визуализации, такие как рентген, компьютерная томография и исследования ядерной медицины.
Радиация — это любая энергия, исходящая от источника и перемещающаяся в пространстве, например свет или тепло. Рентгеновские лучи представляют собой форму лучистой энергии, такой как свет или радиоволны, но в отличие от света, рентгеновские лучи могут проникать в тело, что позволяет рентгеновским лучам создавать изображения или «изображения» внутренних структур тела.В UCSF и большинстве других центров обработки изображений эти изображения просматриваются на мониторе компьютера и сохраняются в электронном виде.
В области интервенционной радиологии рентгеновские изображения используются для помощи при размещении трубок или других устройств в организме или при других терапевтических процедурах и лечении.
Измерение дозы излучения
Научной единицей измерения дозы облучения является грей (Гр), который представляет собой меру количества энергии рентгеновского излучения, поглощенной на единицу массы.Другие единицы измерения излучения включают рад, бэр, рентген и зиверт.
Процедуры рентгеновской визуализации обычно фокусируются на определенной части тела (например, голове или груди) и подвергают облучению только эту часть тела. Кроме того, разные ткани и органы имеют разную чувствительность к радиационному облучению, поэтому реальный радиационный риск от рентгеновской процедуры будет зависеть от визуализируемой части тела и облученных тканей. Термин «эффективная доза» используется для учета части тела, облученной во время процедуры, и усредняет риск облучения по всему телу. Единица эффективной дозы — зиверт. В результате рентгеновских процедур получается малая доля зиверта, обычно одна тысячная зиверта, на что указывает миллизиверт (мЗв).
Единица эффективной дозы — зиверт. В результате рентгеновских процедур получается малая доля зиверта, обычно одна тысячная зиверта, на что указывает миллизиверт (мЗв).
Эффективная доза учитывает относительную чувствительность различных пораженных тканей. Что еще более важно, это позволяет оценить риск и сравнить с более знакомыми источниками воздействия, такими как естественный фоновый радиационный фон. Дополнительная информация доступна на веб-сайте radiologyinfo.org.
Естественное «фоновое» радиационное облучение
Мы постоянно подвергаемся радиации от естественных источников.Согласно последним оценкам, средний человек в Соединенных Штатах получает эффективную дозу около 3 миллизивертов (мЗв) в год от естественных радиоактивных материалов и космических лучей, то есть радиации, исходящей из космоса. Эти естественные «фоновые» дозы различаются по стране.
Высота играет роль в количестве космической радиации, поэтому люди, живущие на плато Колорадо или Нью-Мексико, получают примерно на 1,5 мЗв больше в год, чем люди, живущие на уровне моря. Дополнительная доза космических лучей во время полета туда и обратно от побережья до побережья на коммерческом самолете составляет около 0,03 мЗв. Однако самый большой источник радиационного фона — это радон в наших домах (около 2 мЗв в год). Как и другие источники радиационного фона, облучение радоном широко варьируется от одной части страны к другой.
Дополнительная доза космических лучей во время полета туда и обратно от побережья до побережья на коммерческом самолете составляет около 0,03 мЗв. Однако самый большой источник радиационного фона — это радон в наших домах (около 2 мЗв в год). Как и другие источники радиационного фона, облучение радоном широко варьируется от одной части страны к другой.
Проще говоря, радиационное воздействие от одного рентгеновского снимка грудной клетки эквивалентно количеству радиационного облучения, которое человек испытывает из нашего естественного окружения в течение трех дней.
Лучевая терапия под визуальным контролем (IGRT) — Клиника Мэйо
Мы приветствуем пациентов в клинике Мэйо
Ознакомьтесь с нашими мерами предосторожности в ответ на COVID-19.
Записаться на прием.
Обзор
Лучевая терапия под визуальным контролем (IGRT) — это метод лучевой терапии, который включает методы визуализации во время каждого сеанса лечения.
Лучевая терапия использует высокоэнергетические пучки излучения для борьбы с раком и доброкачественными опухолями.Добавляя подробные изображения, IGRT обеспечивает узкую фокусировку мощного излучения в области лечения.
При прохождении IGRT высококачественные снимки делаются перед каждым сеансом лучевой терапии. IGRT может позволить использовать более высокие дозы излучения, что увеличивает вероятность контроля над опухолью и, как правило, приводит к сокращению сроков лечения.
IGRT — стандарт медицинской помощи при лучевой терапии.Он используется для лечения всех видов рака.
Продукты и услуги
Показать больше продуктов от Mayo ClinicЗачем это нужно
IGRT используется для лечения всех типов рака, но особенно идеально подходит для опухолей и рака, расположенных в непосредственной близости от чувствительных структур и органов. IGRT также полезен для опухолей, которые могут двигаться во время лечения или между курсами лечения.
IGRT также полезен для опухолей, которые могут двигаться во время лечения или между курсами лечения.
IGRT используется как часть планов лучевой терапии, поскольку предлагает:
- Точная доставка излучения
- Улучшенное определение, локализация и мониторинг положения, размера и формы опухоли до и во время лечения
- Возможность более высокой целевой дозы облучения для улучшения контроля над опухолью
- Снижение лучевой нагрузки на нормальные ткани, окружающие опухоль
Что вас может ожидать
Если вы проходите курс IGRT , ваша лечащая бригада может выбрать один или несколько типов изображений, чтобы точно определить местонахождение опухоли и чувствительных органов. IGRT может включать в себя различные методы 2-D, 3-D и 4-D визуализации, чтобы расположить ваше тело и направить излучение так, чтобы ваше лечение было тщательно сфокусировано на опухоли, чтобы минимизировать вред здоровым клеткам и органам поблизости. .
.
Во время IGRT тесты изображений выполняются до, а иногда и во время каждого сеанса лечения. Ваша бригада лучевой терапии сравнивает эти изображения с изображениями, сделанными ранее, чтобы определить, сместилась ли ваша опухоль, и настроить ваше тело и лечение для более точного нацеливания на опухоль.
Лучевая терапия под визуальным контролем (IGRT) в клинике Мэйо
12 ноября 2020 г.
Показать ссылки- Gunderson LL, et al., Eds. Лучевая терапия с модуляцией интенсивности и под визуальным контролем. В кн .: Клиническая радиационная онкология. 4-е изд. Филадельфия, Пенсильвания: Эльзевир; 2016 г. https://www.clincalkey.com. Доступ 10 октября 2017 г.
- Jaffray DA. Лучевая терапия под визуальным контролем: от нынешней концепции к будущим перспективам. Обзоры природы Клиническая онкология.
 2012; 9: 688.
2012; 9: 688. - Лучевая терапия под визуальным контролем (IGRT). RadiologyInfo.org. http://www.radiologyinfo.org/en/info.cfm?pg=igrt. Проверено 10 октября 2017 г.
- Поиск аккредитованного объекта. Американский колледж радиологии. http://www.acraccreditation.org/accredited-facility-search. Доступ 20 октября 2017 г.
- Фонг де лос Сантос ЛЕ (заключение эксперта).Клиника Мэйо, Рочестер, Миннесота. 20 октября 2017 г.
Связанные
Продукты и услуги
Показать больше продуктов и услуг Mayo ClinicЛучевая терапия под визуальным контролем (IGRT)
Лучевая терапия под визуальным контролем | Мемориальный онкологический центр им.
 Слоуна-Кеттеринга
Слоуна-КеттерингаЭта информация поможет вам подготовиться к лучевой терапии под визуальным контролем (IGRT).Это поможет вам узнать, чего ожидать до, во время и после лечения. Вы также узнаете о побочных эффектах и о том, как позаботиться о себе во время лечения.
Прочтите этот ресурс перед началом лучевой терапии. Используйте его в качестве справочника в дни, предшествующие лечению, чтобы вы могли подготовиться как можно больше. Принесите этот ресурс на прием к симулятору и на все будущие приемы к своему онкологу-радиологу. Вы и ваша медицинская бригада будете обращаться к нему на протяжении всего лечения.
Вернуться наверхОб IGRT
В лучевой терапии для лечения рака используются пучки высокой энергии. Он работает, повреждая раковые клетки и затрудняя их размножение. Тогда ваше тело естественным образом сможет избавиться от этих поврежденных раковых клеток. Лучевая терапия также влияет на нормальные клетки. Однако ваши нормальные клетки способны восстанавливать себя так, как раковые клетки не могут.
IGRT может лечить опухоли с большей точностью, чем традиционная лучевая терапия.IGRT предполагает получение множества изображений опухоли во время лечения. Это гарантирует, что мы направляем луч излучения в нужную область. Вы не увидите и не почувствуете излучения.
Вы можете получить IGRT, если:
- Вам будет назначена лучевая терапия от 1 до 5 процедур вместо нескольких.
- Из соображений безопасности ваше лечение должно быть очень точным.
- Вам необходимо лечение той части тела, которая движется. Это может быть:
- Опухоль в легком или печени, которая двигается при дыхании.
- Опухоль в брюшной полости или тазу, которая двигается из-за переполнения или движения пищеварительного тракта.
- Опухоль в позвоночнике или прилегающих областях.
Лучевая терапия требует времени, чтобы подействовать. Прежде чем раковые клетки начнут умирать, требуются дни или недели лечения. Они будут продолжать умирать в течение недель или месяцев после окончания лучевой терапии.
Ваша роль в бригаде лучевой терапии
У вас будет команда поставщиков медицинских услуг, которые будут работать вместе, чтобы предоставить вам правильный уход.Вы являетесь частью этой команды, и ваша роль включает:
- Прибытие вовремя на все сеансы лучевой терапии.
- Задавать вопросы и говорить о том, что вас беспокоит. Мы включили список возможных вопросов в конце этого ресурса.
- Сообщать кому-нибудь из вашей бригады лучевой терапии о побочных эффектах.
- Сообщите врачу или медсестре, если вам больно.
- Уход за собой дома:
- Отказ от курения, если вы курите.Если вы хотите бросить курить, позвоните в нашу Программу лечения табака по телефону 212-610-0507.
- Следуйте инструкциям лечащего врача по уходу за кожей.
- Питьевые жидкости в соответствии с указаниями вашего лечащего врача.
- Есть продукты, рекомендованные вашим лечащим врачом.
- Поддержание веса.

Симуляторы
Перед началом лучевой терапии у вас будет процедура планирования лечения, называемая симуляцией.
Моделирование выполняется, чтобы убедиться, что:
- Ваше место лечения нанесено на карту.
- Вы получили правильную дозу радиации.
- Доза облучения близлежащих тканей минимальна.
Во время симуляции вам сделают рентген, и ваша кожа может быть отмечена маленькими татуировками. Эти отметки помогут вашей команде убедиться, что вы находитесь в правильном положении для лучевой терапии.
Симуляция продлится от 2 до 4 часов, но может длиться дольше в зависимости от лечения, запланированного для вас врачом.
Подготовка к моделированию
- Во время симуляции вы будете лежать в одном положении долгое время . Если вы думаете, что вам будет неудобно лежать неподвижно, вы можете принять ацетаминофен (Tylenol ® ) или свое обычное обезболивающее перед симуляцией.

- Если вам кажется, что во время процедуры у вас может возникнуть беспокойство, узнайте у врача, могут ли вам помочь лекарства.
- Носите удобную одежду, которую легко снимать, потому что вам может потребоваться переодеться в больничную одежду.Не носите украшения, пудры или лосьоны.
Перед симуляцией вам могут потребоваться другие процедуры, которые помогут спланировать лечение. Если вам нужно пройти одну из описанных ниже процедур, мы запланируем их для вас.
Некоторым людям перед симуляцией потребуется выполнить другие процедуры, чтобы помочь в планировании лечения. Если вам нужно пройти какие-либо из описанных ниже процедур, мы запланируем их для вас.
- Размещение маркеров: Несколько золотых маркеров будут имплантированы в обрабатываемую область.Эти маркеры размером с рисовое зерно, их можно увидеть на рентгеновских снимках и компьютерной томографии (КТ). Размещение маркера будет выполнено за несколько дней до симуляции.
 Вам скажут, куда пойти, чтобы это сделать. Сотрудник интервенционной радиологии свяжется с вами накануне, чтобы дать инструкции и подтвердить время вашего прибытия.
Вам скажут, куда пойти, чтобы это сделать. Сотрудник интервенционной радиологии свяжется с вами накануне, чтобы дать инструкции и подтвердить время вашего прибытия. - Миелограмма: В позвоночный канал будет введен контрастный краситель. Это помогает нам более четко видеть ваш спинной мозг и окружающие ткани.Это делается за несколько часов до симуляции.
- Сотрудник отделения радиологии позвонит вам за день до процедуры. Он или она скажет вам, в какое время вы должны прибыть в больницу на процедуру. Если ваша процедура назначена на понедельник, вам позвонят в предыдущую пятницу. Если вам не позвонят до 16:00 за рабочий день до процедуры, позвоните по номеру 212-639-7298.
- Вам нужно будет пойти в Центр вмешательств с визуальным контролем (CIGI) на 1275 York Avenue между улицами East 67 th и East 68 th Streets.Поднимитесь на лифте M на 2 -й этаж .
- Ваша миелограмма будет сделана перед симуляцией.
 После выздоровления вас вернут в отделение радиационной онкологии на носилках для симуляции.
После выздоровления вас вернут в отделение радиационной онкологии на носилках для симуляции.
День симуляции
Чего ожидать
Член вашей бригады лучевой терапии отметит вас. Вам будет предложено несколько раз указать и записать ваше полное имя и дату рождения. Это сделано для вашей безопасности и является частью нашего стандартного процесса идентификации.Люди с такими же или похожими именами могут получать помощь в тот же день, что и вы.
Вас встретит лучевой терапевт. Он или она сфотографирует ваше лицо. Эта фотография будет использоваться для вашей идентификации на протяжении всего лечения.
После этого ваш лучевой терапевт объяснит вам моделирование. Если вы еще не подписали форму согласия, ваш онколог-радиолог рассмотрит все вместе с вами и попросит вашу подпись.
Во время симуляции
Для симуляции вам может потребоваться раздеться и переодеться в платье.Вы должны не снимать обувь. Если вы носите головной убор, например парик, тюрбан или кепку, возможно, вам придется его снять. Ваши лучевые терапевты помогут вам лечь на стол и приложат все усилия, чтобы обеспечить вам комфорт и уединение.
Ваши лучевые терапевты помогут вам лечь на стол и приложат все усилия, чтобы обеспечить вам комфорт и уединение.
Несмотря на то, что на столе есть простыня, он твердый и без подушки. Если вы не принимали обезболивающее и думаете, что оно может вам понадобиться, сообщите об этом своим лучевым терапевтам до начала симуляции. Также в комнате обычно прохладно. Если вы почувствуете дискомфорт в любой момент, сообщите об этом своим радиотерапевтам.
Во время симуляции вы будете чувствовать, как стол перемещается в разные положения. Свет в комнате будет включаться и выключаться, и вы увидите красные лазерные огни на каждой стене. Ваши лучевые терапевты используют эти лазерные лучи в качестве ориентира, когда размещают вас на столе. Не смотрите прямо на красный луч, это может повредить вам глаза.
Хотя во время симуляции ваши радиотерапевты будут входить в комнату и выходить из нее, всегда найдется кто-то, кто может вас видеть и слышать.Вы услышите, как ваши лучевые терапевты разговаривают друг с другом во время работы, и они объяснят вам, что делают. Не двигайтесь после начала симуляции, потому что это может изменить ваше положение. Однако, если вам неудобно или вам нужна помощь, сообщите об этом своим лучевым терапевтам.
Не двигайтесь после начала симуляции, потому что это может изменить ваше положение. Однако, если вам неудобно или вам нужна помощь, сообщите об этом своим лучевым терапевтам.
Чтобы скоротать время, лучевые терапевты могут включить для вас музыку. При желании вы можете принести из дома свой компакт-диск.
Позиционирование и формы
В зависимости от обрабатываемой области вашего тела могут быть изготовлены оправы, формы или маски.Они помогут вам оставаться в правильном положении и будут использоваться при каждом лечении. На их изготовление уходит около 30 минут.
- Верхний отдел позвоночника: Вы будете лежать на спине в рамке, держа руки за ручки по бокам (см. Рисунок 1). Оправа выравнивает ваши плечи и бедра, чтобы держать вас в правильном положении. Для вас изготовят маску, которая будет доходить до плеч.
Рисунок 1. Форма верхнего отдела позвоночника
- Нижний отдел позвоночника: Вы лягте на спину, поместив лопатку по обеим сторонам бедер (см.
 Рисунок 2).
Рисунок 2).Рисунок 2. Форма нижней части корешка
- Компрессия живота: Вы будете лежать на спине. Вам будет предложено надеть жакет, похожий на жгут (см. Рисунок 3). Нижняя часть будет лежать поперек нижней части живота (живота), и в нее будет медленно добавляться воздух, создавая давление. Это сделано для того, чтобы уменьшить подвижность вашей печени, пока мы делаем рентгеновские снимки.
Рисунок 3. Компрессия живота.
- Маска для лица: Ваш лучевой терапевт накроет вам лицо теплым влажным листом пластиковой сетки и придаст ему форму, соответствующую вашей голове.Вы сможете без проблем слышать и дышать, пока маска надета. Когда маска остынет, она затвердеет.
- Форма тела: Вы, вероятно, будете лежать на спине во время симуляции. На верхней части тела может быть изготовлен слепок, который поможет вам сохранять одно и то же положение каждый раз, когда вы проходите лечение.
 Ваш терапевт нальет теплую жидкость в большой пластиковый пакет, который будет запечатан и поставлен на стол. Вы лягте на сумку на спине, подняв руки над головой (см. Рисунок 4).Сначала жидкость будет теплой, но по мере застывания она остынет. Пока он остывает, ваш лучевой терапевт прикрепит сумку к вашей коже липкой лентой, чтобы она приняла форму вашей верхней части тела и рук. Эта процедура занимает около 15 минут. Во время симуляции и каждый день лечения вы будете лежать в этой форме, чтобы убедиться, что вы находитесь в правильном положении.
Ваш терапевт нальет теплую жидкость в большой пластиковый пакет, который будет запечатан и поставлен на стол. Вы лягте на сумку на спине, подняв руки над головой (см. Рисунок 4).Сначала жидкость будет теплой, но по мере застывания она остынет. Пока он остывает, ваш лучевой терапевт прикрепит сумку к вашей коже липкой лентой, чтобы она приняла форму вашей верхней части тела и рук. Эта процедура занимает около 15 минут. Во время симуляции и каждый день лечения вы будете лежать в этой форме, чтобы убедиться, что вы находитесь в правильном положении.Рис. 4. Форма корпуса.
Рентгеновские снимки
В лежачем положении вам сделают рентгеновский снимок обрабатываемой области.Это можно сделать на рентгеновском аппарате, называемом имитатором, или на аппарате компьютерной томографии (КТ). Эти сканы используются только для составления карты вашего лечения. Они не используются для диагностики или обнаружения опухолей. Если вам нужна другая визуализация, медсестра объяснит вам это.
На рентгенографию уйдет около 45 минут. Во время сканирования вы услышите, как устройство включается и выключается. Даже если шум кажется громким, лучевые терапевты смогут вас услышать, если вы поговорите с ними.
Отметины на коже (татуировки)
Ваши лучевые терапевты будут рисовать на вашей коже в области обработки войлочным маркером.Вам могут понадобиться постоянные отметины на коже, называемые татуировками. Ваши лучевые терапевты сделают татуировку с помощью стерильной иглы и капли чернил. Ощущение попадания похоже на укол булавкой. Следы татуировки не больше булавочной головки. Маркировку на фетре можно смыть после моделирования. Татуировки стойкие и не смываются. Если вы беспокоитесь о татуировках в рамках лучевой терапии, поговорите со своим врачом.
После того, как татуировки будут сделаны, терапевты сделают несколько ваших фотографий в вашей позе симуляции.Фотографии и татуировки будут использоваться для правильного расположения вас на столе каждый день лечения.
Дополнительное изображение
Нам может потребоваться использовать другие визуализационные тесты вместе с компьютерной томографией, чтобы помочь нам спланировать ваше лечение. Это делается в тот же день, что и симуляция, сразу после процедуры. Мы составим для вас график и доставим вас на место, где они будут выполняться. Если вы думаете, что будете чувствовать беспокойство во время этих процедур, спросите своего врача о лекарствах, которые помогут вам расслабиться.
- Магнитно-резонансная томография (МРТ): Эта процедура будет сделана в отделении радиационной онкологии, пока вы находитесь в слепке тела, созданном нами во время симуляции. Это помогает нам более четко видеть ваш позвоночник.
- Сканирование позитронно-эмиссионной томографии (ПЭТ): Эта процедура будет выполняться, пока вы находитесь в форме тела, которую мы сделали во время моделирования. Это помогает нам увидеть разницу между нормальными и аномальными тканями.
 Это будет сделано в отделении радиационной онкологии или в Службе молекулярной визуализации и терапии (MITS).MITS иногда называют службой ядерной медицины.
Это будет сделано в отделении радиационной онкологии или в Службе молекулярной визуализации и терапии (MITS).MITS иногда называют службой ядерной медицины.
После моделирования
В конце симуляции вам может быть выдана карточка с указанием даты и времени вашего первого сеанса лечения. Если вам не удастся записаться на прием, мы позвоним вам и сообщим дату и время.
Запланировать лечение
IGRT можно давать по нескольким разным графикам. Ваш график основан на рекомендациях вашего онколога-радиолога.Это может быть:
- Однократная процедура, обычно проводимая в тот же день, что и установка или снимки луча.
- От трех до пяти процедур, обычно через день
- Ежедневное лечение с понедельника по пятницу в течение примерно _____ недель.
Вы должны приходить каждый день, когда вам назначено лечение. Ваше лечение может быть не таким эффективным, если вы пропускаете или пропускаете приемы. Если вам понадобится дополнительное время из-за непредвиденных обстоятельств, ваш онколог-радиолог скажет вам.Если вы по какой-то причине не можете прийти на лечение, вы должны позвонить в офис своего онколога-радиолога, чтобы сообщить об этом своей команде. Если вам по какой-либо причине необходимо изменить свое расписание, поговорите со своим лучевым терапевтом.
Если вам понадобится дополнительное время из-за непредвиденных обстоятельств, ваш онколог-радиолог скажет вам.Если вы по какой-то причине не можете прийти на лечение, вы должны позвонить в офис своего онколога-радиолога, чтобы сообщить об этом своей команде. Если вам по какой-либо причине необходимо изменить свое расписание, поговорите со своим лучевым терапевтом.
Планирование лечения
В период между симуляцией и первым сеансом лечения ваш онколог-радиолог будет работать с командой, чтобы спланировать ваше лечение. Они будут использовать ваши имитационные рентгеновские снимки, компьютерную томографию и любые другие визуальные тесты, которые были сделаны для планирования углов и форм ваших лучей излучения.Они также определят дозу радиации, которую получит ваше тело. Эти детали тщательно планируются и проверяются. Этот процесс занимает около 7 рабочих дней.
Витамины и пищевые добавки
Многие спрашивают о приеме витаминов во время лечения. Если хотите, можете ежедневно принимать поливитамины. Не принимайте больше рекомендованной суточной нормы любого витамина. Не принимайте никакие другие витамины или добавки, не посоветовавшись с врачом. Это включает как пищевые, так и травяные добавки.
Если хотите, можете ежедневно принимать поливитамины. Не принимайте больше рекомендованной суточной нормы любого витамина. Не принимайте никакие другие витамины или добавки, не посоветовавшись с врачом. Это включает как пищевые, так и травяные добавки.
Процедура настройки
Перед первым сеансом лечения вам будет назначена процедура настройки. Обычно это занимает около 1 часа. Если во время симуляции вам помогло обезболивающее, вы можете принять его перед этой процедурой.
Когда вы придете на процедуру настройки, вас проводят в раздевалку и попросят переодеться в халат. Терапевты проводят вас в комнату, где вы будете проходить лечение каждый день.Они поместят вас на лечебный стол. Вы будете лежать точно так же, как в день симуляции.
Будут сделаны специальные рентгеновские снимки, называемые лучевыми пленками, чтобы убедиться, что ваше положение и обрабатываемая область правильные. Пучковые снимки будут повторяться на протяжении всего лечения. Они не используются, чтобы увидеть, как ваша опухоль реагирует на лечение.
Они не используются, чтобы увидеть, как ваша опухоль реагирует на лечение.
В зависимости от вашего плана лечения вы можете начать лечение в тот же день, что и назначенная процедура.
Вернуться наверхВо время лечения
После регистрации на стойке регистрации займите место в зале ожидания.Когда радиотерапевты будут готовы, они скажут вам переодеться в халат. Если вы принимаете обезболивающее, вам следует принять их в это время.
Радиотерапевты проводят вас в процедурный кабинет и помогают лечь в форме на столе (см. Рисунки 5 и 6). Вы будете расположены точно так, как вы лежали во время процедуры настройки.
Рис. 5. Во время лечения верхним слепком позвоночника.
Рисунок 6.При лечении плесени нижней части позвоночника
После того, как вы расположитесь правильно, лучевые терапевты выйдут из комнаты, закроют дверь и начнут лечение. Вы не увидите и не почувствуете излучение, но вы можете услышать, как машина движется вокруг вас, включается и выключается. Вы будете в процедурном кабинете около 2 часов, в зависимости от вашего плана лечения. Большая часть этого времени будет потрачена на то, чтобы занять правильное положение. Если вы получаете более одной процедуры, следующая может длиться от 30 минут до 2 часов, в зависимости от вашего плана лечения.
Вы не увидите и не почувствуете излучение, но вы можете услышать, как машина движется вокруг вас, включается и выключается. Вы будете в процедурном кабинете около 2 часов, в зависимости от вашего плана лечения. Большая часть этого времени будет потрачена на то, чтобы занять правильное положение. Если вы получаете более одной процедуры, следующая может длиться от 30 минут до 2 часов, в зависимости от вашего плана лечения.
Хотя во время лечения вы будете одни, лучевые терапевты будут постоянно видеть вас на мониторе и слышать по внутренней связи. Они позаботятся о том, чтобы вам было комфортно во время процедуры. Во время процедуры дышите нормально, но не двигайтесь. Однако, если вам неудобно или вам нужна помощь, поговорите со своим лучевым терапевтом. Они могут выключить машину и при необходимости зайти к вам в любое время.
Ни вы, ни ваша одежда не станете радиоактивными во время или после лечения.Для вас безопасно находиться рядом с другими людьми.
Еженедельные посещения во время лечения
Ваш онколог-радиолог и медсестра будут видеть вас каждую неделю, чтобы оценить вашу реакцию на лечение. Этот визит будет проводиться до или после вашего лечения каждые _______________. Вы должны запланировать в отделении примерно 1 дополнительный час в эти дни.
Этот визит будет проводиться до или после вашего лечения каждые _______________. Вы должны запланировать в отделении примерно 1 дополнительный час в эти дни.
Во время этих посещений вы должны задавать вопросы и обсуждать любые волнующие вас вопросы. Если вам необходимо поговорить со своим онкологом-радиологом или медсестрой в любое время между этими еженедельными визитами, попросите обслуживающий персонал или терапевтов связаться с ними, когда вы придете на лечение.
Если вы проходите 1 или 3 курса лечения, ваш онколог-радиолог и медсестра увидят вас хотя бы один раз во время лечения.
Вернуться наверхПобочные эффекты
У некоторых людей лучевая терапия вызывает побочные эффекты. Тип и степень тяжести зависят от многих факторов. Сюда входят доза облучения, количество процедур и ваше общее состояние здоровья. Побочные эффекты могут усилиться, если вы также получаете химиотерапию. Ниже приведены наиболее частые побочные эффекты лучевой терапии. У вас может быть все, некоторые или ничего из этого. В зависимости от обрабатываемой области могут быть другие побочные эффекты, которые обсудят с вами ваш врач и медсестра.
У вас может быть все, некоторые или ничего из этого. В зависимости от обрабатываемой области могут быть другие побочные эффекты, которые обсудят с вами ваш врач и медсестра.
Многие пациенты спрашивают о витаминах. Если хотите, можете ежедневно принимать поливитамины. Не принимайте больше рекомендованного суточного количества любого витамина. Не принимайте никаких добавок, если они не одобрены вашим онкологом-радиологом. Это включает как пищевые, так и травяные добавки.
Отек в области лечения
IGRT может вызвать опухоль вокруг обрабатываемой области.Возможно, вам придется принять стероид под названием дексаметазон (Decadron ® ), чтобы предотвратить это. Нужна ли она вам, зависит от области, которую мы лечим, и от количества полученной радиации. Если вам нужен стероид, вам расскажут, как его принимать до и после лечения. Обязательно примите его именно так, как вам говорят.
Если после лечения у вас появятся какие-либо симптомы, такие как усиление боли или затрудненное движение, немедленно обратитесь к врачу или медсестре. Может потребоваться корректировка дозы или вам может потребоваться дополнительное лечение.
Может потребоваться корректировка дозы или вам может потребоваться дополнительное лечение.
Кожные и волосяные реакции
Во время лучевой терапии ваша кожа и волосы в обрабатываемой области могут измениться. Это нормально. Через 2–3 недели ваша кожа может стать розовой или загорелой. Позже он может даже стать ярко-красным или очень темным.
Во время лечения ваша кожа может казаться сухой и зудящей, а также шелушиться. Иногда кожа в чувствительных областях может покрыться волдырями, открыться и отслоиться. Если это произойдет, сообщите об этом своему врачу или медсестре.
Вы также можете заметить сыпь, особенно в тех областях, где вы ранее были на солнце.Хотя это может быть побочным эффектом лечения, сыпь также может быть признаком инфекции. Если во время лечения у вас появится сыпь, сообщите об этом врачу или медсестре.
Медсестра / медбрат может накладывать специальные повязки или кремы и научить вас ухаживать за кожей. Ваш врач может прекратить лечение, пока ваша кожа не заживет. Эта кожная реакция иногда становится более серьезной в течение недели после завершения лечения. Если это произойдет, позвоните своему врачу или медсестре. Ваша кожа постепенно заживет после завершения лечения, но часто это занимает от 3 до 4 недель.
Эта кожная реакция иногда становится более серьезной в течение недели после завершения лечения. Если это произойдет, позвоните своему врачу или медсестре. Ваша кожа постепенно заживет после завершения лечения, но часто это занимает от 3 до 4 недель.
Вы можете потерять часть или все волосы на обрабатываемой области. Волосы обычно отрастают через 3–6 месяцев после завершения лечения.
Ниже приведены рекомендации, которые помогут вам ухаживать за кожей во время лечения. Следуйте этим рекомендациям, пока ваша кожа не станет лучше. Эти рекомендации относятся только к коже в области, подвергающейся облучению.
Держите кожу чистой
- Принимайте ванну или душ ежедневно, используя теплую воду и мягкое мыло без запаха, например Neutrogena ® , Dove ® , детское мыло, Basis ® или Cetaphil ® .Хорошо промойте кожу и промокните ее мягким полотенцем.
- При мытье будьте осторожны с кожей в зоне обработки.
 Не используйте тряпку для мытья посуды, тряпку или щетку.
Не используйте тряпку для мытья посуды, тряпку или щетку. - Если до лечения у вас остались следы татуировок, они навсегда останутся неизменными и не смываются. Во время лечения вы можете получить другие отметки, например очертание области лечения фиолетовым маркером с фетровым наконечником. Вы можете удалить эти отметины с помощью минерального масла, когда терапевт скажет, что это нормально.
- Не наносите спирт или салфетки на кожу в зоне обработки.
Часто увлажняйте кожу
- Начните использовать увлажняющий крем, когда начнете лечение. Это может помочь свести к минимуму любую кожную реакцию. Вы можете использовать безрецептурные увлажняющие средства. Выбирая увлажняющий крем, выберите тот, у которого нет запахов и ланолина. Есть ряд продуктов, которые можно использовать, и медсестра может порекомендовать вам один из них. Используйте только по одному за раз, если медсестра не скажет вам использовать больше.
- Если вы используете увлажняющий крем, наносите его 2 раза в день.

Избегайте раздражения кожи в обрабатываемой области
- Носите свободную хлопковую одежду на обрабатываемой области. Не носите тесную одежду, которая будет натирать кожу.
- Используйте только увлажняющие кремы, кремы или лосьоны, рекомендованные вашим врачом или медсестрой.
- Не используйте косметику, духи, пудру или лосьон после бритья на обрабатываемой области.
- Не используйте дезодорант, если ваша кожа открытая, потрескавшаяся или раздраженная. Вы можете использовать дезодорант на неповрежденной коже в зоне обработки.Прекратите использовать его, если ваша кожа станет раздраженной.
- Если кожа чешется, не расчесывайте ее. Нанесите увлажняющий крем. Спросите у медсестры, как уменьшить зуд.
- Не брейтесь в обрабатываемой области. Если вам необходимо побриться, используйте только электрическую бритву. Прекратите, если ваша кожа станет раздраженной.
- Не наклеивайте скотч на обработанную кожу.
- Не допускайте контакта обработанной кожи с экстремально высокими или низкими температурами.
 Сюда входят гидромассажные ванны, бутылки с водой, грелки и пакеты со льдом.
Сюда входят гидромассажные ванны, бутылки с водой, грелки и пакеты со льдом. - Если во время лечения у вас нет кожных реакций, вы можете плавать в хлорированном бассейне. Однако не забудьте смыть хлор сразу после выхода из бассейна.
- Избегайте загара и ожогов кожи во время лечения и всю оставшуюся жизнь. Если вы собираетесь находиться на солнце, используйте солнцезащитный крем без ПАБА с SPF 30 или выше. Также носите свободную одежду, которая максимально закрывает вас.
Усталость
Усталость — это чувство усталости или слабости, нежелание что-либо делать, неспособность сконцентрироваться или замедление.Через 2–3 недели лечения у вас может появиться усталость, которая может варьироваться от легкой до тяжелой. Усталость может длиться от 6 недель до 12 месяцев после окончания лечения.
Существует множество причин, по которым у вас может развиться утомляемость во время лечения, в том числе:
- Воздействие радиации на ваш организм.

- Поездки на лечение и обратно.
- Недостаток спокойного сна ночью.
- Недостаточное количество белка и калорий.
- Наличие боли или других симптомов.
- Чувство тревоги или депрессии.
- Некоторые лекарства.
Вы можете обнаружить, что в определенное время дня ваша утомляемость усиливается. Ниже приведены рекомендации, которые помогут вам справиться с усталостью.
Способы справиться с усталостью
- Если вы работаете и чувствуете себя хорошо, продолжайте это делать. Однако меньшая работа может повысить вашу энергию.
- Планируйте свою повседневную деятельность. Выбирайте те вещи, которые вам необходимы и наиболее важны, и делайте их, когда у вас будет больше всего энергии.Например, вы можете пойти на работу, но не работать по дому, или посмотреть спортивные соревнования своих детей, но не пойти на ужин.
- Планируйте время для отдыха или коротко вздремните (от 10 до 15 минут) в течение дня, особенно когда вы чувствуете большую усталость.
 Если вы спите, старайтесь спать меньше 1 часа за раз.
Если вы спите, старайтесь спать меньше 1 часа за раз. - Старайтесь спать хотя бы 8 часов каждую ночь. Это может быть больше сна, чем вам было нужно до начала лучевой терапии. Также может оказаться полезным ложиться спать раньше ночью и вставать позже утром.Один из способов лучше спать по ночам — быть активным днем. Например, если вы можете заниматься спортом, вы можете прогуляться, заняться йогой или покататься на велосипеде. Еще один способ лучше спать ночью — расслабиться перед сном. Вы можете прочитать книгу, поработать над головоломкой, послушать музыку или заняться успокаивающим хобби.
- Попросите семью и друзей помочь вам с покупками, приготовлением еды и уборкой. Узнайте в своей страховой компании, покрывают ли они услуги по уходу на дому.
- У некоторых людей появляется больше энергии, когда они тренируются.Спросите своего врача, можете ли вы выполнять легкие упражнения, такие как ходьба, растяжка или йога.
- Ешьте продукты с высоким содержанием белка и калорий.
 Попросите у медсестры материал «Правильное питание во время лечения рака».
Попросите у медсестры материал «Правильное питание во время лечения рака». - Другие симптомы, такие как боль, тошнота, диарея, проблемы со сном, чувство депрессии или беспокойства, могут усилить вашу утомляемость. Попросите вашего врача или медсестру помочь с любыми другими симптомами, которые могут у вас возникнуть.
Другие побочные эффекты
Некоторые люди могут испытывать другие побочные эффекты.Ваш онколог-радиолог или медсестра обсудят это с вами.
Сексуальное здоровье
Вы можете беспокоиться о том, как рак и ваше лечение могут повлиять на вашу сексуальность. Вы не радиоактивны. Вы не можете передать радиацию кому-либо еще, поэтому находиться в тесном контакте с другими людьми безопасно.
Вы можете вести половую жизнь во время лучевой терапии, если только ваш онколог-радиолог не даст вам других указаний. Однако, если вы или ваш партнер можете иметь детей, вы должны использовать противозачаточные средства (контрацепцию), чтобы предотвратить беременность во время лечения.
Американское онкологическое общество располагает ресурсами по вопросам сексуального здоровья во время лечения рака. Для мужчин — Секс и мужчина с раком . Женский — Секс и женщина с раком . Вы можете найти их на сайте www.cancer.org или получить копию по телефону 800-227-2345.
MSK также предлагает программы сексуального здоровья, которые помогут вам снизить влияние вашего заболевания и лечения на ваше сексуальное здоровье. Вы можете встретиться со специалистом до, во время или после лечения.
Эмоциональное здоровье
Диагностика и лечение рака могут быть очень тяжелыми и утомительными. Вы можете почувствовать:
|
|
Все эти типы чувств нормальны, если вы или кто-то из ваших близких серьезно заболели.
Вы также можете побеспокоиться о том, чтобы сообщить своему работодателю, что у вас рак, или об оплате медицинских счетов. Вы можете беспокоиться о том, как могут измениться ваши семейные отношения, о влиянии лечения рака на ваше тело или о том, сохраните ли вы свою сексуальную привлекательность. Вы можете волноваться, что рак вернется. Мы здесь, чтобы поддержать вас.
Способы справиться со своими чувствами
- Разговаривайте с другими людьми. Когда люди пытаются защитить друг друга, скрывая свои чувства, они могут чувствовать себя очень одинокими.Разговор может помочь окружающим узнать, о чем вы думаете. Возможно, вам будет полезно поговорить о своих чувствах с тем, кому вы доверяете. Вы можете поговорить со своим супругом или партнером, близким другом, членом семьи, капелланом, медсестрой, социальным работником или психологом. Вам также может быть полезно поговорить с кем-то, кто проходит лучевую терапию, или с человеком, пережившим рак, или с лицом, осуществляющим уход, который прошел подобное лечение.
 Благодаря нашей программе поддержки пациентов и лиц, осуществляющих уход, у вас есть возможность поговорить с бывшими пациентами и лицами, осуществляющими уход.Чтобы узнать больше об этой услуге, позвоните по телефону 212-639-5007.
Благодаря нашей программе поддержки пациентов и лиц, осуществляющих уход, у вас есть возможность поговорить с бывшими пациентами и лицами, осуществляющими уход.Чтобы узнать больше об этой услуге, позвоните по телефону 212-639-5007. - Присоединяйтесь к группе поддержки. Встреча с другими людьми, больными раком, даст вам возможность поговорить о своих чувствах и выслушать других людей, которые испытывают те же проблемы. Вы узнаете, как другие справляются со своим раком и лечением. Ваш врач, медсестра или социальный работник расскажут вам о группах поддержки, которые могут вас заинтересовать.
- Попробуйте расслабиться и медитировать. Вы можете попытаться представить себя в любимом месте, медленно дыша, обращая внимание на каждый вдох или слушая успокаивающую музыку или звук.Для некоторых людей молитва — это еще одна форма медитации. Подобные занятия помогут расслабиться и успокоиться.
- Упражнение. Многие люди считают, что легкие занятия, такие как ходьба, езда на велосипеде, йога или водная аэробика, помогают им чувствовать себя лучше.
 Поговорите со своим врачом или медсестрой о типах упражнений, которые вы можете выполнять.
Поговорите со своим врачом или медсестрой о типах упражнений, которые вы можете выполнять.
У всех нас есть свой способ справляться с трудными ситуациями. Обычно мы используем то, что сработало для нас в прошлом. Однако иногда этого недостаточно. Мы рекомендуем вам поговорить со своим врачом, медсестрой или социальным работником о ваших проблемах.
Вернуться наверхПосле лечения
Обязательно записывайтесь на прием к своему онкологу-радиологу. Он или она оценит вашу реакцию на лечение. Во время этих посещений у вас могут быть анализы крови, рентген и сканирование. Перед тем как приехать, запишите свои вопросы и опасения. Принесите это и список всех ваших лекарств с собой. Вы также можете позвонить своему врачу или медсестре в любое время после завершения лечения или в период между контрольными визитами, если у вас есть какие-либо вопросы или опасения.
Вернуться наверхКонтактная информация
Если у вас есть какие-либо вопросы или опасения, поговорите с членом вашей медицинской бригады. Вы можете связаться с ними с понедельника по пятницу с 9:00 до 17:00 по номерам, указанным ниже.
Вы можете связаться с ними с понедельника по пятницу с 9:00 до 17:00 по номерам, указанным ниже.
Радиолог-онколог: _________________________
Телефон: _________________________
Медсестра-радиолог: _________________________
Телефон: _________________________
После 17:00, в выходные и праздничные дни позвоните ____________ и спросите дежурного онколога-радиолога.Если в списке нет номера или вы не уверены, позвоните по номеру 212-639-2000.
Вернуться наверхРесурсы
Многие ресурсы, перечисленные в этом руководстве, можно найти в Интернете. Если у вас нет компьютера или вы не знаете, как пользоваться Интернетом, обратитесь в местную публичную библиотеку или общественный центр.
Служба поддержки МСК
Консультационный центр
646-888-0200
Многие люди считают, что консультирование им помогает.Мы предоставляем консультации для отдельных лиц, пар, семей и групп, а также лекарства, которые помогут, если вы чувствуете тревогу или депрессию.
Программа женской сексуальной медицины и женского здоровья
646-888-5076
Эта программа помогает женщинам-пациентам, которые борются с проблемами сексуального здоровья, связанными с раком, включая преждевременную менопаузу и проблемы фертильности.
Служба интегративной медицины
646-888-0800
Служба интегративной медицины MSK предлагает пациентам множество услуг в дополнение к традиционной медицинской помощи.К ним относятся музыкальная терапия, психотерапия / терапия тела, танцевальная и двигательная терапия, йога и сенсорная терапия.
Программа мужской сексуальной и репродуктивной медицины
646-888-6024
Эта программа помогает пациентам-мужчинам, которые сталкиваются с проблемами сексуального здоровья, связанными с раком, включая эректильную дисфункцию.
Служба питания
212-639-7312
Служба питания MSK предлагает консультации по питанию с одним из наших сертифицированных диетологов. Ваш диетолог рассмотрит ваши текущие привычки в еде и посоветует, что нужно есть во время и после лечения.
Ваш диетолог рассмотрит ваши текущие привычки в еде и посоветует, что нужно есть во время и после лечения.
Программа поддержки пациентов и лиц, осуществляющих уход Благодаря нашей Программе поддержки пациентов и опекунов мы можем предложить вам возможность поговорить с бывшими пациентами и опекунами.
Программа «Ресурсы для жизни после рака» (RLAC)
646-888-8106
В центре MSK уход не заканчивается после активного лечения. Программа RLAC предназначена для пациентов и их семей, завершивших лечение.Эта программа включает множество услуг, включая семинары, тренинги, группы поддержки, консультации по вопросам жизни после лечения, а также помощь по вопросам страхования и трудоустройства.
Программа лечения табака
212-610-0507
Если вы хотите бросить курить, в MSK есть специалисты, которые могут вам помочь. Звоните для получения дополнительной информации.
Внешние ресурсы
Американское онкологическое общество (ACS)
www. cancer.org
cancer.org
800-ACS-2345 (800-227-2345)
Предлагает разнообразную информацию и услуги, включая Hope Lodge, бесплатное место для проживания пациентов и лиц, осуществляющих уход во время лечения рака.
Американское общество терапевтической радиологии и онкологии
www.rtanswers.org
800-962-7876
Группа специалистов в области лучевой онкологии, специализирующаяся на лечении пациентов с помощью лучевой терапии. Предоставляет подробную информацию о лечении рака с помощью радиации и контактную информацию для онкологов-радиологов в вашем районе.
Рак Care
www.cancercare.org
800-813-HOPE (800-813-4673)
Седьмая авеню 275 (между улицами West 25 th и 26 th )
New York, NY 10001
Предоставляет консультации, группы поддержки, образовательные семинары, публикации и финансовую помощь.
Сообщество поддержки рака
www.cancersupportcommunity. org
org
Предоставляет поддержку и обучение людям, страдающим раком.
Информационная служба по раку Национального института рака (NCI)
www.cancer.gov
800-4-CANCER (800-422-6237)
Предоставляет образование и поддержку людям, больным раком, и их семьям. Публикации доступны в Интернете и в печати.
Вопросы, которые следует задать врачу или медсестре
Мы рекомендуем вам записать вопросы, которые нужно задать во время визита к врачу или медсестре.Запишите ответы во время встречи, чтобы вы могли еще раз просмотреть их позже.
Какую лучевую терапию я получу?
Сколько процедур я получу?
Какие побочные эффекты следует ожидать во время лучевой терапии?
Пройдут ли эти побочные эффекты после окончания лучевой терапии?
Какие поздние побочные эффекты следует ожидать после лучевой терапии?
Вернуться наверх
Радиация в медицине: процедуры медицинской визуализации
Медицинские визуализационные тесты — это неинвазивные процедуры, которые позволяют врачам диагностировать заболевания и травмы, не вмешиваясь в процесс. Некоторые из этих тестов связаны с воздействием ионизирующего излучения, которое может представлять опасность для пациентов. Однако, если пациенты понимают преимущества и риски, они могут принять наилучшее решение о выборе конкретной процедуры медицинской визуализации.
Некоторые из этих тестов связаны с воздействием ионизирующего излучения, которое может представлять опасность для пациентов. Однако, если пациенты понимают преимущества и риски, они могут принять наилучшее решение о выборе конкретной процедуры медицинской визуализации.
Большинство людей прошли один или несколько тестов с медицинской визуализацией. Процедуры визуализации — это медицинские тесты, которые позволяют врачам заглядывать внутрь тела, чтобы диагностировать, лечить и контролировать состояние здоровья. Врачи часто используют медицинские процедуры визуализации, чтобы определить наилучшие варианты лечения для пациентов.Тип процедуры визуализации, которую может предложить ваш врач, будет зависеть от вашего состояния здоровья и части тела, которую исследуют. Вот некоторые распространенные примеры визуализационных тестов:
Если ваш врач предлагает рентгеновские снимки или другие медицинские методы визуализации, вам следует принять во внимание следующее:
- Медицинские визуализационные тесты следует выполнять только при необходимости.

- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) рекомендует обсудить с врачом преимущества и риски процедур медицинской визуализации.
Преимущества и риски процедур медицинской визуализации с использованием ионизирующего излучения
Медицинские визуализационные тесты могут помочь врачам:
- Получите лучший обзор органов, кровеносных сосудов, тканей и костей.
- Определите, является ли операция хорошим вариантом лечения.
- Проводить медицинские процедуры, включающие размещение катетеров, стентов или других устройств внутри тела, определять местонахождение опухолей для лечения и обнаруживать сгустки крови или другие препятствия.
- Руководство по вариантам замены сустава и лечению переломов.
Как и во многих областях медицины, существуют риски, связанные с использованием медицинской визуализации, в которой для создания изображений тела используется ионизирующее излучение. Риски от воздействия ионизирующего излучения включают:
Риски от воздействия ионизирующего излучения включают:
- Небольшое увеличение вероятности того, что у человека, подвергшегося облучению, в более позднем возрасте разовьется рак.
- Последствия для здоровья, которые могут возникнуть после сильного острого воздействия ионизирующего излучения, например, покраснение кожи и выпадение волос.
- Возможные аллергические реакции, связанные с введением контрастного красителя в вены, чтобы лучше видеть исследуемые структуры тела.
Как можно снизить воздействие диагностического ионизирующего излучения?
В случае рентгеновских лучей или других тестов, связанных с воздействием ионизирующего излучения, врачи и специалисты по радиационной безопасности могут помочь снизить ваше воздействие и риск вреда от диагностического ионизирующего излучения:
- Проверка, не проходили ли вы недавно аналогичный тест, который может предоставить им необходимую справочную информацию.
- Проверка, может ли тест, не использующий ионизирующее излучение, предоставить аналогичную информацию.

- Убедитесь, что для вашей процедуры используется минимально возможное количество излучения, необходимое для получения изображения хорошего качества.
- Обеспечивает защитный свинцовый экран для предотвращения воздействия радиации на другие части тела.
Каковы риски процедур медицинской визуализации для беременных?
Поговорите со своим врачом о потенциальных рисках и преимуществах медицинских процедур. Во многих случаях риск рентгеновской процедуры для матери и будущего ребенка очень мал по сравнению с выгодой от получения информации о состоянии здоровья матери или ребенка.
Однако не следует идти на небольшой риск, если он не нужен. Вы можете снизить риски, связанные с процедурами медицинской визуализации, сообщив своему врачу, беременны ли вы или думаете, что беременны, всякий раз, когда врач предлагает сделать рентген брюшной полости. Другие варианты, предложенные FDA, которые могут быть рассмотрены, следующие:
- Если вы беременны, врач может решить, что лучше всего отменить процедуру визуализации, отложить ее или изменить, чтобы уменьшить количество радиации.

- В зависимости от ваших медицинских потребностей и понимания того, что риск очень мал, врач может посчитать, что лучше продолжить процедуру медицинской визуализации в соответствии с планом.
В любом случае вы можете обсудить решение со своим врачом. Для получения дополнительной информации о медицинской визуализации и беременности см. Рентген, беременность и вы. Внешний значок. Кроме того, для получения дополнительной информации о радиационной безопасности при медицинской визуализации взрослых посетите внешний значок веб-сайта Image Wisely.
Есть ли особые рекомендации для детей?
Важно, чтобы при рентгенографии и других процедурах визуализации детей использовалась минимальная экспозиция, необходимая для получения хорошего клинического изображения. Внешний значок Image Gently Alliance, являющийся частью Альянса радиационной диагностики в педиатрической визуализации, предлагает следующее для визуализации детей:
- Используйте визуализацию, когда медицинская польза превышает риск.

- Используйте наиболее подходящие методы визуализации, соответствующие росту ребенка.
- По возможности используйте альтернативные методы визуализации (например, ультразвук или МРТ).
Для получения дополнительной информации о процедурах медицинской визуализации, не использующих ионизирующее излучение, см. «Радиация в медицине: процедуры медицинской визуализации».
Внешний значок FDA также предоставляет информацию родителям, пациентам и поставщикам медицинских услуг для решения проблем, связанных с преимуществами и рисками процедур медицинской визуализации для детей.
Пожалуйста, посетите веб-сайт CDC «Радиация и ваше здоровье» для получения дополнительной информации.
Белая книга: Инициатива по сокращению ненужного радиационного облучения от медицинских изображений
Версия принтера PDF
(300 КБ)
Содержание
Краткое содержание
Как и все медицинские процедуры, компьютерная томография (КТ), рентгеноскопия и визуализация ядерной медицины представляют как преимущества, так и риски. Эти типы процедур визуализации привели к улучшениям в диагностике и лечении множества заболеваний. В то же время эти типы обследований подвергают пациентов воздействию ионизирующего излучения (далее «радиация»), которое может повысить риск развития рака на протяжении всей жизни человека. Сбалансированный подход к общественному здравоохранению направлен на поддержку преимуществ этих медицинских визуализационных обследований при минимизации рисков.
Эти типы процедур визуализации привели к улучшениям в диагностике и лечении множества заболеваний. В то же время эти типы обследований подвергают пациентов воздействию ионизирующего излучения (далее «радиация»), которое может повысить риск развития рака на протяжении всей жизни человека. Сбалансированный подход к общественному здравоохранению направлен на поддержку преимуществ этих медицинских визуализационных обследований при минимизации рисков.
Управление рисками процедур компьютерной томографии (КТ), рентгеноскопии и ядерной медицины зависит от двух принципов радиационной защиты: соответствующее обоснование для заказа и выполнения каждой процедуры и тщательная оптимизация дозы облучения, используемой во время каждой процедуры .Эти типы визуализационных исследований следует проводить только при наличии медицинского обоснования. При проведении таких обследований пациенты должны получать оптимальную дозу облучения — не больше или меньше, чем необходимо для получения высококачественного изображения./GettyImages-101883469-26e53948c73f40ae911d40b7d32586c6.jpg) Другими словами, каждый пациент должен получить правильную визуализацию в нужное время с правильной дозой облучения.
Другими словами, каждый пациент должен получить правильную визуализацию в нужное время с правильной дозой облучения.
FDA может способствовать достижению этой цели, разумно используя наш регулирующий орган, а также сотрудничая с профессиональным сообществом здравоохранения.
В этом документе объявляется о запуске совместной инициативы по сокращению ненужного радиационного облучения от медицинских изображений . В рамках этой инициативы FDA и наши партнеры предпримут следующие шаги:
- Содействовать безопасному использованию медицинских устройств визуализации;
- Поддержка принятия обоснованных клинических решений; и
- Повысьте осведомленность пациентов.
Координируя эти усилия, мы можем оптимизировать облучение пациентов при определенных типах медицинских визуализационных обследований и, таким образом, снизить связанные с этим риски при максимальном использовании преимуществ этих исследований.
Фон
Процедуры медицинской визуализации, которые используются для просмотра различных областей внутри человеческого тела, могут предоставить врачам важную клиническую информацию. Визуализирующие обследования могут позволить неинвазивную диагностику заболевания и мониторинг терапии, а также могут помочь в планировании медицинского и хирургического лечения. Для многих заболеваний раннее выявление, более эффективная диагностика и улучшенный мониторинг терапии с использованием визуализационных исследований могут способствовать снижению заболеваемости, дополнительным вариантам лечения и увеличению продолжительности жизни. 1 Методы управления изображением также широко используются в различных процедурах, таких как установка катетеров или стентов, удаление сгустков крови или других закупорок.
Визуализирующие обследования могут позволить неинвазивную диагностику заболевания и мониторинг терапии, а также могут помочь в планировании медицинского и хирургического лечения. Для многих заболеваний раннее выявление, более эффективная диагностика и улучшенный мониторинг терапии с использованием визуализационных исследований могут способствовать снижению заболеваемости, дополнительным вариантам лечения и увеличению продолжительности жизни. 1 Методы управления изображением также широко используются в различных процедурах, таких как установка катетеров или стентов, удаление сгустков крови или других закупорок.
1. Типы процедур медицинской визуализации
Существует множество типов — или модальностей — процедур медицинской визуализации, в каждой из которых используются разные технологии и методы. Ультразвуковая визуализация (также называемая сонографией) использует высокочастотные звуковые волны для просмотра мягких тканей, таких как мышцы и внутренние органы. Магнитно-резонансная томография (МРТ) использует радиоволны и магнитные поля для получения изображений.
Магнитно-резонансная томография (МРТ) использует радиоволны и магнитные поля для получения изображений.
В отличие от ультразвука и МРТ, проекционная радиография (обычно называемая стандартным рентгеновским снимком), компьютерная томография, рентгеноскопия и процедуры ядерной медицины используют ионизирующее излучение для создания изображений тела. Ионизирующее излучение — это форма излучения, обладающая достаточной энергией, чтобы потенциально вызвать повреждение ДНК. Люди ежедневно подвергаются воздействию естественного ионизирующего излучения определенного фонового уровня. 2
В этих различных процедурах визуализации используется разное количество ионизирующего излучения.В процедурах проекционной радиографии, которые включают рентген грудной клетки и маммографию, используется относительно небольшое количество излучения. (См. Таблицу 1 ниже, где указаны типичные дозы облучения от стоматологического рентгена, рентгеновского снимка грудной клетки и маммографии. ) В этих исследованиях устройство пропускает рентгеновские лучи через тело пациента, чтобы произвести от одного до нескольких из двух. -размерные изображения — так называемые рентгенограммы — определенной области тела. В то время как проекционная рентгенография, включая маммографию, составляет примерно 74% процедур визуализации с использованием излучения, которые ежегодно проводятся в США.S., он составляет лишь 11% от общего годового облучения по данным медицинской визуализации. 3
) В этих исследованиях устройство пропускает рентгеновские лучи через тело пациента, чтобы произвести от одного до нескольких из двух. -размерные изображения — так называемые рентгенограммы — определенной области тела. В то время как проекционная рентгенография, включая маммографию, составляет примерно 74% процедур визуализации с использованием излучения, которые ежегодно проводятся в США.S., он составляет лишь 11% от общего годового облучения по данным медицинской визуализации. 3
Во время компьютерной томографии (также называемой компьютерной томографией) вращающийся источник пропускает рентгеновские лучи через тело пациента, чтобы получить несколько изображений поперечного сечения определенной области. Эти двухмерные изображения также можно объединить в цифровом виде для создания единого трехмерного изображения. В рентгеноскопической процедуре устройство пропускает рентгеновские лучи через тело пациента в течение короткого промежутка времени для получения движущегося изображения в реальном времени, которое можно использовать для наблюдения за движением объекта или вещества в теле. Во время процедуры ядерной медицины, такой как сканирование с помощью позитронно-эмиссионной томографии (ПЭТ), пациенту вводят небольшое количество радиоактивного вещества, называемого радиофармпрепаратом или радиоактивным индикатором. Затем используется детектор вне тела для просмотра изображения радиоактивного материала, движущегося через тело.
Во время процедуры ядерной медицины, такой как сканирование с помощью позитронно-эмиссионной томографии (ПЭТ), пациенту вводят небольшое количество радиоактивного вещества, называемого радиофармпрепаратом или радиоактивным индикатором. Затем используется детектор вне тела для просмотра изображения радиоактивного материала, движущегося через тело.
Поскольку процедуры компьютерной томографии, рентгеноскопии и ядерной медицины включают многократное или продолжительное воздействие радиации, эти типы исследований связаны с более высокой дозой облучения, чем проекционная радиография.Например, эффективная доза для взрослых при компьютерной томографии головы эквивалентна эффективной дозе для взрослых при примерно 100 рентгеновских снимках грудной клетки. Эффективная доза для взрослых при КТ брюшной полости примерно эквивалентна эффективной дозе для взрослых при примерно 400 рентгеновских снимках грудной клетки. 4 (диапазон доз от различных процедур КТ, рентгеноскопии и ядерной медицины см. В Таблице 1 ниже). В то время как исследования КТ, интервенционной рентгеноскопии и ядерной медицины составляют лишь приблизительно 26% процедур визуализации с использованием излучения, которое проводятся ежегодно в США.S., они составляют 89% от общего годового облучения по данным медицинской визуализации. 5
В Таблице 1 ниже). В то время как исследования КТ, интервенционной рентгеноскопии и ядерной медицины составляют лишь приблизительно 26% процедур визуализации с использованием излучения, которое проводятся ежегодно в США.S., они составляют 89% от общего годового облучения по данным медицинской визуализации. 5
Таблица 1. Дозы излучения при различных типах процедур медицинской визуализации 6
| Тип процедуры | Средняя эффективная доза для взрослых (мЗв) | Расчетный эквивалент дозы (Количество рентгеновских снимков грудной клетки) |
|---|---|---|
| Стоматологический рентген | 0.005-0.01 6a | 0,25-0,5 |
| Рентген грудной клетки | 0,02 | 1 |
| Маммография | 0,4 | 20 |
| CT | 2-16 6b | 100-800 |
| Nuclear Medicine | 0,2-41 6c | 10-2050 |
| Интервенционная рентгеноскопия | 5-70 6д | 250-3500 |
2.
 Опасения по поводу радиационного облучения
Опасения по поводу радиационного облученияСогласно отчету Национального совета по радиационной защите и измерениям (NCRP) за март 2009 года, общее воздействие ионизирующего излучения на население США почти удвоилось за последние два десятилетия. 7 Этот рост во многом объясняется увеличением облучения от компьютерной томографии, ядерной медицины и интервенционной рентгеноскопии. 8 По оценкам NCRP, в США было выполнено 67 миллионов компьютерных томографов, 18 миллионов процедур ядерной медицины, 17 миллионов процедур интервенционной рентгеноскопии и 18 миллионов процедур ядерной медицины.С. в 2006 г., и авторы прогнозируют, что эти цифры будут продолжать расти. 9
Высказывались опасения по поводу рисков, связанных с облучением пациентов при медицинской визуализации. Поскольку ионизирующее излучение может вызвать повреждение ДНК, воздействие может повысить риск развития рака на протяжении всей жизни человека. Хотя риск для человека от одного обследования сам по себе не может быть большим, ежегодно проводятся миллионы обследований, что делает радиационное облучение от медицинских изображений важной проблемой для общественного здравоохранения. 10 Беррингтон де Гонсалес и др. По оценкам, примерно 29 000 будущих раковых заболеваний могут быть связаны с компьютерной томографией, проведенной в США в 2007 году. 11 Smith-Bindman et al. подсчитали, что у 1 из 270 женщин и 1 из 600 мужчин, которые проходят КТ-коронарную ангиографию в возрасте 40 лет, разовьется рак после этого КТ-сканирования; риски для 20-летних примерно вдвое выше, а для 60-летних примерно вдвое меньше. 12 Хотя эксперты могут расходиться во мнениях относительно степени риска рака по данным медицинской визуализации, существует единое мнение о том, что следует тщательно взвесить медицинскую необходимость данного уровня радиационного облучения с рисками.
10 Беррингтон де Гонсалес и др. По оценкам, примерно 29 000 будущих раковых заболеваний могут быть связаны с компьютерной томографией, проведенной в США в 2007 году. 11 Smith-Bindman et al. подсчитали, что у 1 из 270 женщин и 1 из 600 мужчин, которые проходят КТ-коронарную ангиографию в возрасте 40 лет, разовьется рак после этого КТ-сканирования; риски для 20-летних примерно вдвое выше, а для 60-летних примерно вдвое меньше. 12 Хотя эксперты могут расходиться во мнениях относительно степени риска рака по данным медицинской визуализации, существует единое мнение о том, что следует тщательно взвесить медицинскую необходимость данного уровня радиационного облучения с рисками.
Случайное воздействие очень высоких доз радиации также может вызвать краткосрочные травмы, такие как ожоги и выпадение волос. Прямое воздействие таких доз на глаза может увеличить риск развития катаракты. FDA в настоящее время расследует несколько недавних случаев острого чрезмерного облучения при КТ-сканировании перфузии головного мозга. 13 В каждом из этих случаев пациенты получали гораздо более высокую дозу радиации, чем обычно при таких сканированиях.
13 В каждом из этих случаев пациенты получали гораздо более высокую дозу радиации, чем обычно при таких сканированиях.
3. Ненужное облучение
Поскольку компьютерная томография, рентгеноскопия и ядерная медицина требуют использования радиации, этим типам процедур присущ некоторый уровень радиационного облучения.Тем не менее, когда эти процедуры выполняются надлежащим образом, медицинские преимущества, которые они могут обеспечить, обычно перевешивают риски.
Однако, если не принять надлежащих мер предосторожности, пациенты могут подвергнуться облучению без клинической необходимости или пользы. Ненужное облучение может быть результатом использования дозы облучения, превышающей оптимальную для удовлетворения клинических потребностей данной процедуры. В какой-то момент использование более высокой дозы облучения может дать изображение с более высоким разрешением. Если доза слишком мала, качество результирующего изображения может быть плохим, и, как результат, врач не сможет сделать точное клиническое определение. Оптимальная доза облучения — это минимально достижимая малая доза при сохранении достаточного качества изображения для удовлетворения клинических потребностей.
Оптимальная доза облучения — это минимально достижимая малая доза при сохранении достаточного качества изображения для удовлетворения клинических потребностей.
Ненужное облучение может также быть результатом выполнения определенной процедуры медицинской визуализации, когда это не оправдано с медицинской точки зрения с учетом признаков и симптомов пациента или когда альтернатива может быть предпочтительнее, учитывая всю историю радиационного облучения пациента.
Существует широкое согласие с тем, что следует принимать меры для уменьшения ненужного облучения.
Факторы, способствующие ненужному облучению
Несколько факторов могут способствовать ненужному облучению при медицинских исследованиях.
1. Проблемы, связанные с использованием устройства
Высказывались опасения по поводу того, как центры визуализации проводят медицинские визуализационные обследования, в которых используется излучение: наблюдались широкие различия между дозами облучения, связанными с конкретными типами медицинских визуальных обследований. Например, изучая компьютерную томографию, проведенную на взрослых пациентах в нескольких учреждениях в районе залива Сан-Франциско, Smith-Bindman et al.Сообщите о среднем 13-кратном разбросе между самой высокой и самой низкой дозой для каждого типа оцениваемого исследования. 14 Столь большие различия в дозах облучения требуют стандартизации и говорят о необходимости повышения качества.
Например, изучая компьютерную томографию, проведенную на взрослых пациентах в нескольких учреждениях в районе залива Сан-Франциско, Smith-Bindman et al.Сообщите о среднем 13-кратном разбросе между самой высокой и самой низкой дозой для каждого типа оцениваемого исследования. 14 Столь большие различия в дозах облучения требуют стандартизации и говорят о необходимости повышения качества.
Практикующие врачи, использующие медицинское оборудование для визуализации, могут не иметь адекватной информации или всестороннего понимания дозы облучения и связанных с ними процессов обеспечения качества для обеспечения качества, согласованности и радиационной безопасности при обследовании с помощью медицинской визуализации.Например, в то время как новые КТ и рентгеноскопические устройства включают отображение показателей дозы, в некоторых отсутствуют другие меры безопасности, такие как настройки параметров по умолчанию, которые оптимизируют дозу облучения или предупреждают, когда доза облучения в данном исследовании превышает определенный референсный уровень или диапазон. Поскольку современные методы измерения дозы облучения в значительной степени основаны на моделях для взрослых, получение значимых показателей дозы в реальном времени для педиатрических процедур может быть особенно сложной задачей. FDA занимается улучшением и установлением стандартов для расчета доз для детей.
Поскольку современные методы измерения дозы облучения в значительной степени основаны на моделях для взрослых, получение значимых показателей дозы в реальном времени для педиатрических процедур может быть особенно сложной задачей. FDA занимается улучшением и установлением стандартов для расчета доз для детей.
Нормы дозы облучения пациента называются «диагностическими контрольными уровнями» или «контрольными значениями дозы», и они обычно соответствуют точкам 75-го или 80-го процентиля распределения значений измеренных доз для конкретных процедур визуализации. 15 Диагностические референтные уровни — это эталоны, с которыми можно сравнить практику учреждения в программе обеспечения качества радиационной защиты: когда диагностический референтный уровень превышается при любом конкретном обследовании, учреждение может провести расследование, чтобы увидеть, можно ли снизить облучение без ухудшения качества изображения.
Группы, включая Американский колледж радиологии (ACR), Американскую ассоциацию физиков в медицине (AAPM) и NCRP, провели работу по установлению признанных на национальном уровне диагностических референтных уровней для многих процедур визуализации, и FDA было активным участником этих усилий. . 16 Однако функции безопасности оборудования предупреждают операторов и интерпретируют врачей о дозах, которые превышают диагностические референсные уровни или превышают пиковую дозу на кожу. 17 пороговые значения для радиационно-индуцированного поражения кожи еще не стандартизированы.Кроме того, существует множество процедур медицинской визуализации, особенно для педиатрических пациентов, для которых референтные диагностические уровни еще не установлены. Без диагностических референсных уровней практикующим специалистам сложно оценить, попадает ли доза облучения, использованная во время данного исследования, в разумные пределы.
. 16 Однако функции безопасности оборудования предупреждают операторов и интерпретируют врачей о дозах, которые превышают диагностические референсные уровни или превышают пиковую дозу на кожу. 17 пороговые значения для радиационно-индуцированного поражения кожи еще не стандартизированы.Кроме того, существует множество процедур медицинской визуализации, особенно для педиатрических пациентов, для которых референтные диагностические уровни еще не установлены. Без диагностических референсных уровней практикующим специалистам сложно оценить, попадает ли доза облучения, использованная во время данного исследования, в разумные пределы.
Даже при наличии средств защиты оборудования пользователи могут не пройти надлежащую подготовку по правильному использованию этих функций и важности оптимизации дозы облучения.Кроме того, учреждения по визуализации могут не иметь надлежащих методов обеспечения качества, таких как регулярная оценка их протоколов исследований и оборудования.
Некоторые шаги были предприняты для решения этих проблем. В рамках кампаний Image Gently и Step Lightly Альянс за радиационную безопасность в педиатрической визуализации разработал учебные материалы для педиатров, радиологов, техников-радиологов и родителей, чтобы поощрять осторожное использование компьютерной томографии и интервенционной рентгеноскопии у детей. 18 Эти кампании разработаны для повышения осведомленности о способах снижения дозы облучения при педиатрических процедурах визуализации. ACR и Радиологическое общество Северной Америки (RSNA) в настоящее время разрабатывают кампанию Image Wisely, в которой те же принципы будут применяться к взрослым пациентам.
2. Вопросы, связанные с принятием клинических решений
Также высказывались опасения, что врачам может не хватать важной информации, которая могла бы послужить основой для их решений при назначении медицинских визуальных исследований с использованием радиации.
Лечащие врачи могут не иметь доступа к медицинской визуализации пациентов или истории доз облучения. Из-за недостатка информации врачи могут без необходимости заказывать процедуры визуализации, которые уже были проведены. Кроме того, стандартизованная отчетность со структурированной дозой, технически доступная в новых системах компьютерной томографии и флюороскопах, используемых в интервенционных процедурах, все еще находится в зачаточном состоянии; Отчеты о дозах обычно не связаны средствами обслуживания ни с файлами изображений, ни с медицинскими картами пациентов.Если у врача была запись о дозе радиации, которой пациент подвергался в предыдущих процедурах медицинской визуализации, такая информация могла бы повлиять на его или ее решение назначить обследование определенного типа.
В некоторых случаях лечащие врачи могут не знать или не знать рекомендуемых критериев для принятия решений о том, является ли конкретная процедура визуализации эффективной с медицинской точки зрения. В результате они могут без достаточных оснований заказывать процедуры визуализации и подвергать пациентов облучению без надобности.Различные профессиональные организации, в том числе ACR и Американский колледж кардиологии (ACC), разработали и работают над распространением критериев направления на визуализацию, называемых «критериями соответствия» или «критериями надлежащего использования», связанных с рядом заболеваний. 18 Тем не менее, критерии для надлежащего порядка проведения медицинских исследований изображений еще не получили широкого распространения в практикующем медицинском сообществе.
Инициатива по сокращению ненужного радиационного облучения от медицинских изображений
FDA запускает совместную инициативу по сокращению ненужного радиационного облучения от медицинских изображений , уделяя особое внимание типам процедур визуализации, которые связаны с самыми высокими дозами радиации: компьютерной томографии, рентгеноскопии и ядерной медицине.
В рамках этой инициативы FDA предпримет шаги — напрямую и в сотрудничестве с другими — для смягчения факторов, способствующих ненужному облучению от этих трех методов медицинской визуализации. Цель этих усилий — поддержать преимущества, связанные с медицинской визуализацией, при минимизации рисков. Поскольку некоторые из описанных выше факторов не входят в компетенцию FDA, мы также рекомендуем другим группам дополнительные действия, которые будут поддерживать нашу работу.FDA будет сотрудничать с нашими партнерами и другими сторонами для мониторинга и оценки результатов этих усилий.
1. Содействовать безопасному использованию устройств медицинской визуализации
Надзор FDA за медицинскими устройствами распространяется на весь жизненный цикл продукта, от разработки до использования. FDA предпримет следующие действия для обеспечения безопасного использования медицинского оборудования для визуализации.
1.1. Установить требования к производителям КТ и рентгеноскопических устройств по включению дополнительных мер безопасности в дизайн оборудования, маркировку и обучение пользователей.FDA выпустит целевые требования для производителей КТ и рентгеноскопических устройств, чтобы включить важные дополнительные меры безопасности в конструкцию этих машин, разработать более безопасные технологии и обеспечить дополнительное обучение для поддержки безопасного использования практикующими врачами. В качестве первого шага FDA намерено провести открытое собрание 30 и 31 марта 2010 г., чтобы запросить мнение о том, какие требования устанавливать. FDA может потребовать, например, чтобы компьютерная томография и рентгеноскопические устройства отображали, регистрировали и сообщали о дозе облучения и предупреждали пользователей, когда доза превышает диагностический референсный уровень, пиковый порог кожной дозы для повреждения или какое-либо другое установленное значение.FDA может также потребовать от производителей предоставить дополнительные данные в своих предпродажных материалах для поддержки конкретных клинических применений и включить эту информацию в маркировку продуктов и обучение, чтобы повысить безопасность использования этих устройств.
1.2. Сотрудничайте с центрами услуг Medicare и Medicaid (CMS), чтобы включить ключевые методы обеспечения качества в критерии аккредитации и участия для учреждений визуализации и больниц.В соответствии с Законом об улучшении медицинских услуг для пациентов и поставщиков медицинских услуг (MIPPA), 20 CMS наблюдает за аккредитацией автономных медицинских учреждений визуализации. 21 Кроме того, CMS установила условия участия для больниц и сопроводительные инструкции для инспекторов Medicare. 22
FDA работает с CMS и ее назначенными организациями по аккредитации, чтобы поддержать включение ключевых практик обеспечения качества в критерии аккредитации MIPPA для автономных средств визуализации. FDA и CMS также изучают варианты улучшения существующих инструкций по интерпретации для больниц, связанных с их услугами радиологической и ядерной медицины.FDA традиционно встраивает инструкции по обеспечению качества в маркировку продукта и обучение, чтобы способствовать безопасному использованию. Сотрудничество с CMS поможет повысить качество обслуживания пользователей и в дальнейшем будет способствовать безопасному использованию медицинского оборудования для визуализации.
1.3. Рекомендовать профессиональному сообществу здравоохранения в сотрудничестве с FDA продолжать усилия по разработке диагностических референтных уровней для процедур компьютерной томографии, рентгеноскопии и ядерной медицины на местном уровне, а также через национальный регистр доз облучения.Опираясь на усилия различных профессиональных организаций, таких как ACR и NCRP, FDA рекомендует медицинским организациям продолжать разработку признанных на национальном уровне диагностических референтных уровней для процедур медицинской визуализации, в которых используется излучение, включая педиатрические процедуры. FDA расширит наше участие в этих усилиях. Например, мы будем сотрудничать с другими в разработке инструментов для сбора более значимых данных о дозах облучения на объектах пользователей, чтобы поддержать установление более точных диагностических контрольных уровней.Эти уровни будут способствовать обеспечению качества и безопасному использованию медицинских устройств визуализации, помогая практикующим специалистам оценить, является ли доза облучения, используемая во время данного обследования, разумной.
Для процедур, для которых такие нормы еще не разработаны на национальном уровне, FDA рекомендует, чтобы каждое пользовательское учреждение, насколько это возможно, разработало свои собственные местные диагностические референсные уровни для использования до тех пор, пока не станут доступны более широко признанные уровни.
Регистр доз облучения — это совокупность данных о дозах облучения пациентов, не идентифицируемых в результате индивидуальных медицинских визуализационных исследований.Путем объединения данных о дозах по всем учреждениям визуализации по всей стране национальный регистр доз облучения 23 поможет поддержать разработку диагностических референсных уровней там, где они еще не существуют, и позволит провести широкую проверку тех уровней, которые были разработаны на сегодняшний день. 24
Такой реестр также поможет установкам сравнивать свои дозы облучения с дозами других источников и может быть ключевым источником информации о тенденциях изменения доз во времени. Рафф, Чиннайян, Доля и др.недавно использовал реестр доз для кардиальной КТ-ангиографии в Мичигане, чтобы измерить эффективность применения избранных передовых методов снижения доз. 25
2. Поддержка принятия обоснованных клинических решений
FDA не наблюдает за медицинской практикой; однако существуют прямые и косвенные действия, которые FDA может предпринять, чтобы предоставить медицинским работникам инструменты, которые будут информировать их о решениях в отношении медицинской визуализации.
2.1. Установить требования к производителям КТ и рентгеноскопических устройств по регистрации информации о дозах облучения для использования в медицинских записях пациентов или реестре доз облучения.FDA выпустит целевые требования для производителей КТ и рентгеноскопических устройств, чтобы включить в них функции оборудования, которые предоставят клиницистам дополнительную информацию для принятия решений. В качестве первого шага FDA намерено провести открытое собрание 30 и 31 марта 2010 г., чтобы запросить мнение наших внешних клиентов о том, какие требования следует установить.FDA может потребовать, например, чтобы компьютерная томография и рентгеноскопические устройства были способны выполнять определенные функции, такие как получение значения дозы излучения от каждого исследования и связывание его с исследуемым изображением для облегчения хранения информации о дозе в бумажной или электронной медицинской карте пациента . FDA может также потребовать, чтобы устройства были способны автоматически записывать информацию о дозе облучения в стандартизированный структурированный отчет по цифровым изображениям и коммуникациям в медицине (DICOM) и передавать эту информацию в электронную медицинскую карту пациента или реестр доз.Такие шаги предоставят врачам более полную информацию о визуализации пациента и истории доз облучения, чтобы поддержать их решения о наиболее подходящем клиническом курсе действий для каждого пациента.
2.2. Рекомендовать профессиональному сообществу здравоохранения продолжать разработку и принятие критериев для надлежащего использования процедур компьютерной томографии, рентгеноскопии и ядерной медицины или других процедур, в которых используются эти методы.Опираясь на усилия различных профессиональных организаций, включая ACR и ACC, FDA рекомендует профессиональному сообществу здравоохранения продолжать разработку и принятие соответствующих критериев использования для процедур компьютерной томографии, рентгеноскопии и ядерной медицины.Электронные средства поддержки принятия решений для заказа процедур визуализации могут включать эти критерии для повышения качества и согласованности принятия клинических решений.
3. Повышение осведомленности пациентов
По мере того, как усилия, описанные выше, продолжаются, FDA признает важность предоставления пациентам информации и инструментов, которые помогут им и их врачам контролировать свое воздействие радиации на основе медицинских изображений в краткосрочной перспективе, даже до того, как долгосрочные изменения вступят в силу.
3.1. Предоставьте пациентам инструменты для отслеживания их личной истории болезни.FDA сотрудничает с совместной рабочей группой ACR и RSNA, которая в настоящее время координирует Image Wisely, чтобы разработать и распространить карту записи медицинских изображений пациента. 26 FDA разместит эту карту на нашем веб-сайте. Хотя в конечном итоге лучшим способом отслеживания истории радиационного облучения пациента будет включение ее в бумажную или электронную медицинскую карту пациента, личная учетная карточка даст пациентам и их опекунам средство в краткосрочной перспективе отслеживать их собственное медицинское историй изображений и обмена этой информацией со своими врачами.Это поможет облегчить критические дискуссии между пациентами и поставщиками медицинских услуг о лучших доступных клинических вариантах.
Заключение
Медицинская визуализация имеет много важных клинических применений и может дать значительные преимущества. Однако компьютерная томография, рентгеноскопия и методы визуализации ядерной медицины также представляют опасность. Сбалансированный подход к общественному здравоохранению направлен на поддержку преимуществ медицинской визуализации при одновременном снижении рисков. FDA, другие представители федерального правительства и профессиональное сообщество здравоохранения должны сыграть свою роль в таком подходе.В рамках Инициативы по сокращению ненужного облучения от медицинских изображений FDA и наши партнеры будут работать над значительным сокращением ненужного облучения пациентов при КТ, рентгеноскопии и исследованиях ядерной медицины.
1 См., Например, точку зрения Обуховски Н.А. и др. «Десять критериев эффективного скрининга: их применение для мультиспирального КТ-скрининга легочного и колоректального рака», Американский журнал рентгенологии , июнь 2001 г., Vol.176, стр. 1357-1362.
2 Средняя эффективная доза от фонового излучения составляет около 3 мЗв в год. (Mettler, Jr. FA, et al., Эффективные дозы в радиологии и диагностической ядерной медицине: каталог, Radiology , июль 2008 г., том 248, № 1, стр. 254-263.)
3 Национальный совет по радиационной защите и измерениям, Отчет NCRP № 160: Воздействие ионизирующего излучения на население США, , 3 марта 2009 г., стр.142-146.
4 Здесь средние эффективные дозы для взрослых при КТ-исследованиях головы (2 мЗв) и живота (8 мЗв) сравниваются со средней эффективной дозой для взрослых при задне-переднем рентгеновском снимке грудной клетки (0,02 мЗв). (Mettler, Jr. FA, et al., Июль 2008 г.)
5 Национальный совет по радиационной защите и измерениям, Отчет NCRP № 160 , март 2009 г., стр. 142-146.
6 В таблице 1 средние эффективные дозы для взрослых при различных типах исследований сравниваются со средней эффективной дозой для взрослых при задне-передней рентгенографии грудной клетки (0.02 мЗв). Дополнительная информация представлена ниже. (Mettler, Jr. FA, et al., Июль 2008 г.)
6a 0,005 мЗв — средняя эффективная доза для взрослого человека при внутриротовом рентгеновском снимке. 0,01 мЗв — средняя эффективная доза для взрослого человека при панорамном рентгеновском снимке зубов.
6b 2 мЗв — средняя эффективная доза для взрослого человека при компьютерной томографии головы. 16 мЗв — это средняя эффективная доза для взрослого человека при КТ-коронарной ангиографии.
6c 0,2 мЗв — средняя эффективная доза для взрослого человека при исследовании вентиляции легких с использованием 99mTc-DTPA.41 мЗв — это средняя эффективная доза для взрослого человека в результате сердечного стресс-теста и отдыха с использованием хлорида таллия 201.
6d 5 мЗв — средняя эффективная доза для взрослого при ангиографии головы и / или шеи. 70 мЗв — средняя эффективная доза для взрослых при размещении трансъюгулярного внутрипеченочного портосистемного шунта.
7 В начале 1980-х годов воздействие ионизирующего излучения из всех источников на душу населения в США составляло 3,6 мЗв. К 2006 году эта цифра выросла до 6.25 мЗв. (Национальный совет по радиационной защите и измерениям, Отчет NCRP No. 160 , март 2009 г., стр. 242-243.)
8 В начале 1980-х годов на медицинскую визуализацию приходилось 15% воздействия ионизирующего излучения из всех источников на душу населения в США (0,54 мЗв из 3,6 мЗв). В 2006 г. на медицинскую визуализацию приходилось 48% облучения на душу населения (3 мЗв из 6,25 мЗв), при этом на КТ, ядерную медицину и интервенционную рентгеноскопию приходилось 24%, 12% и 7% соответственно.(Национальный совет по радиационной защите и измерениям, Отчет NCRP No. 160 , март 2009 г., стр. 242-243.)
9 Национальный совет по радиационной защите и измерениям, Отчет NCRP № 160 , март 2009 г., стр. 142-146.
10 Бреннер Д. Д. и Холл Э. Дж., Компьютерная томография: возрастающий источник радиационного воздействия, Медицинский журнал Новой Англии , ноябрь 2007 г., том. 357, No. 22, pp. 2277-2284.
11 Беррингтон де Гонсалес А. и др., «Прогнозируемые риски рака по результатам компьютерного томографического сканирования, проведенного в США в 2007 г.», Архив внутренней медицины , декабрь 2009 г., том. 169, No. 22, pp. 2071-2077.
12 Смит-Биндман и др., «Доза излучения, связанная с обычными компьютерными томографическими исследованиями и связанный с этим риск рака в течение всей жизни», Архив внутренней медицины , декабрь 2009 г., том. 169, No. 22, pp. 2078-2086.
13 Пресс-релиз FDA, «FDA делает промежуточные рекомендации по устранению опасений чрезмерного радиационного воздействия во время КТ-перфузионной визуализации», 7 декабря 2009 г. 14 Смит-Биндман и др., Декабрь 2009 г.
15 Референсные диагностические уровни были введены в Великобритании (NRPB / RCR, «Снижение дозы для пациентов в диагностической радиологии», Doc. NRPB , 1990, Vol. 1, No. 3, pp. 1-46). включены в рекомендации Международной комиссии по радиологической защите ( Радиологическая защита и безопасность в медицине, , Публикация МКРЗ 73 , Анналы МКРЗ , 1996 г., том 26, № 2). В соответствии с Директивой Европейского Совета 97/43 / Евратом ( Официальный вестник Европейских сообществ , 9 июля 1997 г., No.L 180, pp. 22-27), диагностические референтные уровни широко приняты в Европе. См., Например, следующие ссылки и цитаты в нем: Gray JE, et al., «Справочные значения для диагностической радиологии: применение и влияние», Radiology , май 2005 г., Vol. 235, № 2, стр. 354-358; Рода А.Р., Лопес М.С. и Фаусто А.М., «Контрольные уровни диагностики в компьютерной томографии в IPOCFG, EPE», Всемирный конгресс по медицинской физике и биомедицинской инженерии, 7–12 сентября 2009 г., Мюнхен, Германия, IFMBE Proceedings , Vol.25 / III, Олаф Дёссель и Вольфганг К. Шлегель (ред.), Springer 2009, стр. 26-29; Treier R и др., «Диагностические контрольные уровни в компьютерной томографии в Швейцарии», , там же, ., Стр. 146-149.
16 Контрольные уровни диагностики, рекомендованные ACR. Референсные значения, рекомендованные AAPM, опубликованы в Gray JE, et al., «Справочные значения для диагностической радиологии: применение и влияние», Радиология, май 2005 г., Vol. 235, № 2, с. 354-358. Информация об усилиях NCRP по разработке диагностических референсных уровней.
17 См., Например, Miller DL, et al., «Дозы излучения в процедурах интервенционной радиологии: исследование RAD-IR, часть II: доза на кожу», , Журнал интервенционной сосудистой радиологии, , август 2003 г., том. 14, No. 8, pp. 977-990; и Маркс М.В., «Доза радиации в интервенционном радиологическом исследовании: знание несет ответственность», , там же, ., стр. 947-951.
18 Дополнительную информацию о кампаниях Image Gently и Step Lightly можно найти в Интернете по адресу https: // www.imagegently.org/.
19 Критерии соответствия ACR® доступны в Интернете по адресу https://www.acr.org/Clinical-Resources/ACR-Appgotiness-Criteria/About-the-ACR-AC.
20 Закон об улучшении медицинской помощи для пациентов и поставщиков медицинских услуг от 2008 г. P. L. 110-275. 15 июля 2008 г. 122 Стат. 2494.
21 42 C.F.R. 414,68.
22 42 C.F.R. 482.
23 Можно создать единый национальный регистр доз для нескольких типов процедур визуализации или отдельные регистры для различных типов процедур.Хотя термин «реестр» используется здесь в единственном числе, FDA поддерживает любой подход.
24 ACR работает над созданием реестра индекса дозы для различных методов визуализации, чтобы можно было проводить сравнения между участвующими учреждениями. ACR недавно провела пилотный проект регистрации индекса дозы для КТ. Дополнительная информация доступна в Интернете по адресу https://www.acr.org/Practice-Management-Quality-Informatics/Imaging-3/Case-Studies/Quality-and-Safety/Big-Data-Registry.
25 Raff GL, Chinnaiyan KM, Share DA, et al., «Доза облучения от компьютерной томографии сердца до и после внедрения методов снижения дозы облучения», журнал Американской медицинской ассоциации , июнь 2009 г., том. 301, No. 22, pp. 2340-2348.
26 Новая карта записи медицинских изображений обновлена и в настоящее время доступна по адресу:
Карта медицинской карты пациента (стандартный размер)
Карта медицинской карты пациента (размер бумажника)
Управление изображениями в лучевой терапии: методы и применение
В современной лучевой терапии акцент на уменьшении объема облучения высокими дозами лучевой терапии, повышении точности лечения, а также снижении связанной с радиацией токсичности нормальных тканей увеличился, и, таким образом, больше Важное значение придается точной проверке и коррекции положения до проведения лучевой терапии.В настоящее время разработано несколько методов, которые безупречно достигают этих целей, хотя все они имеют свои ограничения. Не существует единого доступного метода, который устраняет неопределенности, связанные с обработкой, без значительного увеличения стоимости. Однако проведение «высокоточной лучевой терапии» без периодического контроля изображений принесет больше вреда, чем обработка больших объемов для компенсации ошибок настройки. В настоящем обзоре мы обсуждаем концепцию управления изображением в лучевой терапии, доступные в настоящее время методы, а также ожидаемые преимущества и недостатки.
1. Введение
Радиотерапия всегда требовала входных данных от визуализации для планирования и выполнения лечения, когда цель лечения не расположена на поверхности, а осмотр и визуальное подтверждение невозможны. Традиционные методы лучевой терапии включают использование анатомических ориентиров на поверхности, а также радиологическую корреляцию с двумерной визуализацией в виде пленок порта или рентгеноскопической визуализации.
В целом визуализация играет две основные роли в лучевой терапии: (a) Сложные методы визуализации, такие как сканирование компьютерной томографии с контрастным усилением (CECT), магнитно-резонансная томография (MRI), сканирование позитронно-эмиссионной томографии (PET) и ангиография для получения трехмерных изображений. (3D) структурная и биологическая информация, которая используется для точного определения цели и, таким образом, обеспечивает точное и точное планирование лечения с помощью фигурных лучей в изоцентрической или неизоцентрической геометрии.(b) Методы визуализации «в помещении» (планарные, объемные, видео или ультразвуковые) позволяют периодически получать информацию о положении и перемещении цели (в рамках одного сеанса или между последовательными сеансами), сравнивать ее с эталонной визуализацией и давать обратную связь. чтобы исправить настройку пациента и оптимизировать локализацию цели. Они также могут предоставить обратную связь, которая может помочь адаптировать последующие сеансы лечения в соответствии с ответом опухоли.
Более конкретно, современная лучевая терапия рассматривает последнее применение с визуализацией «в помещении» как «лучевую терапию под визуальным контролем» (IGRT).
Современные методы лучевой терапии с дистанционным облучением, такие как лучевая терапия с модуляцией интенсивности (IMRT), терапия с объемной модуляцией дуги (VMAT), стереотаксическая радиохирургия (SRS) или стереотаксическая лучевая терапия (SRT), помогли снизить запас безопасности вокруг целевых объемов, что позволило более низкие нормальные тканевые дозы без ущерба для доставки опухолевидных доз. Однако существует большая неопределенность в точном определении положения мишеней во время проведения фракционированной лучевой терапии, как во время данной фракции, так и между последовательными фракциями.Цели, которые могут двигаться во время лечения из-за дыхательных или перистальтических движений или пульсации сердца, создают еще большую проблему. Следовательно, существует необходимость в разработке и реализации стратегий для измерения, мониторинга и исправления этих неопределенностей. Это привело к развитию различных технологий визуализации в помещении, которые позволяют оценивать и исправлять ошибки настройки, анатомические изменения, связанные с потерей или деформацией веса, или движения внутренних органов, связанные с дыханием, перистальтикой или наполнением прямой кишки / мочевого пузыря.
Планирование лечения брахитерапией также включает ортогональную рентгенографию и рентгеноскопию для направления установки катетера / аппликатора для брахитерапии, объемную визуализацию с КТ или МРТ для идентификации и реконструкции аппликатора, а также оптимизацию плана в трех измерениях на основе изображений. Распределение изодозы анализируется и оптимизируется для визуализации распределения дозы на цель, а также на критические структуры. Это повышает эффективность и безопасность лечения.
2. Концепция IGRT
Несмотря на техническую сложность, хирургические процедуры позволяют оперирующим хирургам непосредственно визуализировать и обрабатывать свои цели, что устраняет двусмысленность в идентификации и надлежащем управлении.Радиотерапия, несмотря на то, что является местной терапией, направленной на достижение аналогичных целей, по своей сути несет в себе недостаток, заключающийся в том, что при использовании традиционных методов лечения делается большое количество допущений. Набор данных трехмерного изображения, полученный при моделировании, представляет собой снимок опухоли, ее отношения к нормальным структурам, а также форму и положение пациента в один момент времени, и именно эта модель используется для разработки плана и расчета дозы. На этапе планирования используется множество предположений, основанных на предыдущем опыте и литературе, в отношении границ клинического целевого объема (CTV) для определения микроскопического распределения вокруг опухоли и планирования границ целевого объема (PTV) для включения ожидаемого диапазона внутренних движение органа и ошибки настройки.Затем лечение проводится с верой в то, что все эти предположения будут верны для любого данного пациента во время ежедневных сеансов лечения, главным из которых является то, что анатомия пациента и опухоли, а также их положение относительно устройств позиционирования не изменились со времени моделирование. Однако предположение о том, что доза, рассчитанная по набору данных компьютерной томографии в системе планирования, соответствует дозе, полученной через каждую фракцию или через весь курс лучевой терапии, является серьезной ошибкой.Кроме того, внутренние органы и цели движутся вместе с дыханием и перистальтикой, и планирование лучевой терапии в наборе данных статического изображения не может учесть ошибки, связанные с этим движением. Чтобы гарантировать, что все эти допущения не ставят под угрозу доставку дозы к CTV, принимаются более широкие пределы PTV. Это приводит к включению большого объема нормальных тканей в облучаемый объем. IGRT дает метод регулярного сбора этой информации во время курса лечения в виде серийных «снимков» и является средством проверки точной и точной доставки излучения.Проще говоря, процесс IGRT гарантирует, что проводимое лечение соответствует предполагаемому лечению в точном нацеливании на опухоль при минимизации «побочного ущерба». Изменения суммарной доставленной дозы и их влияние на борьбу с заболеванием, а также на токсичность можно свести к минимуму путем использования соответствующих устройств локализации и границ PTV. Иногда может потребоваться перепланировка, если наблюдаются грубые отклонения, превышающие заданные допуски [1–3].
IGRT позволяет оценить геометрическую точность «модели пациента» во время лечения.Он обеспечивает метод, с помощью которого определяются отклонения анатомии от первоначального плана, и эта информация используется для обновления дозиметрических допущений. Стратегии коррекции могут включать в себя ежедневное изменение положения пациента для регистрации положения пациента в соответствии с базовым планом или пересчет лечения в реальном времени, чтобы отразить представление пациента во время данной фракции. Эта философия переоценки лечения и учета различий между реальной анатомией пациента в конкретный день и моментальным снимком запланированного лечения известна как адаптивная лучевая терапия [4].Конечная цель — переоценить и в определенных ситуациях переопределить ежедневное позиционирование для лечения, чтобы оно оставалось в том же русле, что и предполагаемое лечение. Будущие применения могут включать титрование дозы для максимального эффекта или смягчения побочных эффектов.
3. Ошибки и поля
Ошибка в проведении лучевой терапии определяется как любое отклонение от запланированного или запланированного лечения. Большая степень неопределенности присуща практике лучевой терапии и может быть в форме механических неопределенностей, связанных с параметрами лечебного блока, такими как движение кушетки и гентри, неуверенность пациента, связанная с возможностью комфортно лежать в определенном положении и сотрудничать во время лечения. геометрические неопределенности, связанные с положением и движением цели, и дозиметрические неопределенности.IGRT имеет дело с геометрическими неопределенностями, которые могут быть как внутрифракционными, так и межфракционными [5, 6].
Как межфракционные, так и внутрифракционные неопределенности могут быть результатом комбинации систематических и случайных ошибок.
Систематическая ошибка — это, по сути, ошибка подготовки к лечению, которая вводится в цепочку в процессе позиционирования, моделирования или определения цели. Эта ошибка, если ее не исправить, повлияет на все фракции обработки одинаково. С другой стороны, случайная ошибка — это ошибка выполнения лечения, она непредсказуема и зависит от каждой доли.Систематические ошибки смещают все распределение дозы от CTV, в то время как случайные ошибки размывают это распределение вокруг CTV. Из этих двух систематическая ошибка более опасна, поскольку она будет иметь гораздо большее влияние на точность лечения и, следовательно, терапевтическое соотношение.
Поля добавляются к CTV, чтобы учесть эти ошибки. Эти поля представляют собой геометрические расширения вокруг CTV и могут быть неоднородными во всех измерениях в зависимости от ожидаемых ошибок. Эти запасы обеспечивают достижение целей дозиметрического планирования, несмотря на различия во фракциях и между ними.ICRU 62 определяет распространение PTV вокруг CTV как совокупность двух факторов — внутреннего движения цели (внутренний запас) и вариаций настройки (запас настройки) [7]. В зависимости от наблюдаемых систематических и случайных ошибок в данной настройке для конкретного участка лечения в литературе существует множество рецептов для расчета пределов PTV [8, 9]. Для повышения терапевтического соотношения может применяться множество стратегий коррекции для уменьшения этих границ и может включать в себя оперативную или автономную коррекцию межфракционных ошибок или коррекцию внутрифракционного движения в реальном времени.Отслеживание и коррекция движения органа помогает уменьшить внутренний запас, в то время как повышенная точность позиционирования сокращает пределы настройки, тем самым уменьшая необходимый запас PTV.
4. Офлайн-коррекция и онлайн-коррекция
Офлайн- и онлайн-стратегии коррекции IGRT относятся к тому, находится ли пациент на лечебной кушетке во время проверки, и будет ли корректировка применяться к тому же или к последующим сеансам.
В автономной стратегии изображения получают до обработки и сопоставляют с эталонным изображением в более поздний момент времени.Эта стратегия направлена на определение индивидуальной систематической ошибки настройки и, таким образом, ее уменьшение. В сочетании с данными настройки других пациентов, проходящих лечение по тому же протоколу, он помогает определить стандартную ошибку населения для этого лечения в этом учреждении. К широко используемым протоколам автономной коррекции относятся протоколы «Уровень действия сжатия» и «Уровень без действия» [10, 11]. Маржа PTV в учреждении зависит от этих определений индивидуальных и популяционных систематических ошибок.
С другой стороны, онлайн-стратегия предполагает получение изображений, их проверку и исправление перед дневным лечением.Он направлен на уменьшение как случайных, так и систематических ошибок. Место лечения и ожидаемая величина ошибки могут определять частоту онлайн-визуализации. Участки, где ожидаются большие ежедневные сдвиги (брюшная полость, таз и грудная клетка) или где даже небольшие сдвиги изменят распределение дозы в смежных критических структурах (параспинальные опухоли, внутричерепные опухоли в непосредственной близости от оптических структур), лучше всего контролировать с помощью ежедневной визуализации. Наш опыт онлайн-коррекции показал, что максимальное количество ошибок наблюдается в грудной клетке, за которой следуют брюшная полость и таз.Минимальные ошибки наблюдались в области головы и шеи [12]. Кроме того, такие виды лечения, как VMAT и SBRT, могут привести к значительным изменениям в распределении доз и, следовательно, требуют ежедневной онлайн-проверки. Для ежедневной онлайн-коррекции систематические и случайные ошибки могут быть рассчитаны на основе сопоставленных данных. Визуализация после лечения необходима для количественной оценки как внутрифракционного движения, так и остаточных ошибок. При оценке для популяции пациентов эти данные могут помочь проверить предел PTV для этого протокола лечения.Фактически, использование ежедневной онлайн-визуализации с коррекциями в сочетании с использованием автоматической кушетки с 6 степенями свободы устранило необходимость инвазивных рамок для лечения SRS [13].
5. Технологические решения IGRT
В зависимости от используемых методов визуализации системы IGRT в широком смысле можно разделить на системы на основе излучения и системы без излучения [14, 15].
5.1. Системы без излучения [16–22]
В них могут использоваться ультразвуковые системы, системы на основе камер, системы электромагнитного слежения и МРТ, интегрированные в процедурный кабинет.
5.1.1. Системы на основе ультразвука
Эти системы (например, BAT, SonArray, Clarity) получают трехмерные изображения, которые помогают выровнять цели для исправления межфракционных ошибок. Геометрическая точность составляет 3–5 мм, а главное преимущество — отсутствие ионизирующего излучения. Области общего применения включают лучевую терапию простаты, легких и груди.
5.1.2. Камерные (инфракрасные) или оптические системы слежения
Эти системы идентифицируют положения опорных точек настройки пациента по сравнению с их положением в системе координат планирования КТ, что помогает в вычислении смещения лечебной кушетки для выравнивания изоцентра лечения с изоцентром плана.Оптическое слежение также может использоваться для внутрифракционного мониторинга положения либо для стробирования (доставка лечения только в определенном положении цели), либо для изменения положения для коррекции. Такие инструменты, как AlignRT, визуализируют пациента напрямую и отслеживают поверхность кожи, чтобы в режиме реального времени получать информацию о необходимых коррекциях. Эти системы нашли применение при лечении рака простаты и груди, а также для вентиляции дыхательных путей с использованием внешних суррогатов. Геометрическая точность составляет 1-2 мм, но применение ограничено только ситуациями, когда внешняя поверхность может выступать в качестве надежного заменителя внутреннего положения или движения.
5.1.3. Системы электромагнитного слежения
В этих системах (например, Calypso) используются электромагнитные транспондеры (маяки), встроенные в опухоль, и движение этих маяков можно отслеживать в реальном времени с помощью системы детекторной матрицы. Маяки необходимо устанавливать с помощью минимально инвазивной процедуры, их присутствие может привести к появлению артефактов на МРТ-изображениях, а также существуют ограничения по размеру пациента. Калипсо имеет геометрическую точность <2 мм, но в настоящее время его использование ограничено лучевой терапией простаты.
5.1.4. IGRT с контролем МРТ
Эти системы (например, ViewRay) помогают в реальном времени оценивать внутреннюю анатомию и движение мягких тканей с использованием непрерывной визуализации мягких тканей и позволяют проводить внутрифракционные коррекции. Геометрическая точность системы 1-2 мм. Однако МРТ имеет определенные недостатки, такие как артефакты движения, искажения из-за неоднородных магнитных полей, и не может выполняться для пациентов с кардиостимуляторами или металлическими имплантатами. Все эти ограничения диагностической МРТ применимы и к этой системе IGRT.Существует широкий потенциал применения в лечении простаты, печени и головного мозга, а также в брахитерапии.
5.2. Системы на основе излучения
К ним относятся статическое отслеживание, а также отслеживание в реальном времени с использованием киловольтных (КВ), мегавольтных (МВ) или гибридных методов.
5.2.1. Электронные портальные устройства формирования изображений (EPID)
EPID были разработаны в качестве замены пленочной дозиметрии для проверки в полевых условиях и основаны на плоскопанельных тепловизорах с активной матрицей непрямого обнаружения (AMFPI).Они предлагаются в качестве стандартного оборудования почти всеми поставщиками линейных ускорителей (LINAC) в качестве инструментов как для полевой проверки, так и для обеспечения качества (QA). Получение изображения 2D, с геометрической точностью 2 мм. Костные ориентиры на плоских изображениях используются в качестве суррогатов для определения вариаций положения, соответствующих цифровым реконструированным рентгенограммам (DRR), разработанным на основе набора данных КТ для планирования (рисунок 1). Различные системы могут использовать для визуализации рентгеновские лучи KV или MV, при этом контраст изображения выше, чем у изображений KV, в то время как металлические имплантаты (зубные протезы, протезы бедра) меньше искажают изображения MV.Системы EPID не способны обнаруживать или количественно определять ротации. Средняя доза на изображение составляет 1–3 мГр для систем КВ, а для систем среднего напряжения — 30–70 мГр [23–25].
5.2.2. КТ с коническим лучом (КЛКТ), KV или MV
Эти системы состоят из выдвижной рентгеновской трубки и детекторов из аморфного кремния, установленных либо ортогонально (Elekta Synergy, Varian OBI), либо вдоль оси лечебного луча (Siemens Artiste). Они имеют возможность 2D, рентгеноскопии и КЛКТ. Другая система (Vero, BrainLAB) состоит из рентгеновской головки на карданном шарнире, установленной на уплотнительном кольце, с двумя рентгеновскими трубками KV, двумя плоскими детекторами и EPID.Уплотнительное кольцо можно вращать на 360 градусов вокруг изоцентра и на 60 градусов вокруг своей вертикальной оси. Геометрическая точность составляет 1 мм или меньше с возможностью согласования 2D и 3D с DRR или объемными рентгеновскими изображениями, созданными на основе наборов данных КТ планирования. Сканирование осуществляется путем непрерывного частичного или полного вращения гентри вокруг кушетки с получением «среднего» положения органов при дыхательном движении. Можно отслеживать как изменения межфракционного взаимодействия, так и анатомические изменения, связанные с изменениями веса или наполнением органов (мочевой пузырь, прямая кишка) (рис. 2).Повторное сканирование в конце лечения может дать оценку внутрифракционных изменений. Для опухолей, различимых отдельно от окружающей нормальной ткани, можно также отслеживать реакцию на лечение, и эти сканирования могут использоваться для пересчета дозы или адаптации плана лечения после необходимой обработки изображения. KV CT дает лучшее контрастное разрешение по сравнению с MV CT, но может быть ограничено артефактами от протезов и разбросом от громоздкой анатомии пациента. Средняя доза на изображение составляет 30–50 мГр [26–29].
5.2.3. Вентиляторный луч KV CT (CT-on-Rails)
Эта система имеет компьютерный томограф в комнате и гентри, которые перемещаются через кушетку / пациента, которую можно поворачивать в сторону сканера или гентри для получения изображений и лечения соответственно . Трехмерные изображения получают с пациентом, иммобилизованным на кушетке, отличием от диагностической КТ является больший размер отверстия (диаметр> 80 см) для размещения громоздких иммобилизационных устройств и мультисрезовый детектор. Точность и применение аналогичны КЛКТ со средней дозой 10–50 мГр на изображение [30].
5.2.4. Веерный луч МВ КТ (Томотерапия Hi ART II)
Включает бортовую систему визуализации для получения КТ МВ пациента в положении лечения. Один и тот же LINAC используется для генерации луча обработки (6 МВ) и луча изображения (3,5 МВ). Ксеноновый детектор, расположенный на гентри напротив LINAC, собирает данные на выходе для генерации изображений КТ МВ. Доза облучения пациента от изображения меняется в зависимости от настройки звука и обычно составляет 10–30 мГр за сканирование [31].
5.2.5. Гибридные системы для отслеживания 4D в реальном времени
2D КВ стереоскопическое изображение (CyberKnife) .Роботизированная радиохирургическая система Accuray CyberKnife состоит из компактного LINAC, установленного на руке промышленного робота-манипулятора, который направляет лучи излучения на желаемую цель на основе входных сигналов от двух систем ортогональной рентгеновской визуализации, установленных на потолке комнаты с плоскими напольными детекторами на каждой из них. сторона кушетки, интегрированная для обеспечения визуального сопровождения процесса лечения. Изображения получаются на протяжении всего сеанса лечения с периодическими интервалами от 5 до 90 секунд, а движения кушетки и головы робота управляются автоматически.В зависимости от участка лечения можно использовать несколько методов отслеживания (рис. 3). Опухоли черепа, основания черепа или головного мозга можно лечить с помощью отслеживания черепа 6D, паравертебральные опухоли, движение которых аналогично движению позвоночника, можно лечить с помощью отслеживания позвоночника X-Sight, а опухоли легких, окруженные нормальной паренхимой легких, можно отслеживать с помощью X- Отслеживание легкого прицела. Отслеживание легких может использовать автоматическое создание внутреннего целевого объема в зависимости от видимости опухоли через обе, одну или ни одну из рентгеновских систем визуализации в позиции лечения.Для всех других опухолей (например, простаты, печени, шейных узлов, новообразований в брюшной полости и т. Д.) Может потребоваться размещение внутренних суррогатов или реперных маркеров внутри опухоли или в непосредственном контакте с ней, а движение опухоли отслеживается и корректируется посредством мониторинга. исходное положение, включая смещения, вращения и деформации. Дыхательное движение также отслеживается и учитывается при корректировке положения и движения цели с помощью синхронной модели, созданной в реальном времени. В системе также есть кушетка с 6 степенями свободы для корректировки позиционных изменений.Лечение может быть ограничено положением и размером пациента, а также нельзя использовать задние лечебные пучки. Если для отслеживания необходимы реперные маркеры, может потребоваться полуинвазивная процедура. Эта система может использоваться как для краниальной (безрамной), так и для экстракраниальной радиохирургии или СРТ [32, 33].
Система отслеживания опухолей в реальном времени (RTRT) . Эта система предназначена для отслеживания опухолей в реальном времени путем визуализации имплантированных реперных точек и использования этой информации для стробирования. Он состоит из четырех систем рентгеновских камер, установленных на полу, усилителя изображения, установленного на потолке, и генератора рентгеновского излучения высокого напряжения.LINAC запускается для облучения опухоли только тогда, когда маркер находится в пределах заданного допуска от его запланированных координат относительно изоцентра [34, 35].
VERO . Эта система имеет две рентгеновские трубки и соответствующие плоскопанельные детекторы и использует комбинацию начального движения кушетки и пары рентгеновских снимков для выравнивания пациента. Кушетка может выполнять трехмерное выравнивание для начальной грубой настройки, а затем встроенная подсистема визуализации помогает выполнить точную настройку. Пара рентгеновских снимков делается и регистрируется с помощью предыдущих DRR с использованием костных ориентиров для оценки поступательных и вращательных сдвигов.Система также может компенсировать движение органов [36].
5.2.6. Комбинированные системы выравнивания: оптическая визуализация и ортогональная 2D-визуализация KV
ExacTrac X-Ray 6-D стереотаксическая система IGRT . Он использует комбинацию оптического позиционирования и рентгенографической визуализации KV для онлайн-коррекции позиционирования. Есть две основные подсистемы: инфракрасная система для первоначальной настройки пациента и точного управления движением кушетки с помощью роботизированной кушетки и рентгенографическая система рентгеновской визуализации KV для проверки положения и корректировки на основе внутренней анатомии или имплантированных маркеров.Инфракрасная система также может использоваться для респираторного мониторинга и передачи сигналов в LINAC для отслеживания луча и стробирования. Novalis Tx сочетает эту систему с дополнительной бортовой системой визуализации (МВ, КВ рентгеновские лучи и КВ КЛКТ) на многофотонном / электронном пучке LINAC [37, 38].
6. Руководящие принципы для медицинского персонала и их внедрение
Американский колледж радиологии (ACR) и Американское общество радиационной онкологии (ASTRO) совместно разработали руководящие принципы для IGRT, определяющие квалификацию и обязанности персонала, включая онкологов-радиологов, медицинских физиков, дозиметристов и лучевые терапевты, стандарты обеспечения качества, клиническое внедрение и предлагаемая документация.Аналогичные руководящие принципы были также предложены европейскими агентствами [39–41]. Краткое изложение ключевых моментов приводится ниже.
6.1. Квалификация и обязанности
Квалификация . Перед выполнением любых стереотаксических процедур соответствующий персонал должен пройти соответствующую сертификацию и пройти специальную подготовку по IGRT.
Обязанности
Радиолог-онколог . (i) Проведение лечения конкретного заболевания, определение стадий, оценка сопутствующих заболеваний и предшествующего лечения, изучение всех доступных методов лечения, включая обсуждение плюсов и минусов IGRT, лечения и последующего наблюдения.
(ii) Определение наиболее подходящего метода позиционирования пациента, рекомендация соответствующего подхода к управлению движением органов, наблюдение за симуляцией с уделением особого внимания позиционированию, иммобилизации и надлежащему управлению движением, определение и разграничение целевых объемов и соответствующих нормальных критических структур использование доступных методов визуализации, информирование об ожидаемых целях и ограничениях и сотрудничество с физиком в итеративном процессе разработки плана для достижения желаемых целей, надзор за проведением лечения и определение приемлемых повседневных вариантов настройки, а также участие в QA. процесс и последующее согласование.
Медицинский физик . (i) Приемочные испытания и ввод в эксплуатацию, обеспечивающие механическую, программную и геометрическую точность и точность, а также проверку качества изображения и документацию в данной системе IGRT.
(ii) Внедрение и управление программой обеспечения качества.
(iii) Разработка и внедрение стандартных операционных процедур (СОП) для использования IGRT в сотрудничестве с онкологом-радиологом.
Дозиметрист . (i) Обозначение нормальной структуры под руководством онколога-радиолога.
(ii) Управление данными объемных изображений пациента (КТ и другие объединенные наборы данных) в системе планирования лучевой терапии (RTP).
(iii) Составление плана лечения под руководством онколога и физика.
(iv) Создание всей технической документации для реализации плана IGRT.
(v) Помощь в проверке лечения.
Лучевой терапевт . (i) Понимание и надлежащее использование систем иммобилизации / репозиции.
(ii) Выполнение моделирования и генерации данных визуализации для планирования, выполнения плана лечения, получения изображений для периодической проверки под наблюдением и периодической оценки стабильности и воспроизводимости системы иммобилизации / репозиции, а также немедленного сообщения о несоответствиях.
6.2. Реализация IGRT
Опорные маркеры . Они служат суррогатами мишеней из мягких тканей, когда их трудно визуализировать, и их расположение не может быть связано с анатомией кости.Их можно отслеживать в реальном времени для получения трехмерных координат цели для последующих корректировок.
Движущиеся цели и определение границ . При определении PTV следует учитывать внутрифракционное движение мишени или межфракционное смещение, деформацию или изменение мишеней и других тканей. Соответствующие методы управления движением следует выбирать в зависимости от имеющегося опыта, степени и типа движения. Этот процесс начинается во время симуляции и продолжается до конца терапии.
Расположение пациента . Крайне важно обеспечить точность положения пациента и его воспроизводимость при фракционированном лечении относительно выбранного устройства IGRT, а также лечебного блока.
Получение изображений . Система IGRT должна быть откалибрована для обеспечения высокого качества изображения с учетом однородности толщины срезов, контрастности изображения, пространственного разрешения, выравнивания изоцентра между системами визуализации и планирования и доставки лечения, точности программного обеспечения, используемого для идентификации, и коррекции несовпадений кушетки.Соответствующие процедуры обеспечения качества должны гарантировать надежность и воспроизводимость всего процесса.
Проверка лечения . Осмотр изображения онкологом-радиологом сначала необходимо, а затем периодически, чтобы гарантировать точность и воспроизводимость лечения. Каждое отделение должно определить свой собственный порог изменения положения кушетки, который потребует пересмотра или изменения настроек до начала лечения.
Контроль качества и документация .Следует вести документацию по всем необходимым процедурам обеспечения качества в ходе моделирования, обработки и периодической проверки. Это поможет определить пороговые значения для действий в отделе, а также послужит руководством для модификации задействованных процессов после анализа результатов.
7. IGRT: клинические преимущества
Использование процесса IGRT улучшило нашу осведомленность и понимание ежедневных меж- и внутрифракционных вариаций настройки и движения. Отслеживание в реальном времени помогло количественно оценить вариации движений опухолей легких и печени у разных пациентов и внутри пациентов, связанные с дыханием, и сложность такого движения стала более ясной.Теперь мы понимаем, что даже когда задержки дыхания повторяются, относительное положение мягких тканей и структур скелета может меняться, что делает использование костных ориентиров бесполезным для таких усилий. Изменения положения простаты (перемещение, вращение и форма) были количественно оценены, и мы можем лучше исправить эти ошибки, а также адаптировать границы PTV к этим результатам, что позволяет более точно нацеливать. Понимание различных методов IGRT, их применимости, ограничений и дополнительных радиационных опасностей помогает онкологу-радиологу принять обоснованное решение о методе, наиболее подходящем для конкретной клинической ситуации для получения максимальной пользы от лучевой терапии.Изменения положения околоушной железы относительно опухоли в случаях головы и шеи, изменение контура тела из-за потери веса, серомы или скопления жидкости в организме, изменение положения простаты относительно наполнения мочевого пузыря или прямой кишки и влияние кишечного газа, уменьшение размера опухоли во время лечения и изменения положения позвоночника во время лучевой терапии позвоночника или головы и шеи — это ситуации, которые никогда даже не считались важными в эпоху до IGRT, и их соответствующие роли и решения разрабатываются, поскольку мы понимаем их роль во время лечения.При большей геометрической точности объем облученной здоровой нормальной ткани может быть значительно уменьшен с уменьшением риска токсичности. Адаптация к уменьшению объема опухоли может привести к дополнительному снижению токсичности нормальных тканей.
Результаты текущих и будущих испытаний, мы надеемся, продемонстрируют чистый выигрыш в терапевтическом соотношении от применения технологий IGRT, и ответственность за демонстрацию преимуществ этих потенциально дорогостоящих подходов лежит на сообществе радиационной онкологии.
IGRT, скорее всего, принесет пользу в клинических ситуациях, когда опухоль находится в непосредственной близости от чувствительных здоровых тканей, когда дозы, необходимые для контроля заболевания, превышают допустимые уровни соседних нормальных тканей или когда движение большого органа и ошибки настройки могут привести к серьезным последствиям позиционные ошибки. Теоретически все пациенты, получавшие конформную лучевую терапию, IMRT и SBRT, должны получить пользу от IGRT. Цели в области грудной клетки и верхней части живота со значительным респираторным движением, пациентами с ожирением, раком головы и шеи, параспинальной и забрюшинной саркомой и раком простаты — это ситуации, которые, как ожидается, принесут максимальную пользу при наличии определенного клинического опыта.Клинические ситуации, когда даже низкодозовое облучение обеспечивает превосходный местный контроль, паллиативная лучевая терапия проводится с использованием больших полей и поверхностные опухоли, которые поддаются прямому визуальному осмотру, вероятно, принесут наименьшую пользу от IGRT.
8. Проблемы, связанные с IGRT
Ограниченное наличие опытного обученного персонала является серьезным препятствием для широкого применения метода, несмотря на его очевидные преимущества даже при простейших подходах. Другие факторы, которые необходимо учитывать, включают контроль качества, алгоритмы, которые определяют решения, следует ли изменить план или продолжить с первоначальным планом, а также необходимость коммерческой разработки программного обеспечения, а также оборудования для соответствия клиническим потребностям и требованиям.Другой серьезной проблемой, связанной с частой визуализацией во время лечения, является доза облучения нормальных тканей. Хотя дозы от IGRT кажутся незначительными, только долгосрочное наблюдение определит любой потенциальный риск вторичных злокачественных новообразований от воздействия низких доз. Таким образом, продолжаются дискуссии о необходимой частоте проверочной визуализации, особенно при использовании ионизирующего излучения. Недавние разработки MR-LINAC направлены на решение этих проблем, одновременно позволяя получать изображения для подтверждения лечения.Другая проблема связана с безопасностью лечения, поскольку технологии, доступные в клинике, требуют интеграции оборудования и программного обеспечения от разных поставщиков. Клиническому использованию любой системы должны предшествовать надлежащие приемочные испытания, ввод в эксплуатацию и рутинный контроль качества, используемый для обеспечения точной регулярной работы. Обучение всех пользователей (онкологов, физиков и технологов) безопасному использованию и клинической применимости является обязательным, наряду со знанием дополнительной дозы и возможных рисков, связанных с использованием.Ни одна технология не является идеальной для каждого сценария, и ни одно учреждение не может объединить все или большинство технологий в одном месте. Только время покажет, какой из этих методов получит более широкую популярность и признание, исходя из клинической значимости и простоты использования.
9. Клиническое применение: настоящее и будущее
Использование систем IGRT необходимо для лечения любого участка, где ожидаются отклонения в настройке и движение органов. Дополнительным преимуществом является ежедневный мониторинг реакции на лечение, изменений веса и наполнения органов.С улучшенной точностью систем планирования, использованием SRS или SRT и режимов гипофракционирования с высокими дозами, вероятность небольших отклонений, ведущих к значительным ошибкам в проведении лечения, намного выше, и использование IGRT является гораздо более важным в таких ситуациях. Интеграция LINAC с визуализацией мягких тканей на основе МРТ и биологической визуализацией на основе ПЭТ может помочь еще больше повысить точность наведения в будущем [42, 43]. Однако необходимо обеспечить надлежащее обучение персонала и обеспечение качества на всех этапах для оптимального использования такой технологии и ее интеграции в повседневное использование.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов относительно публикации данной статьи.
Принципы КТ: доза излучения и качество изображения
Эта статья, вторая из серии статей для непрерывного образования, посвященных принципам КТ, фокусируется сначала на дозиметрии КТ и дозе излучения, а затем на качестве изображения КТ.
СТ ДОЗИМЕТРИЯ И ДОЗА ИЗЛУЧЕНИЯ
До того, как компьютерная томография стала использоваться, планарная рентгенография и рентгеноскопия включали все неядерные методы использования ионизирующего излучения для визуализации в медицине.В этих типах обследований доза облучения пациента максимальна там, где рентгеновский луч попадает на поверхность кожи. Следовательно, было разумно использовать радиационное воздействие на входную поверхность (называемое входным воздействием на кожу) в качестве индикатора радиационного риска при сравнении различных методов, рецепторов и рентгеновских аппаратов. Расчет воздействия на кожу на входе выполняется просто, используя измерения воздействия ионизационной камеры в воздухе при нескольких киловольтах в рентгеновской трубке, охватывающих клинический диапазон.Такие измерения обычно выражаются как экспозиция на миллиампер-секунду (мР / мАс, или, точнее, сегодня, мГр керма воздуха / мАс).
Во время сканирования КТ-среза, с другой стороны, рентгеновский луч входит со всех сторон в какой-то момент во время сканирования. Больше не ясно, где (на поверхности или внутри пациента) происходит максимальная доза, равно как и вычисление дозы в любой точке пациента или на нем не является простым. Например, рассмотрим 2 точки, A и B, которые находятся, соответственно, рядом с передней поверхностью и в центре цилиндрического пациента.Во время вращения на 360 ° точка A получает много излучения, когда рентгеновская трубка находится над пациентом (передняя входная поверхность). Однако точка A также получает некоторое (хотя и меньшее) излучение, когда трубка находится в каждой точке во время своего вращения, даже когда трубка находится на противоположной стороне от пациента. Для каждого местоположения трубки различное количество излучения достигает точки A, в зависимости от глубины A (то есть, сколько ткани должно быть проникнуто) и величины внутреннего рассеяния. Для сравнения, точка B внутри пациента симметричной цилиндрической формы получает одинаковое количество излучения из всех точек трубки во время вращения.
Были предприняты первые попытки оценить дозы КТ с использованием измерений дозы в зависимости от глубины, суммированных по всем углам и положениям рентгеновской трубки. Хотя такие данные обычно используются для высокоэнергетических пучков в лучевой терапии, такие данные «доза – глубина» слишком чувствительны к различиям в спектрах рентгеновских лучей и затуханию в тканях, чтобы иметь значение при КТ. Требовался другой подход: подход, основанный на реальных измерениях внутри фантомов, репрезентативных для пациента.
CT фантомы, термолюминесцентные дозиметры (TLD) и профили доз CT
Во время разработки процедур дозиметрии КТ, 2 стандартных фантома дозиметрии КТ были приняты Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов и используются до сих пор (рис.1): цилиндрический акриловый фантом диаметром 32 см для изображения живота взрослого и версия диаметром 16 см для изображения головы взрослого или маленьких педиатрических тел ( 1 ). Оба имеют толщину 15 см (в направлении оси z ) и содержат несколько отверстий диаметром 1 см для установки дозиметров. Отверстия находятся в центре фантома и на глубине 1 см в положениях на 3, 6, 9 и 12 часов (называемых периферийными участками). Некоторые модели имеют отверстия в других местах колодца.
РИСУНОК 1.Стандартные дозиметрические фантомы CT состоят из цилиндрических акриловых фантомов с отверстиями для установки дозиметра в различных местах. Два размера: 16 см в диаметре для изображения головы и маленьких детских тел и 32 см в диаметре для взрослых. (Предоставлено Лоуренсом Ротенбергом.)
Первый шаг — понять природу излучения внутри фантома и исследовать форму луча излучения в направлении z- .Размер рентгеновского луча в направлении z- («ширина луча») обычно составляет 10 мм или меньше (обычно эквивалентно толщине среза). Из-за практических трудностей в использовании ионизационных камер, размер которых обычно превышал ширину измеряемых пучков, для этих исследований использовались TLD ( 1,2 ).
Каждый TLD представляет собой небольшой кристалл (чаще всего фторида лития) размером 3 мм в квадрате на 1 мм толщиной. Специальные вставки TLD были разработаны для удержания нескольких TLD, что позволяет измерять дозу рентгеновского излучения на близком расстоянии внутри пучка рентгеновских лучей и проводить измерения вне пучка (рис.2). Закрытая вставка будет помещена в фантомное отверстие, и одно сканирование будет выполнено с вставкой по центру среза (были отсканированы специальные выравнивающие вставки, чтобы точно определить центр среза перед сканированием TLD). Затем были считаны открытые TLD, и доза облучения для каждого TLD была нанесена на график относительно его положения по оси z .
РИСУНОК 2.Фантомная вставка для удержания TLD, используемых для измерения профилей дозы. TLD расположены близко друг к другу в пределах первичного пучка рентгеновских лучей и находятся дальше друг от друга для измерения хвостов профиля.
Пример такого графика — или профиля дозы для одного среза — для толщины среза 10 мм показан на рисунке 3. Для этого примера профиля дозы следует отметить два наблюдения: во-первых, ширина профиля на уровнях, соответствующих 50 % пиковой дозы (называемой полной шириной на половине высоты) приблизительно равен толщине среза; это наблюдение имеет смысл в том, что более широкий луч без необходимости обнажил бы соседнюю ткань, тогда как более узкий луч пропустил бы часть ткани внутри среза.Во-вторых, значительный уровень радиации все еще находится за пределами среза шириной 10 мм и переносит часть дозы на соседние срезы. Фактически, измеримое количество дозы (в основном из-за рассеивания) может распространяться на несколько сантиметров по обе стороны от облученного среза.
РИСУНОК 3.Пример доз, измеренных TLD внутри фантома для толщины среза 10 мм, построенный как функция положения TLD по оси z . Этот тип графика называется профилем дозы.Толщина среза для односрезовых компьютерных томографов обычно эквивалентна полной ширине на половине максимального профиля дозы.
Вывод состоит в том, что каждый срез ткани получает излучение не только при сканировании этого среза, но также и при сканировании соседних срезов. Точное количество дополнительной дозы, полученной срезом от других срезов в серии, зависит от нескольких факторов, включая геометрию сканера, конструкцию коллиматора, расстояние между срезами и положение среза в серии срезов.Осевые (неспиральные) исследования обычно состоят из более чем 10 срезов с постоянным интервалом. Расстояние обычно равно толщине среза, и в этом случае срезы называют смежными. На рисунке 4 показан пример кумулятивной дозы от серии смежных срезов. Средняя кумулятивная доза на центральные срезы из такой серии срезов с постоянным интервалом называется средней дозой для нескольких срезов (MSAD). MSAD может в 1,25–1,4 раза превышать дозу для одного среза, в зависимости от факторов, описанных выше.Суммарная доза для конечных срезов несколько ниже, чем для центральных срезов из-за отсутствия вклада с одной стороны.
РИСУНОК 4.Кумулятивная доза от серии смежных срезов известна как средняя доза мультисрезов (MSAD). Хвосты профиля дозы простираются довольно далеко от центра рентгеновского луча и, таким образом, вносят дозу облучения в близлежащие срезы. Общая доза для процедуры состоит из нескольких смежных срезов и обычно на 25-40% выше, чем доза для одного среза.
Практическая КТ-дозиметрия
Несмотря на информативность, рутинные измерения профиля дозы с помощью TLD не являются клинически практичными: измерения требуют больших затрат времени и труда, требуют осторожного обращения и методов калибровки и требуют специального оборудования. Были использованы и другие методы, но либо они требовали много времени и труда (методы на основе пленки), либо использовались устройства, которые не были коммерчески доступны ( 3,4 ). Потребовалась практическая процедура, и вскоре была разработана одна, которая напрямую измеряет значение, тесно связанное с MSAD и требующее только прямых измерений ионизационной камеры ( 5 — 7 ).Чтобы понять, как производится такое измерение, рассмотрим геометрический аргумент, показанный на рисунке 5.
РИСУНОК 5.(A) Доза для среза 1 при сканировании среза 1. (B) Доза для среза 1 от сканирования среза 2 равна дозе для среза 2 от сканирования среза 1. (C) Доза для среза 1 от сканирования среза 3 равна дозе к срезу 3 от сканирования среза 1. (D) Доза для среза 1 от сканирования всех срезов равна дозе для всех срезов от сканирования среза 1 или общей площади под профилем дозы, которая измеряется с использованием длинная ионизационная камера.
На рис. 5A показан профиль одного среза при сканировании среза (который мы обозначаем срезом 1). Заштрихованная область представляет дозу, которую получает ткань среза 1, когда срез 1 действительно сканируется. Однако, как отмечалось, хвосты профиля дозы также откладывают часть дозы в соседних срезах ткани. Теперь предположим, что мы сканируем непрерывный срез (срез 2) (рис. 5B). Более темная заштрихованная область справа от среза 1 представляет дозу, которую сканирование среза 1 дает ткани среза 2.Обратите внимание на симметрию, что эта доза равна дозе, полученной срезом 1 при сканировании среза 2. Мы повторяем это важное соотношение следующим образом: доза, которую сканирование среза 1 дает срезу 2, равна дозе, которую срез 1 получает от сканирования среза. 2.
Продолжая таким же образом, мы сканируем третий непрерывный срез (рис. 5C). Как и раньше, самая темная заштрихованная область справа представляет дозу, внесенную в срез 3 при сканировании среза 1, что равняется дозе, которую сканирование среза 3 дает срезу 1.То есть доза, которую сканирование среза 1 дает срезу 3, равна дозе, которую срез 1 получает от сканирования среза 3.
Выполняя итерацию таким образом для всех срезов по обе стороны от среза 1, мы приходим к следующему выводу: Уравнение. 1
Теперь предположим, что доза, данная срезом 1 всем срезам, представляет собой просто общую дозу (то есть общую площадь) под профилем дозы для одного среза на фиг. 5A (перерисована на фиг. 5D, чтобы выделить всю дозу под кривой. ).Концептуально измерить общую дозу под профилем легко: используйте ионизационную камеру, достаточно длинную, чтобы перехватить всю дозу в хвостах профиля ( 5,6 ). Коммерчески доступная ионизационная камера CT с активной длиной 100 мм показана на рисунке 6 (вопрос о том, действительно ли длина 100 мм достаточно для перекрытия полного профиля, обсуждается в Приложении A). Камера вставляется в одно из отверстий фантома и центрируется в отверстии относительно толщины фантома в направлении z- , и одно сканирование получается вокруг центра фантома.Соответствующий коэффициент f (обычно 0,87) и калибровочный коэффициент применяются к показаниям, которые затем умножаются на длину камеры и делятся на толщину среза.
РИСУНОК 6.Пример ионизационной камеры CT длиной 100 мм для измерения CTDI.
Хотя измерение камеры используется для определения левой части уравнения 1, мы интерпретируем результат как правую часть: то есть как дозу, полученную срезом при сканировании всех смежных срезов в серии.Такое измерение называется индексом дозы CT (CTDI). Полная формула с использованием камеры длиной L, f-фактора 0,87 и среза толщиной T выглядит следующим образом: Уравнение. 2 CTDI, полученный с использованием камеры диаметром 100 мм (наиболее часто используемый тип), обозначается как CTDI 100 . Уравнение 2 обобщается для многосрезового КТ (будет обсуждаться в третьей статье этой серии) путем замены T в знаменателе на N × T, где N — количество одновременно полученных срезов толщиной T ( n = 1 для одиночных -срез КТ).Физически N × T — это общая ширина луча в направлении z- , облучающего N одновременных срезов. Применение коэффициента L / T (или L / [N × T] для многосрезового КТ) в уравнении 2 физически эквивалентно предположению, что вся доза облучения, перехваченная на всю длину камеры L, была фактически отложена в пределах толщины T отсканированного среза. . Мы повторяем значение CTDI: это доза (в месте фантома, в котором она измеряется) от полной серии смежных срезов. Когда это определение сравнивается с определением MSAD, кажется, что CTDI и MSAD эквивалентны; Фактически, единственное практическое различие — это длина включенного профиля дозы.Другие версии CTDI (например, CTDI perfect и CTDI норматив ) также различаются только длиной включенного профиля дозы. Эти различия обсуждаются в Приложении A. Для наших целей мы будем ссылаться на CTDI, измеренный на длине профиля 100 мм (CTDI 100 ), потому что это наиболее часто измеряемый параметр.
В целом, CTDI, измеренные в дозиметрическом фантоме в разных местах и на разных глубинах, будут разными. На рисунке 7 показаны типичные CTDI, измеренные при 120 кВп на односрезовом компьютерном томографе фантомов головы и тела с 5-миллиметровой коллимацией (толщина среза 5 мм) с использованием клинической техники.Дозы для 4 периферийных (глубиной 1 см) отверстия почти одинаковы, как и следовало ожидать, исходя из симметрии сканирования на 360 °. CTDI, измеренный в положении «6 часов» в фантоме тела, часто несколько ниже из-за затухания стола. CTDI в центре фантома головы почти такой же, как и на периферии, тогда как центральный CTDI в фантоме тела составляет более половины периферического CTDI. Сканирование с высоким пиковым напряжением (≥120) и симметричным (360 °) сканированием, по-видимому, дает дозы, которые меняются с глубиной лишь умеренно в фантоме тела и почти не достигаются в фантоме головы.Этот несколько противоречивый результат связан с эффектами компенсации: доза от первичного излучения выше на периферии в обоих случаях, но доза от рассеяния значительно увеличивается к центру. Поскольку измерение с помощью длинной ионизационной камеры включает хвосты профиля дозы (которые в основном представляют собой разброс), CTDI автоматически включают как первичный, так и рассеянный вклады в дозу.
РИСУНОК 7.Типичные центральные и периферические дозы (CTDI) в фантомах головы и тела.Центральная доза примерно равна периферической дозе в фантоме головы и более чем вдвое меньше периферической дозы в фантоме тела. Взвешенная сумма центральной и периферической доз, известная как CTDIw, представляет собой однозначную оценку дозы облучения пациента в сканированном объеме.
В свете незначительного или умеренного изменения CTDI с глубиной, разумно спросить, есть ли в фантоме средний CTDI, который можно использовать в качестве однозначного показателя дозы облучения пациента. Обычно используемый такой индикатор — это взвешенный CTDI (CTDI W ): Eq.3 CTDI, измеренный в положении «12 часов», обычно используется для CTDI периферии . Значения CTDI W для размеров головы и тела на рисунке 7 составляют 4,3 и 1,8 сГр соответственно. CTDI W или связанный с ним индикатор, называемый CTDI volume , часто отображается на консоли оператора КТ во время настройки параметров сканирования.
CTDI для несмежных срезов и CTDI для спирального сканирования
CTDI, определенный выше и в Приложении A, предполагает процедуры, состоящие из смежных срезов: то есть интервал среза I равен толщине среза T (или N × T в случае многосрезового CT).Обычно это происходит при осевом сканировании. Для спирального CT параметром, аналогичным шагу среза, является перемещение стола за оборот, которое включается в шаг спирали, P. Шаг определяется как перемещение стола за оборот I, деленное на толщину среза T (или, в более общем смысле, как I, деленное на N × T для мультиспиральной CT) ( 8 ). 4
Поскольку спиральное сканирование с P, равным 1, по существу эквивалентно осевому сканированию с непрерывными срезами, CTDI для таких сканирований примерно такие же, как и для осевого сканирования с непрерывным срезом с использованием эквивалентной техники (эквивалентные пиковые напряжения, силы тока, время сканирования и толщина срезов ).Однако при спиральной КТ обычно используется шаг больше 1 (соответствующий более широкому интервалу между рентгеновскими лучами соседних вращений), а в многосрезовой КТ — шаг меньше 1 (более узкий интервал с большим перекрытием рентгеновских лучей от последовательных вращений).
Чтобы учесть влияние шага на спиральную дозу и учесть дозы осевого сканирования, когда расстояние между срезами I отличается от толщины срезов T (или N × T), вводится индикатор CTDI volume : Eq. 5 Например, если CTDIw для спирального сканирования с P, равным 1, составляет 3 сГр, то CTDI для того же протокола сканирования, но с P, равным 1.5 будет 3 / 1,5 или 2 сГр. Фактически CTDI , том , распределяет дозу, соответствующую CTDIw, на более длинную (P> 1) или более короткую (P <1) z -осную длину ткани ( 9 ).
Продукты длины доза и эффективная доза
Разумное беспокойство по поводу дозы и риска компьютерной томографии связано с количеством и типом облученного тела. Чтобы понять беспокойство по поводу объема облученной анатомии, рассмотрим следующий сценарий:Джонс подвергается компьютерной томографии, состоящей из 20 смежных срезов толщиной 5 мм (или, что эквивалентно, спирального сканирования длиной 100 мм с шагом 1). Г-н Смит выполняет сканирование, которое идентично, за исключением количества срезов — 40, а не 20 (или эквивалентное 200-миллиметровое спиральное сканирование с шагом 1). В каждом случае CTDI w , измеренный в фантоме тела, будет одинаковым (например, 3 сГр). Однако теоретически мы полагаем, что г-н Смит подвергается большему радиационному риску, чем г-н Джонс, потому что его лучевая нагрузка вдвое больше, чем у мистера Джонса.Джонс (вдвое больше тканей получили дозу облучения 3 сГр).
CTDI в любой форме — это оценка средней дозы облучения только в облучаемом объеме. Риск от ионизирующего излучения, однако, более тесно связан с общим количеством дозы радиации (то есть энергии), вложенной в пациента. Ясно, что мистер Смит получил больше вложенной энергии, чем мистер Джонс. Одним из показателей, который пропорционален общей вложенной энергии, является произведение дозы на длину, определяемое следующим образом: Ур.6, где L — общая длина исследования в направлении z- . Некоторые компьютерные томографы отображают произведение «доза – длина» вместе с CTDI для каждого сканирования. Хотя произведение дозы и длины пропорционально общей вложенной энергии, оно само по себе не является подходящим индикатором риска, поскольку произведение дозы и длины не учитывает радиочувствительность облученных тканей. Для этого введено понятие эффективной дозы (D E ) ( 10 ).
D E определяется как доза облучения, которая, если она получена всем телом, обеспечивает такой же радиационный риск (т.е. рака), как и более высокая доза, полученная фактически облучаемой ограниченной частью тела (то есть отсканированным объемом) ( 11 ). Формально расчет D E сложен: мы должны оценить дозы, депонированные в каждом типе органа и ткани, которые затем взвешиваются в соответствии с радиочувствительностью и суммируются. Количество облучаемых анатомических образований и весовые коэффициенты для вовлеченных тканей резко влияют на полученный D E . Американский колледж радиологии в рамках своей программы аккредитации компьютерной томографии использует измерения CTDIw головы и тела для оценки эффективной дозы при рутинных исследованиях головы и живота.Для сканирования головы Американский колледж радиологии предполагает общую длину сканирования 17,5 см и общий весовой коэффициент ткани 0,0023. Для живота длина сканирования и весовой коэффициент составляют 25 см и 0,015 соответственно. Используя значения CTDIw, рассчитанные для Рисунка 7, и предполагая, что срезы непрерывны (или шаг 1), D E для сканирования головы и живота оценивается как 0,17 и 0,68 сГр соответственно. Хотя CTDIw для головы намного выше, чем для тела, брюшной D E намного выше (в 4 раза), чем голова D E , потому что сканирование головы облучает меньшее количество менее радиочувствительной ткани ( нервная ткань и кость).
После расчета D E весьма полезен: его можно добавить к дозе, полученной пациентом при других рентгеновских исследованиях, или ее можно сравнить с дозами излучения от естественных источников. Активно ведется большая работа по разработке простых методов оценки эффективных доз на основе измерений CTDI ( 12 ).
Факторы конструкции сканера, влияющие на дозу облучения КТ
Как факторы конструкции сканера, так и факторы клинического протокола влияют на дозу облучения пациента.Некоторые конструктивные факторы, влияющие на дозу облучения, необходимую для достижения определенного качества изображения, обсуждались ранее ( 8 ). Это факторы, определяющие эффективность дозы ( 9 ).
Способность сканера визуализировать низкоконтрастные структуры по своей природе ограничена шумом изображения (квантовой пятнистостью). Для любой заданной дозы облучения максимальная чувствительность требует захвата и использования как можно большего количества первичных рентгеновских лучей, исходящих от пациента. Эффективность дозы, определяемая как доля первичных рентгеновских лучей, выходящих из пациента, которые вносят вклад в изображение, состоит из двух компонентов: геометрической эффективности (доля прошедшего рентгеновского излучения, взаимодействующего с активными областями детектора) и эффективности поглощения (доля фактически захваченного x -лучей, взаимодействующих с активными участками детектора).Геометрическая эффективность снижается, если часть рентгеновских лучей поглощается до обнаружения (например, в корпусе детектора) или если некоторые рентгеновские лучи не попадают в активные области детектора (например, проходя между детекторами или поражая неактивные разделители между отдельными детекторами). Эффективность поглощения снижается, если некоторые рентгеновские лучи, попадающие в детекторы, не поглощаются.
Геометрическая эффективность современных односрезовых сканеров третьего поколения относительно высока (~ 80%), при этом потери в основном связаны с мертвыми пространствами между элементами детектора.Геометрическая эффективность снижается в многосрезовой КТ по сравнению с односрезовой КТ, потому что расстояния между элементами детектора в направлении z- создают больше мертвого пространства, и потому, что необходимо отбросить большую часть полутени пучка в направлении z- (проблемы с дозой в Мультисрезовая КТ будет рассмотрена в третьей статье этого цикла). В современных сканерах обычно используются твердотельные детекторы с эффективностью поглощения порядка 99%.
Другие конструктивные факторы, которые могут повлиять на дозу облучения, включают расстояние рентгеновской трубки от изоцентра (и, следовательно, от пациента), конструкцию коллиматора рентгеновского пучка для подготовки пациента, а также конструкцию фильтра-бабочки и любые другие лучевая фильтрация.
Факторы клинического сканирования, влияющие на дозу облучения КТ
Доза облучения зависит от тока трубки (силы тока), времени сканирования среза и пикового напряжения трубки. Как и в рентгенографии, ток трубки и время сканирования среза берутся вместе как мА в зависимости от дозы облучения и качества изображения. Увеличение мАс (путем увеличения тока трубки или времени сканирования среза) увеличивает дозу пропорционально: 300 мАс доставляют вдвое большую дозу 150 мАс. Таким образом, доза CT-излучения часто выражается как доза на мАс (или на 100 мАс).
Увеличение пикового напряжения (при прочих равных) также увеличивает дозу облучения, потому что луч несет больше энергии. Однако увеличение пикового напряжения значительно увеличивает интенсивность рентгеновских лучей, проникающих через пациента и достигающих детекторов. Следовательно, для достижения аналогичного качества изображения необходимы значительно меньшие мА. Следовательно, более высокое пиковое напряжение не обязательно означает увеличение дозы для пациента и, фактически, может позволить снизить дозу.
CT, толщина срезов, расстояние между срезами и шаг спирали также могут влиять на дозу. В однослойной КТ с хорошо спроектированными коллиматорами доза (как указано CTDI) относительно не зависит от толщины среза для смежных срезов. Конечно, общая длина отсканированной области, а также расстояние между срезами будут определять, сколько общей энергии вкладывается в пациента. Для тех же методов дозы для спирального сканирования с шагом 1,0 эквивалентны осевому сканированию с непрерывными срезами.Шаги больше или меньше 1 снова влияют на значения CTDI пропорционально.
Относительно недавнее нововведение, позволяющее снизить дозу во многих случаях, — это модуляция мА. До того, как модуляция мА стала использоваться, одно значение мА было указано (на основании опыта или рекомендаций производителя) для всей длины сканирования, даже несмотря на то, что размер пациента или затухание могли значительно меняться по длине сканирования (например, сравнить затухание через грудную клетку с через брюшную полость для сканирования обеих областей).Результатом часто были излишне высокие значения мА (и дозы) для некоторых срезов и, возможно, недостаточная доза (и пониженное качество изображения) для других срезов. Используя информацию из начального обзора разведчика (цифровая рентгенограмма с низкой дозой, сформированная из линейного сканирования, когда стол движется по гентри, с неподвижной рентгеновской трубкой, например, под углом 0 ° или 90 °), значение тока сканирования регулируется индивидуально, в зависимости от положения z- , для каждого поворота трубы. Усовершенствованная версия модуляции мА, доступная на некоторых сканерах, позволяет регулировать мА не только для каждого поворота (положение z- ), но также в зависимости от угла во время каждого поворота.Зависимая от угла модуляция особенно полезна для анатомических областей, в которых переднезадняя и латеральная толщина пациента сильно различаются (например, таз). В таких случаях заранее выбранное значение мА часто недостаточно для обеспечения адекватной интенсивности рентгеновского излучения на детекторах для боковых углов или может обеспечивать чрезмерную интенсивность на детекторах для переднезадних / задне-передних углов. Угловая модуляция мА оптимизирует выбор мА для каждого угла, чтобы обеспечить наименьшую дозу облучения для требуемого уровня качества изображения ( 13 ).
Сводка
CTDI обеспечивают оценку дозы облучения в области сканирования для всей серии срезов. Хотя CTDI обычно намного выше при сканировании головы, чем при сканировании тела, D E для последнего обычно намного выше, потому что облучается больше тканей (и более радиочувствительных тканей). Кроме того, в отличие от пленочной / экранной рентгенографии, для которой требуются узкие диапазоны экспозиции, чтобы избежать пере- или недоэкспонирования, КТ-исследования могут выполняться с произвольно высокими дозами (и чем больше доза, тем лучше качество изображения).Чтобы помочь компенсировать тенденции к более высоким дозам, Американский колледж радиологии рекомендует CTDI W пределы 6 сГр (60 мГр) и 3,5 сГр (35 мГр) для рутинного сканирования головы и живота соответственно. Независимо от того, рассматриваете ли вы CTDI или D E , дозы облучения CT значительно выше, чем дозы от обследований планарной рентгенографии, которые заменили CT. Однако это увеличение более чем компенсируется тем, что обычно предоставляется гораздо больше медицинской информации.
КАЧЕСТВО ИЗОБРАЖЕНИЯ КТ
По сути, качество изображения при компьютерной томографии, как и при любой медицинской визуализации, зависит от 4 основных факторов: контраст изображения, пространственное разрешение, шум изображения и артефакты.В зависимости от диагностической задачи эти факторы взаимодействуют, чтобы определить чувствительность (способность воспринимать малоконтрастные структуры) и видимость деталей.
Контрастность изображения CT
Контрастность изображения КТ зависит от контраста объекта и контрастности дисплея. Поскольку контраст КТ-дисплея произвольный (зависит только от выбранного уровня и ширины окна), он не будет обсуждаться далее.
Как и в рентгенографии, контраст объекта КТ определяется дифференциальным ослаблением: то есть различиями в ослаблении рентгеновских лучей за счет поглощения или рассеяния в разных типах тканей и, таким образом, приводит к различиям в интенсивности рентгеновских лучей, в конечном итоге достигающих детекторов.Из-за высокого пикового напряжения и относительно высокой фильтрации пучка (жесткости пучка), используемых в КТ, взаимодействия рентгеновского излучения с тканями (за исключением кости) в подавляющем большинстве случаев являются явлениями комптоновского рассеяния. Дифференциальное затухание для комптоновского рассеяния возникает из-за различий в плотности электронов в тканях (электроны / см 3 ), которые, в свою очередь, в первую очередь связаны с различиями в физической плотности ( 14 ). Таким образом, контраст мягких тканей объекта при КТ в основном определяется различиями в физической плотности. То, что небольшие различия в плотности мягких тканей могут быть визуализированы на КТ, связано с природой изображения (двухмерное изображение двухмерного среза), способностью сопоставить небольшие различия в затухании с большими различиями в уровне серого с помощью использование окон, почти полное устранение рассеяния и использование рентгеновского излучения достаточной интенсивности.
К контрасту изображения КТ относится шкала контрастности КТ. Напомним, что числа CT получены из коэффициентов затухания вокселей, вычисленных во время реконструкции изображения с использованием следующего соотношения: Ур. 7, где μ p и μ w — линейные коэффициенты затухания для данного воксела и для воды (μ w определяется из калибровочных сканирований). Поскольку число CT является линейной функцией от μ p , график ожидаемых чисел CT для материалов с известными коэффициентами ослабления должен быть линейным во всем диапазоне клинических чисел CT (например.г., от -1,000 до +1,000). Для оценки шкалы контрастности сканера доступны различные тестовые фантомы КТ, которые содержат материалы, предназначенные для получения определенных чисел КТ (например, чисел КТ для воды, жира, мягких тканей, костей и воздуха) ( 15 ).
CT Пространственное разрешение и дискретизация
Пространственное разрешение в КТ, как и в других модальностях, — это способность различать небольшие близко расположенные объекты на изображении. Обычный тест — это оценка предельного разрешения, выполняемая с использованием тестовых шаблонов для пар линий.Шаблоны пар фантомных линий CT состоят из полос из акрила (или более плотного пластика), разделенных промежутками, содержащими менее ослабляющий материал. Ширина полос и промежутков одинакова и обычно составляет от 0,05 или менее до 0,5 см. Примеры показаны на рисунке 8. Свинцовые стержни или другие плотные материалы могут вызвать серьезные артефакты на КТ-изображениях и поэтому не используются. Для разрешения тестового шаблона пары линий необходимо, чтобы каждая полоса и пробел были видны на изображении отдельно. Каждая полоса плюс прилегающий пробел называется парой линий.Вместо указания ширины полосы, размеры полосок обычно описываются пространственной частотой в парах линий на сантиметр, определяемой следующим образом, где ширина полосы выражается в сантиметрах: 8 Например, узор с полосами шириной 0,1 см и пробелами имеет пространственную частоту 1 / (2 × 0,1) или 5 пар линий на сантиметр. При рентгенографии размер фокусного пятна рентгеновской трубки и размытость, возникающая в рецепторе изображения, являются основными причинами снижения разрешения. Хотя размер фокального пятна действительно влияет на пространственное разрешение КТ, разрешение КТ обычно ограничивается размером измерений детектора (называемым размером апертуры) и разносом измерений детектора, используемых для восстановления изображения.Эта концепция, называемая выборкой, проиллюстрирована на рисунке 9. На рисунке 9A рассмотрим сканирование фантома, содержащего гипотетический тестовый образец: например, 5 пар линий на сантиметр (полосы 0,1 см) и детекторы, которые в два раза шире. (скажем, 0,2 см с интервалом 0,2 мм). Апертура приблизительно равна ширине детектора — ширина, которая в данном случае явно слишком велика, чтобы разрешить более мелкие полосы: все измерения (показанные внизу рисунка как данные просмотра) включают затухание, соответствующее половине полосы и половине пространства.Вместо этого предположим, что размер детектора уменьшен до размера полосок, но расстояние сохраняется на уровне 0,2 см (5 образцов на сантиметр; рис. 9B). Теперь, даже несмотря на то, что апертура достаточно мала, полосы по-прежнему не разрешены, потому что образцы находятся слишком далеко друг от друга (в этом случае промежутки между полосами отсутствуют). В дополнение к небольшой апертуре для хорошего разрешения требуются измерения, расположенные близко друг к другу (рис. 9C). Общее правило, известное как критерий Найквиста, гласит, что разрешение N пар линий на сантиметр требует измерения как минимум 2 × N образцов на сантиметр.Например, для разрешения 5 пар линий на сантиметр (полоски 0,010 см) требуется не менее 10 измерений на сантиметр. Некоторые факторы конструкции сканера, связанные с отбором образцов, обсуждались ранее ( 8 ).
РИСУНОК 8.КТ фантом с пространственным разрешением, состоящий из 4–12 пар линий на сантиметр (от фантома аккредитации Американского колледжа радиологии), реконструированный с использованием стандартного (A) и костного (B, высокое разрешение) фильтров.
РИСУНОК 9.Разрешение КТ ограничивается выборкой — размером и интервалом измерений (выборок), используемых для формирования изображения.(A) Шаблон не разрешен, потому что размер образца (апертура) слишком большой. (B) Образец неразрешен, потому что образцы слишком далеко друг от друга. (C) Размер апертуры и расстояние между образцами достаточны для разрешения рисунка. (D) «Эффективное» разрешение может быть ниже ожидаемого из-за положения образцов относительно шаблона. (E) При сглаживании паттерн кажется разрешенным, но с неправильным количеством полосок.
Две дополнительные проблемы, связанные с выборкой, — эффективное разрешение и наложение. Критерий Найквиста не гарантирует, что образец будет разрешен.Например, предположим, что мы берем схему на фиг. 9C, но смещаем детекторы относительно схемы (фиг. 9D). Еще раз, из-за неудачного совмещения тестового объекта и образцов, из-за которого каждое измерение перекрывает полосу и пробел, полосы не отображаются. Подразумевается, что измерение предельного разрешения (с использованием теста пар линий) в целом будет ниже, чем можно было бы ожидать на основе размера апертуры и расстояния между образцами. Это эффективное разрешение аналогично фактору Келла, связанному с вертикальным разрешением телевизионного экрана.
Псевдонимы показаны на рисунке 9E. Хотя штриховая диаграмма слишком мала, чтобы ее можно было разрешить с помощью размера и расстояния между детекторами, данные обзора показывают последовательность более высоких и более низких ослаблений. Однако данные обзора показывают меньше максимумов и минимумов (полос и промежутков), чем на самом деле в паттерне. На изображении могут быть отдельные полосы и промежутки, но их меньше, чем на самом деле. Такое изображение называется псевдонимом: из-за недостаточной выборки тестовый шаблон с более высокой пространственной частотой появляется в псевдониме шаблона с более низкой частотой и, таким образом, не разрешается по-настоящему.
Другие факторы CT, влияющие на пространственное разрешение
Размер фокусного пятна действительно влияет на разрешение КТ, но в меньшей степени, чем при рентгенографии. Движение также может вызывать размытие, хотя более важным эффектом движения является возможное создание артефактов. Два дополнительных фактора — один потенциальный и один общий — это размер матрицы и фильтр восстановления.
На отображаемое пространственное разрешение может влиять реконструкция или слишком большие пиксели отображения.Основное ограничение — размер и интервал измерений детектора. Предположим, что на основе выборки должно быть возможно разрешить 10 пар линий на сантиметр (столбики 0,05 см). Теперь предположим, что матрица размером 512 × 512 пикселей реконструирована, представляя круг сканирования размером 50 см (т. Е. Изображение представляет собой область диаметром 50 см, что может иметь место при сканировании большого тела). Размер пикселей составляет примерно 0,1 × 0,1 см (т.е. 50 см / 512 пикселей), что слишком велико для разрешения 0.Бруски 05 см. Часто возможно, если необработанные данные еще не перезаписаны, восстановить изображение по меньшему кругу, скажем, 25 см, чтобы получить меньшие пиксели и более высокое разрешение. Точно так же, если пиксели дисплея больше пикселей матрицы реконструкции (что редко встречается в современных сканерах), полное разрешение не будет отображаться. В таком случае графическое масштабирование (функция, доступная на большинстве сканеров) обеспечит лучшее разрешение.
Хотя размер пикселя может влиять на разрешение (например, для больших кругов сканирования), фильтр реконструкции всегда влияет на разрешение — часто значительно.Фильтр реконструкции применяется во время реконструкции отфильтрованной обратной проекции, чтобы удалить размытие изображений ( 8 ). Однако обычно фильтр преднамеренно выбирается для получения несколько размытых изображений. Причина в том, что слишком резкие изображения КТ обычно слишком искажены шумом изображения для большинства диагностических задач. Размытый фильтр также размывает шум и, таким образом, обеспечивает лучшее качество диагностики. Для задач визуализации, требующих более подробной информации (например, для просмотра костей), оператор может дополнительно выбрать более резкий фильтр при настройке параметров для сканирования.Обычно используемые фильтры разработаны как компромисс между приемлемым пространственным разрешением и приемлемым уровнем шума. Например, стандартный фильтр может создавать изображения с максимальным разрешением, скажем, 6 пар линий на сантиметр, тогда как костный фильтр может создавать изображения с разрешением 10 пар линий на миллиметр или лучше. Показан тестовый фантом, реконструированный как со стандартным фильтром (фиг. 8A), так и с фильтром высокого разрешения (костный) (фиг. 8B).
Шум изображения
Если графический курсор используется для отображения чисел CT пикселей в изображении однородного фантома (например,g., фантом, содержащий всю воду), видно, что числа CT не являются однородными, а скорее колеблются вокруг среднего значения (которое должно быть приблизительно 0 для воды): некоторые пиксели равны 0, некоторые — +1, некоторые +2. , некоторые −1 и т. д. Эти случайные колебания числа КТ однородных материалов на КТ-изображениях проявляются как зернистость. Эта зернистость является аналогом КТ радиографической квантовой неоднородности и имеет ту же природу: она связана с использованием ограниченного числа фотонов для формирования изображения ( 16,17 ).
В рентгенографии шум изображения связан с количеством рентгеновских фотонов, составляющих каждую небольшую область изображения (например, каждый пиксель прямой цифровой рентгенограммы). В КТ рентгеновские лучи влияют на измерения детектора, а не на отдельные пиксели. Таким образом, шум КТ-изображения связан с количеством рентгеновских лучей, участвующих в каждом измерении детектора. Чтобы понять, как метод КТ влияет на шум, нужно представить, как каждый фактор в методе влияет на количество обнаруженных рентгеновских лучей.Примеры:
Сила тока рентгеновской трубки: изменение значения мА пропорционально изменяет интенсивность луча и, следовательно, количество рентгеновских лучей. Например, удвоение значения мА удвоит интенсивность луча и количество рентгеновских лучей, обнаруженных при каждом измерении.
Время сканирования (вращения): изменение времени сканирования изменяет продолжительность каждого измерения — и, следовательно, количество обнаруженных рентгеновских лучей — пропорционально. Поскольку сила тока и время сканирования одинаково влияют на шум и дозу пациента, они обычно рассматриваются вместе как мА × с или мАс.
Толщина среза: изменение толщины изменяет ширину луча, входящего в каждый детектор, и, следовательно, количество обнаруженных рентгеновских лучей примерно пропорционально. Например, по сравнению с толщиной среза 5 мм, толщина 10 мм примерно вдвое увеличивает количество рентгеновских лучей, попадающих в каждый детектор.
Пиковое напряжение в киловольтах: увеличение максимального напряжения в киловольтах увеличивает количество рентгеновских лучей, проникающих через пациента и достигающих детекторов. Таким образом, увеличение напряжения в киловольтах снижает шум изображения, но также может (немного) снизить контраст объекта.
Хотя фильтр реконструкции не влияет на количество обнаруженных рентгеновских лучей, он существенно влияет на внешний вид шума на изображении: плавные фильтры размывают шум, уменьшая его визуальное воздействие, тогда как фильтры резкости усиливают шум. На изображениях мягких тканей шум обычно больше мешает, чем размытость, поэтому предпочтительны более плавные фильтры. На изображениях структур с краями и мелкими деталями, такими как кости, размытие обычно больше мешает, чем шум, и предпочтительнее более резкие фильтры.Для сравнения на рисунке 10 показаны примеры шума при сканировании однородных фантомов с использованием стандартных фильтров и фильтров более высокого разрешения (костные) и со стандартными и очень низкими значениями мА.
РИСУНОК 10.Шум изображения КТ зависит от количества рентгеновских фотонов, вносящих вклад в изображение. (A и B) Сравнение шума при сканировании с использованием 270 мАс (типичное клиническое значение) и 100 мАс. (C) Внешний вид шума изображения сильно зависит от фильтра реконструкции; резкий фильтр, такой как кость, также усиливает резкость шума.
Поскольку шум КТ проявляется в виде колебаний в числах КТ, измерение шума изображения является измерением этих колебаний, и такое измерение может быть выполнено с использованием областей интереса (ОИ) при сканировании однородного фантома. Функция статистической области интереса (доступная на большинстве компьютерных томографов) позволяет пользователям размещать прямоугольную или овальную область интереса на изображении, в пределах которой вычисляется среднее значение и стандартное отклонение (SD) чисел CT для включенных пикселей. SD указывает величину случайных колебаний числа CT и, таким образом, связано с шумом: чем больше SD, тем выше шум изображения.Более полное обсуждение шума изображения представлено в Приложении B.
Поскольку шум вызывает наибольшее беспокойство при просмотре низкоконтрастных структур мягких тканей, важным тестом производительности сканера является то, насколько хорошо малоконтрастные тестовые объекты видны при типичных уровнях шума. На рисунке 11 показан пример тестового фантома с низким контрастом, состоящего из групп стержней, внедренных в материал, обеспечивающий контраст объекта приблизительно на 0,6% (т.е. номинальная разница числа КТ, равная 6, между стержнями и фоном).Группы стержней имеют диаметр от 6 до 2 мм. В этом примере видны 5-миллиметровые стержни, а более мелкие теряются в шуме.
РИСУНОК 11.Низкоконтрастный фантом для проверки работы КТ в присутствии типичных уровней шума изображения (от фантома аккредитации Американского колледжа радиологии). Видны пятимиллиметровые стержни, но более мелкие не видны из-за шума.
Артефакты изображения
Артефакты можно определить как любую структуру, которая видна на изображении, но не отражает фактическую анатомию.Большинство типов артефактов CT делятся на 1 из 3 категорий: артефакты затенения, артефакты кольца или артефакты полос ( 18 ).
Самый распространенный тип артефактов затенения — это эффекты усиления луча. Артефакты усиления пучка фактически присутствуют на всех КТ-изображениях в той или иной степени и связаны с несовершенной коррекцией усиления пучка. Они проявляются в виде неоднородностей в числах CT однородного материала, например, в числах CT, которые ниже в центре однородного фантома, чем на периферии.Такие неоднородности, как правило, довольно малы (<5 HU) и не видны, если только не просматривается сканирование однородного фантома с очень узким окном. Однако иногда большее затвердевание происходит, когда сканирование проходит через толстые участки кости или через контрастное вещество. В этом случае области гипоинтенсивности (т. Е. Числа CT ниже ожидаемого) могут появиться ниже по потоку на путях чрезмерно закаленных лучей (рис. 12). Рассеивание также может вызывать артефакты затенения, хотя они редко встречаются в большинстве современных сканеров.
РИСУНОК 12.Артефакт усиления луча, вызванный необычно сильным затвердеванием рентгеновских лучей, проходящих через толстую кость.
Кольцевые или частичные кольцевые (дуговые) артефакты связаны с геометрией сканирования третьего поколения и обсуждались ранее ( 8 ). Кольцевые артефакты возникают из-за ошибок, дисбаланса, отклонений калибровки или других неточностей измерений в элементе матрицы детекторов относительно его соседей. Каждый детектор в сканере третьего поколения всегда измеряет лучи, проходящие на фиксированном расстоянии d от центра вращения, причем d зависит от расположения детектора в матрице.Любые такие неточности в измерениях от конкретного детектора, возникающие во время сканирования (или части сканирования), проецируются обратно по траекториям лучей, измеренным этим детектором. Эти неточности вносят незначительный вклад в количество пикселей на большей части изображения (потому что несколько сотен проецируемых назад значений вносят вклад в каждый пиксель), но имеют тенденцию усиливаться вдоль кольца радиуса d, где несколько таких лучей пересекаются.
Кольцевые (или дуговые, если они возникают только на части сканирования) артефакты обычно легко распознаются программными алгоритмами кольцевой коррекции и, таким образом, могут быть удалены с изображения.Кольца малого радиуса (т. Е. Около центра вращения) или дуги небольшой угловой протяженности могут не распознаваться как артефакты и, таким образом, свертываться на изображении. На практике сканеры третьего поколения чувствительны к неточностям детектора, которые без корректирующих алгоритмов были бы видны на большинстве или на всех КТ-изображениях.
Артефакты из полос могут возникать на всех сканерах. Хотя они возникают по многим причинам, большинство из них связано с несогласованными или плохими измерениями детектора. Факторы, вызывающие несогласованность, включают движение (анатомия в разных местах во время разных частей сканирования), эффекты частичного объема, металл (измеренная интенсивность, которая находится в пределах откалиброванного диапазона детектора, и, возможно, эффекты упрочнения луча и частичного объема), недостаточная интенсивность рентгеновского излучения (приводящая к высокому количеству случайных ошибок) и неисправности (искрение в трубке или несоосность системы).Несогласованность из-за эффектов частичного объема проиллюстрирована на рисунке 13. Во время осевого сканирования 360 ° один и тот же луч (или почти тот же луч) отбирается дважды, но рентгеновские лучи проходят в противоположных направлениях. Однако из-за расходимости пучка рентгеновского пучка конической формы образуются несколько разные объемы в каждом направлении. Небольшая структура, такая как край кости, может частично заходить в объем, чтобы ослабить луч, идущий в одном направлении (скажем, вниз, когда трубка находится выше), но может быть пропущена, когда луч идет из противоположной стороны. направление (вверх, когда трубка внизу).Таким образом, два измерения одного и того же пути луча несовместимы и приведут к полосе изображения.
РИСУНОК 13.Полосы частичного объема вызваны противоположными рентгеновскими лучами, которые номинально проходят через одни и те же воксели, но фактически отбирают немного разные конусообразные объемы ткани в результате расхождения луча. Небольшая структура, такая как кусок кости, обнаруживается лучом с одного направления, но пропускается противоположным лучом. Возникающая несогласованность приводит к артефакту полосы.
Независимо от источника, эффект несогласованности — создание артефакта полосы из-за природы реконструкции обратной проекции.В некоторых случаях несоответствия можно распознать и исправить с помощью программных алгоритмов. В других случаях полос можно избежать или свести к минимуму с помощью соответствующих методов сканирования, включая сканирование после 360 °, известное как пересканирование (для уменьшения полос из-за некоторого движения) или использование более тонких слоев (для минимизации эффектов частичного объема).
ЗАКЛЮЧЕНИЕ
В этой статье обсуждаются доза КТ-излучения, измерение дозы КТ и качество изображения КТ. Чаще всего используется дескриптор дозы CTDI, который представляет дозу для местоположения (например,g., глубина) в отсканированном объеме из полной серии срезов. Средневзвешенное значение CTDI, измеренного в центре и на периферии фантомов дозы, CTDI w , обеспечивает удобную оценку дозы пациента для процедуры одним числом, и это значение (или связанный показатель, который включает длину сканирования, CTDI том ) часто отображается на консоли оператора.
Качество изображенияКТ, как и в большинстве изображений, описывается с точки зрения контраста, пространственного разрешения, шума изображения и артефактов.Сильной стороной компьютерной томографии является ее способность визуализировать структуры с низким контрастом на объекте, задача, которая ограничена в первую очередь шумом и поэтому тесно связана с дозой облучения: чем выше доза, вносимая в изображение, тем менее заметны шумы изображения и тем легче воспринимать малоконтрастные структуры. Пространственное разрешение в конечном итоге ограничено выборкой, но фильтр реконструкции сильно влияет на шум изображения и разрешение.
В результате, диагностически приемлемое качество изображения при приемлемых дозах излучения требует надлежащим образом разработанных клинических протоколов, включая соответствующие пики в киловольтах, силу тока, толщину срезов и фильтры реконструкции.

 — «Есть несколько причин, по которым вам понадобится ядерная энергия. Первое: она не прерывистая. Другое дело, что это производит большое количество энергии, которую вы могли бы использовать для электролиза и получения водорода».
— «Есть несколько причин, по которым вам понадобится ядерная энергия. Первое: она не прерывистая. Другое дело, что это производит большое количество энергии, которую вы могли бы использовать для электролиза и получения водорода».
 Вам скажут, куда пойти, чтобы это сделать. Сотрудник интервенционной радиологии свяжется с вами накануне, чтобы дать инструкции и подтвердить время вашего прибытия.
Вам скажут, куда пойти, чтобы это сделать. Сотрудник интервенционной радиологии свяжется с вами накануне, чтобы дать инструкции и подтвердить время вашего прибытия. После выздоровления вас вернут в отделение радиационной онкологии на носилках для симуляции.
После выздоровления вас вернут в отделение радиационной онкологии на носилках для симуляции. Рисунок 2).
Рисунок 2). Ваш терапевт нальет теплую жидкость в большой пластиковый пакет, который будет запечатан и поставлен на стол. Вы лягте на сумку на спине, подняв руки над головой (см. Рисунок 4).Сначала жидкость будет теплой, но по мере застывания она остынет. Пока он остывает, ваш лучевой терапевт прикрепит сумку к вашей коже липкой лентой, чтобы она приняла форму вашей верхней части тела и рук. Эта процедура занимает около 15 минут. Во время симуляции и каждый день лечения вы будете лежать в этой форме, чтобы убедиться, что вы находитесь в правильном положении.
Ваш терапевт нальет теплую жидкость в большой пластиковый пакет, который будет запечатан и поставлен на стол. Вы лягте на сумку на спине, подняв руки над головой (см. Рисунок 4).Сначала жидкость будет теплой, но по мере застывания она остынет. Пока он остывает, ваш лучевой терапевт прикрепит сумку к вашей коже липкой лентой, чтобы она приняла форму вашей верхней части тела и рук. Эта процедура занимает около 15 минут. Во время симуляции и каждый день лечения вы будете лежать в этой форме, чтобы убедиться, что вы находитесь в правильном положении. Это будет сделано в отделении радиационной онкологии или в Службе молекулярной визуализации и терапии (MITS).MITS иногда называют службой ядерной медицины.
Это будет сделано в отделении радиационной онкологии или в Службе молекулярной визуализации и терапии (MITS).MITS иногда называют службой ядерной медицины. Не используйте тряпку для мытья посуды, тряпку или щетку.
Не используйте тряпку для мытья посуды, тряпку или щетку. Сюда входят гидромассажные ванны, бутылки с водой, грелки и пакеты со льдом.
Сюда входят гидромассажные ванны, бутылки с водой, грелки и пакеты со льдом.
:max_bytes(150000):strip_icc()/radioactive-warning-sign-73096487-5b8ab053c9e77c0025b81cb6.jpg) Если вы спите, старайтесь спать меньше 1 часа за раз.
Если вы спите, старайтесь спать меньше 1 часа за раз. Попросите у медсестры материал «Правильное питание во время лечения рака».
Попросите у медсестры материал «Правильное питание во время лечения рака». Благодаря нашей программе поддержки пациентов и лиц, осуществляющих уход, у вас есть возможность поговорить с бывшими пациентами и лицами, осуществляющими уход.Чтобы узнать больше об этой услуге, позвоните по телефону 212-639-5007.
Благодаря нашей программе поддержки пациентов и лиц, осуществляющих уход, у вас есть возможность поговорить с бывшими пациентами и лицами, осуществляющими уход.Чтобы узнать больше об этой услуге, позвоните по телефону 212-639-5007. Поговорите со своим врачом или медсестрой о типах упражнений, которые вы можете выполнять.
Поговорите со своим врачом или медсестрой о типах упражнений, которые вы можете выполнять.

