Что нужно, чтобы событие запомнилось?
Черный порох (дымный порох)
Черный порох (дымный порох) является метательным взрывчатым веществом, состоящим, в основном, из трех компонентов: селитра, древесный уголь, сера. При сгорании порохового состава селитра выделяет кислород необходимый для сгорания угля. Сера в пороховом составе выступает в качестве цементирующего звена между угдем и селитрой.
Изобретение пороха
Считается достоверно установленным фактом, что порох был изобретен в Китае примерно около Х века. Изобретателями считаются монахи даосистских храмов, которые проводили эксперементы с целью создания элексира бессмертия. Для создания заветного элексира монахи смешивали в разных пропорциях различные вещества. Создавались элексиры бессмертия для Китайских императоров, которые мечтая обрести бессмертие, употребляли опасные вещества. В середине девятого века одним их монахов был издан трактат, в котором были изложены составы всех изобретенных элексиров. Но самым примечательным в этом трактате было упоминание опаснейшего элексира, который воспламенившись причинил ожоги рук китайских алхимиков. Погасить элексир не удалось и за некоторое время сгорел дом изобретателей. В переводе с китайского слово «порох» звучит как «пламя медицины»
Применение пороха в Китае
Обнаружив способность порошка взрываться и дымить китайцы начали широко использовать для праздничных случаев. Порох стал основным компонентом для хлопушек и фейерверков. Правильная комбинация компонентов позволяла выбрасывать в небо тысячи ярких огней, придавая празднику незабываемые впечатления. Стабелизировав формулу пороха китайцы научились его взрывать. В 11 веке было изобретено первое боевое оружие- ракеты, где горение пороха переходилов в детонацию. Ракеты применялись при захвате крепостей, помимо боевых качеств ракеты оказывали психологическое воздействие на врага. Самым мощным боевым оружием, изобретенным Китайцами, были глинянные горшки, которые при взрыве разлитались сотнями осколков.
Появление пороха в Европе
Порох в Европе появился примерно в 11 веке. Завезли порох арабские купцы в ракетах для фейерверков. В боевых условиях порох с успехом применялся монголами при захвате рыцарских замков. Под стеной замка делался большой подкоп, в котором размещался большой пороховой заряд. Взрыв заряда пороха образовывал в стене большую брешь, через которую в замок врывались воины. При захвате Испании в 1118 арабами впервые были применены пушки. В 1308 году уже испанцы, перенявшие от арабов пушки, успешно штурмовали Гибралтарскую крепость. После этого изготовление пушек началось во всей Европе.
Бертольд Шварц
Повторно порох был изобретен в 14 веке немецким монахом Бертольдом Шварцем. Увлечением ученого была химия, а поскольку в те времена ученых зачастую принимали за колдунов- это увлечение привело его за решетку. Именно в заключении монахом и был изобретен порох. Позним вечером Бертольд Шварц перемалывал в ступке компоненты (сера, уголь, селитра). Поскольку было темно им было решено зажечь свечу. Высекая огонь искра случайно попала в ступку, произошел сильный хлопок. По счастливой случайности экспериментатор не пострадал. Монах повторно смешал в ступке компоненты и инициировал поджег смеси- результат был анологичным. Так был изобретен порох европийским ученым.
Области применения дымного пороха сегодня
1. В настоящее время дымный порох широко применяется в военном деле. В артеллерии из него готовят воспламенители к выстрелам, подрывники используют порох в бикфордовом шнуре и т.д. 2. Охотники используют дымный порох при снаряжении патронов. 3. Ценным свойством дымного пороха является следующее: при сгорании в зарядных камерах происходит откалывание или сдвигание горной породы по линии зарядных шпуров. При этом в горной породе не образуется трещин, что важно при добыче штучного камня, который в последствии используется для изготовления например памятников. Также порох используется в нефтяных скважинах, при их ремонтных работах.
Открытие пороха. | Fandom
Сегодня, ученые из ГК изобрели порох…
Чёрный порох состоит обычно из трёх компонентов: селитры, угля и серы. При сгорании пороха селитра даёт кислород для сжигания угля; сера — цементирует угольно-селитряную смесь. Кроме того, обладая более низкой температурой воспламенения, чем уголь, сера ускоряет процесс воспламенения пороха
Обычно для изготовления пороха берётся калиевая селитра (нитрат калия), как менее гигроскопичная по сравнению с другими селитрами (например, натриевой). Селитра должна отличаться высокой степенью чистоты — 99,8 %;
Древесный уголь для пороха получают путём обжига (пиролиза) несмолистых пород дерева (ольха и особенно крушина) с получением продукта, на 80—90 % состоящего из углерода; применение смолистой древесины отрицательно сказывается на свойствах пороха, да и хвойные породы не склонны к образованию угля. Однако хвойные дрова применяют для инициации процесса горения с последующей засыпкой древесины иных пород при историческом способе производства древесного угля. Следует отметить, что до XIX века выжигание древесного угля производилось в угольных ямах, не позволявших получать однородный по своим свойствам продукт (ввиду наличия одновременно и недожжёной (не пиролизованной), и пережжёной древесины (то есть золы)). И только внедрение пиролиза в стальных ретортах с водяным замком позволило получать гарантированно качественный уголь, при этом лучшими сортами древесины для получения угля считались бук, граб, дуб для тяжёлых углей и береза в смеси с осиной для лёгких. В зависимости от наличия древесины той или иной породы в данной местности и развития производства угля формировались национальные требования и особенности производства чёрного пороха, поскольку именно качество древесины и степень обжига угля в значительной степени определяют качество пороха.
Малоизвестные факты о получении порохового состава | Исторические Сражения
К началу XX века черный порох уже устарел и массово заменялся бездымными составами. Но это время одновременно являлось и пиком совершенства старого рецепта – большего разнообразия составов, вероятно, не было за всю почти тысячелетнюю история этого вещества. Если обратиться к страницам справочника «Наука и техника» 1912 года, то можно найти рецептуру как минимум десятка сортов пороха (минный, английский охотничий, английский военный, французский, русский, американский, немецкий и т. д.). И никак не меньше упоминаний других сортов, различающихся пропорциями основных компонентов и способом их производства. Потому что именно эти вещи сильно влияли на характеристики конечного состава.
Как известно, дымный порох относится к смесям. Причем для создания требуется всего три компонента: сера, селитра, древесный уголь. И все время активного применения такого пороха шел поиск оптимальной технологий получения этих компонентов. И потому различался, порой, в разных странах по качеству порох сильно – из-за доступа к разным ресурсам и умении ими воспользоваться.
С серой все более-менее просто. Ее научились добывать в чистом виде еще в античности и особых затруднений ее получение ни у кого не вызывало. А вот с углем и селитрой пришлось повозиться.
Черный порох сильно засоряет канал ствола. И больше всего в этом участие принимает уголь. И для уменьшения этой напасти приходилось неустанно заботиться о его чистоте и качестве.
Добыча древесного угля в XIX веке. Рисунок из французского журнала «La Science iIlustrée»На первых порах в ход шел тот уголь, которым получалось разжиться у обычных углежогов. Но оказалось, что в нем или содержатся различные смолы, совсем лишние в зелейном деле, или он недостаточно обожжен, отчего порох горит замедленно. И начались поиски оптимального исходного материала и режимов обжига. В результате практически каждая страна обзавелась своей методой, довольно тщательно охраняемой от посторонних.
Но оказалось, что в нем или содержатся различные смолы, совсем лишние в зелейном деле, или он недостаточно обожжен, отчего порох горит замедленно. И начались поиски оптимального исходного материала и режимов обжига. В результате практически каждая страна обзавелась своей методой, довольно тщательно охраняемой от посторонних.
Во многих странах на пороховой уголь пережигали крушину. Высоко котировалась ольха и ива. Иные растения шли в ход целиком, от других брали только сердцевину.
Сначала наловчились обжигать в герметичных ретортах, потом додумались их вращать – для равномерного прогрева. В результате уголь стал у всех более-менее схожий по качеству. А вот с селитрой хлопот вышло больше всех – уж сильно много ее требовалось.
Когда в Чили открыли огромные залежи селитры, за обладание ими толкались многие участники мировой политической арены. А вот до той поры приходилось довольствоваться месторождением в Египте. А то и вовсе получать ее самостоятельно. Беда в том, что технологией ее синтеза никто тогда не обладал, а получали это стратегическое вещество… из навоза и мочи.
Процесс выглядел примерно так: в кучу требовалось свалить массу фекалий и хорошенько полить их мочой. А потом ждать, пока это все перегниет. Желательно защитив от дождя – чтобы накопленное сырье не ушло в почву. Как только этот компост перегнивал, в нем образовывалась селитра. Чтобы ее получить в чистом виде, эту почву кипятили, и полученный настой сливали и пускали в переработку. Путем нехитрых хлопот получали уже чистую селитру. И в целом выглядело все несложно, вот только для получения тонны пороха требовалось освоить тонн 40 – 50 навоза. И где набраться столь ценного сырья в промышленных масштабах – еще та задачка для логистики той поры.
Конечно, можно было каким-то образом договориться с ассенизаторами, занятыми очисткой выгребов и вывозом отходов за город. Это в теории. А на практике эти санитарные службы если и существовали, то работали не очень эффективно. Многие домовладельцы старались экономить, отчего предпочитали мириться с переполненными ямами, а не отдавать деньги за то, что вроде бы и не относится к жизненно важным расходам.
Чтобы как-то противодействовать подобной беде, англичане в XVII столетии создали особую государственную службу. Представители производителей селитры имели право досмотра выгребных ям любого британца, независимо от происхождения. То есть они следили за опорожнением выгребных ям и собирали по утрам мочу – ту специально выставляли за дверь в специальных сосудах. Так что на улицах рано утром бидонами гремели не одни молочники…
В ряды этих чиновников, крепко нелюбимых и презираемых населением, набирались отбросы общества – нередко довольно мелочная и агрессивная публика. С такой предпочитали не ссориться. Правда, и на порог пускали только по принуждению. Сохранились свидетельства, что их презирали даже нищие. Но все же, служба работала неплохо, так что пороха хватило и на правление Стюартов, и на гражданскую войну впоследствии.
Вакуумный насос для сбора «ночных удобрений» (так их именовали в Англии). Из журнала «The Practical Magazine», Лондон, 1874 годФранцузы вспомнили о практике соседей во времена Наполеоновских войн, когда многочисленные их противники устроили блокаду, отчего рушащаяся империя стала испытывать серьезную нехватку селитры. И отбор мочи и содержимого выгребов организовали не только в крупных городах, но и в самой захолустной сельской местности. А для перегноя этого добра выделили немалые земельные площади. Собственно, часть таких участков были выделены еще при Людовиках, но Бонапарт к ним прибавил примерно столько же – пушкам требовалось стрелять.
Отходы жизнедеятельности укладывались в огромные кучи и хорошенько укутывались (примерно как нынешний силос), чтобы хоть как-то ускорить процесс разложения и образования селитры. Собственно, задолго до этого искусственно получать селитру научился химический гений Глаубер, но его метод никак не годился для серьезных объемов из-за общей дороговизны. Оттого и благоухали под Парижем огромные пирамиды нечистот. А по домам горожан ходили имперские чиновники, интересуясь пищеварением.
× Поддержите подпиской наш телеграм-канал: @battlez
Любопытно, но до открытия в начале ХХ столетия норвежской технологии синтеза селитры, страны, не имевшие доступа к запасам Южной Америки, так и обходились проверенными навозными кучами. Ну а под Парижем и сегодня водят туристов на поля, где когда-то получали стратегическое сырье.
Ну а под Парижем и сегодня водят туристов на поля, где когда-то получали стратегическое сырье.
Обязательно делитесь статьей и ставьте «пальцы вверх», если она вам действительно понравилась!
И не забывайте подписываться на канал — так вы не пропустите выход нового материала
К слову о порохе — Статьи об оружии и боеприпасах
Начиная с XIV века (по крайней мере, среди европейских народов) порох безусловно был и по-прежнему остается основным метательным зарядом любого огнестрельного оружия, независимо от системы и ее мест в истории. Бездымный нитропорох создан сравнительно недавно. До этого все огнестрельное оружие работало на дымном порохе.
Достоинства черного пороха в том, что он прост в изготовлении, относительно дешев, может храниться в годном состоянии хоть сто лет, только бы не отсырел, хорошо отмеривается меркой и нагар от него не сильно вредит стволу. Из недостатков: отсырев, портится и уже не восстанавливает своих качеств после сушки, сильно пачкает стволы и механизмы ружья, так что бой дробью, а в особенности пулей, после нескольких выстрелов заметно ухудшается, но недостатки не идут ни в какой счет с преимуществами.
Дымный порох — это смесь селитры, угля и серы. В его состав входит 75% калиевой селитры, 15% угля и 10% серы. Назначение этих составляющих следующее: селитра дает кислород для сжигания горючего угля, сера цементирует всю смесь. Кроме того, сера, обладая более низкой температурой воспламенения, чем уголь, ускоряет процесс воспламенения пороха. В XVIII-XIX веках процентное содержимое пороха в разных странах-производителях было различно. В Англии законодательно утвердили, что выпускающийся в стране порох содержит 75 частей селитры, 15 частей древесного угля и 10 частей серы. В Бельгии и Франции постановили, что в порохе должно быть 75% селитры и по 12,5% древесного угля и серы. В Австрии и Германии соотношение было: 76 частей селитры, 14 частей древесного угля и 10 частей серы. В процессе производства пороха из экономических соображений содержание селитры снижалось до минимума.
Дымный охотничий порох должен обладать следующими качествами:
- Зерна хорошо полированы;
- Цвет зерна — черный или слегка коричневый;
- При осторожном раздавливании зерна, оно не обращается полностью в порошок, а лишь раскалывается на части;
- При рассмотрении частей зерна в лупу 5-10-кратного увеличения не должно обнаруживаться белого налета выкристаллизовавшихся зерен селитры или желтоватых крошек серы и других посторонних примесей;
- При пересыпании пороха не должно быть слежавшихся комков и пороховой пыли.
Черный порох выпускается четырех градаций размера зерна. Каждый размер отмечен номером или символом.
- Швейцарские пороха идут от №1 (самый мелкий) до №4 (мушкетный с большими гранулами).
- В мире чаще используют буквенный идентификатор F(Fine). Спортивный мелкий порох FFFFg идеально подходит для пистолетов и револьверов калибра 0,31.
- FFFg предназначен для пистолетов, револьверов и винтовок до 0,45 калибра. Чаще всего на соревнованиях используют именно этот порох.
- Для винтовок от 0,45 калибра и выше используют FFg.
- Fg — мушкетный и артиллерийский порох.
- Для стрельбы из гладкоствольного оружия 12 калибра идеален порох FFg а также можно использовать и FFFg.
Дымный порох при сгорании дает 42-44% (по весу) газообразных продуктов, остальные 56-58% приходятся на твердые остатки в виде облака дыма и нагара в канале ствола.
Соотношение маркировок швейцарских и американских порохов:
- Swiss N1 — FFFFg
- Swiss N2 — FFFg
- Swiss N3 — FFg
- Swiss N4 — 1,5Fg
- Swiss N5 — Fg
Всем хороши импортные пороха: и стабильные, и размер зерна у них одинаковый для всей партии, и выбор производителей большой… Поскольку пока не завозят эти чудо-пороха к нам, остановимся на отечественном, хоть он больше похож на крупный артиллерийский с примесями более мелких номеров пороха. В одной банке может встречаться порох нескольких размеров зерна — ни о какой стабильности горения и ровности осыпи заряда речь идти не может. Если ваше ружье сможет стрелять на этом порохе – уже хорошо. Стрельба из дульнозарядного оружия только начинает вновь завоевывать просторы России. Искренне надеемся, что это движение поддержат производители пороха.
В одной банке может встречаться порох нескольких размеров зерна — ни о какой стабильности горения и ровности осыпи заряда речь идти не может. Если ваше ружье сможет стрелять на этом порохе – уже хорошо. Стрельба из дульнозарядного оружия только начинает вновь завоевывать просторы России. Искренне надеемся, что это движение поддержат производители пороха.
Отечественные пороховые заводы имеют долгую и славную историю. Ау-у-у! Где вы?.. А пока что в ожидании возобновления выпуска высококачественного дымного пороха используем тот, который есть. Главное – обеспечить мелкий порох для натруски на полку.
Делается это достаточно просто. На лист ватмана высыпаем не более 50 граммов пороха тонким слоем и накрываем вторым листом ватмана. Берем бутылку и раскатываем, как тесто, 1-2 минуты с нажимом примерно 10 кг. Просеиваем пороховую смесь через бабушкино сито для мелкой муки (в идеале через несколько сит с разным размером ячеек) на чистый лист ватмана. Что не просеялось — опять прокатываем, а прошедшее через сито откладываем в баночку для мелкого пороха. При аккуратном ссыпании пороховая пыль остается на шершавом ватмане и затем смывается в унитаз. Использовать ее в зарядах НЕЛЬЗЯ. Наличие в порохе большого количества пороховой пыли иногда является причиной разрыва стволов ружей, т.к. горение пыли происходит быстрее, чем горение зерен пороха. Может произойти резкий скачок давления. Удовлетворительная резкость боя получается в тех случаях, когда дымного пороха по весу взято приблизительно в шесть раз меньше, чем дроби, а отличная резкость бывает, если пороха взять в пять раз меньше, чем дроби.
В этих пределах и приходится искать величину порохового заряда к дульнозарядным ружьям 12 калибра. Различные марки и сорта пороха, различные величины навески и способы заряжания, форма и масса пули — все это переменные в задаче. Отвешиваете заряды для вашего ружья с шагом, скажем в 0,2 г и — милости просим на природу! Можно рассчитывать на бумаге, используя заводские рекомендации, но только эксперименты с целевой стрельбой скажут вам, какой порох лучше подходит для вашего ружья. Понадобится некоторое время, но результат и удовольствие от проделанной работы стоят этих усилий.
Понадобится некоторое время, но результат и удовольствие от проделанной работы стоят этих усилий.
Никакого открытого огня в его присутствии! Ни в каком проявлении. Не курить!
Работать с небольшими порциями пороха, основной объем пороха должен быть удален на значительные расстояния.
Не используйте синтетические материалы или металлы, способные накапливать статическое электричество. Медь, бронза, дерево — лучшие материалы.
Работайте исключительно в защитных очках.
Примите все возможные противопожарные меры.
Соблюдайте последовательность действий.
Храните порох сухим!
Сергей Паункснис
Blackpowder №1, 05-2010
Нитрат калия (калийная селитра или просто селитра)
Нитрат калия (селитра) KNO3.
Отрывок из книги: Головков Б.Ю., Ломакин А.Г., Рейбман Л.А. Калий в прошлом, настоящем и будущем. – Санкт-Петербург: ИПК «НП-Принт», 2001. – 180 с.
Нитрат калия (калийная селитра или просто селитра) KNO3
Селитры — общее название азотнокислых солей щелочных и щелочноземельных металлов. Но если говорят одно слово – селитра (не «натриевая, не «аммиачная»), значит, имеется в виду KNO3.
Это бесцветная соль плотностью примерно 2,1, легко растворимая в воде, с температурой плавления 339 °С. При нагревании выше этой температуры она разлагается, частично выделяя кислород.
В природе образование селитры происходит естественным образом при гниении животных отбросов в присутствии гидроксида или карбоната калия. Это было подмечено еще в средние века, и именно так селитру столетиями получали искусственно. В настоящее время ее производят промышленными способами – взаимодействием хлорида калия с нитратом натрия (например, в Чили, где существуют природные залежи NaNO3), нейтрализацией гидроксида калия азотной кислотой и др.
Селитра – самая знаменитая из всех солей калия, поскольку служит основой дымного (черного) пороха, который в течение 600 лет – с середины XIII до середины XIX века – был единственным взрывчатым веществом, применявшимся в военном деле и в промышленности. Калийная селитра идеально подошла для этой цели, потому что в противоположность натриевой селитре она не гигроскопична, и порох на ее основе при правильном хранении не отсыревает.
Дымный порох – это механическая смесь калийной селитры, серы и древесного угля. Первый известный рецепт изготовления пороха дается в написанной около 1250 г. «Книге огня» Максима Грека: «Возьми один фунт серы, два фунта липового или ивового угля, шесть фунтов селитры. Очень мелко разотри каждое из этих веществ на мраморной доске и смешай». В дальнейшем установился примерно следующий состав дымного пороха: 75% селитры, 10% серы, 15% древесного угля. Густой белый дым, образующийся при сгорании (взрыве) этого пороха, хорошо знакомый охотникам, имевшим с ним дело, а всем остальным – по историческим кинофильмам и батальной живописи, не что иное, как облака мельчайших частиц сульфида калия K2S.
Вследствие своего значения для пороходелия, селитра считалась важнейшим стратегическим материалом. Она стала первым химическим продуктом, производство которого в России было поставлено под государственный контроль (со времен Петра I). «Географический словарь» 1807 г. сообщает: «Немалое употребление в России селитры, а потому и много вываривается оной, и даже отпускается в чужие края ежегодно по нескольку тысяч пудов из одного Петербурга, особливо в мирное для России время. Селитроварни принадлежат большей частию казне». Калийная селитра стала и первым веществом, совершенствованием технологии которого озаботилось непосредственно правительство. В 1810 г. Министерством внутренних дел был объявлен конкурс на разработку высокопроизводительного способа получения селитры./GettyImages-83189380-56cfda653df78cfb37ae0f61.jpg) Первую премию – «золотую медаль во сто червонных – получил за представленных им технологический процесс выдающийся русский химик и минералог, один из основоположников прикладной химии в России академик В.М. Севергин (1765-1826).
Первую премию – «золотую медаль во сто червонных – получил за представленных им технологический процесс выдающийся русский химик и минералог, один из основоположников прикладной химии в России академик В.М. Севергин (1765-1826).
После появления в конце XIX века бездымных порохов на основе органических нитросоединений производство дымного пороха значительно сократилось. Но он не ушел в отставку. Раскаленные твердые частицы в продуктах его сгорания обладают прекрасной воспламеняющей способностью. Поэтому заряды из дымного используют в качестве воспламенителей для основных зарядов труднее разгорающегося бездымного пороха в артиллерийских боеприпасах и даже в некоторых ракетных двигателях. Дымным порохом наполняют огнепроводные («бикфордовы») шнуры. И он всегда будет служить охотникам.
Калийная селитра применяется также в производстве некоторых сортов стекла, служит для получения нитрита калия, который используют при изготовлении красителей, и т.д.
Список источников:
- Головков Б.Ю., Ломакин А.Г., Рейбман Л.А. Калий в прошлом, настоящем и будущем. – Санкт-Петербург: ИПК «НП-Принт», 2001. – 180 с.
- Головков Б.Ю. ОАО «ВНИИГалургии» — 70 лет научно-технической деятельности в становлении и развитии горно-химической промышленности//Обогащение руд. – 2001. — №5. С.45-48.
- Путешествие в страну элементов. М.: Молодая гвардия, 1963. – 368 с.
- Рич В.И. В поисках элементов. – М: Химия, 1985. – 167 с.
- http://stami.org
До недавнего времени считалось, что состав черного пороха в Новое Время и Раннее Новое Время (14-17 века) был неизменен: древесный уголь, сера и селитра, коей считается нитрат калия. Однако не все … — @дневники: асоциальная сеть
среда, 22 ноября 2017
До недавнего времени считалось, что состав черного пороха в Новое Время и Раннее Новое Время (14-17 века) был неизменен: древесный уголь, сера и селитра, коей считается нитрат калия. Однако не все так просто, и сейчас ученые вполне предполагают, что вместо нитрата калия вполне мог использоваться и использовался азотнокислый кальций. Который в те времена…. тоже называли селитрой. Ибо, извините, науки «Химия» не было, а была алхимия, и судили об элементах не по их химическому составу, а по их свойствам. Раз Азотнокислый кальций вполне заменяет нитрат калия в составе пороха — то почему не селитра-то?
Однако не все так просто, и сейчас ученые вполне предполагают, что вместо нитрата калия вполне мог использоваться и использовался азотнокислый кальций. Который в те времена…. тоже называли селитрой. Ибо, извините, науки «Химия» не было, а была алхимия, и судили об элементах не по их химическому составу, а по их свойствам. Раз Азотнокислый кальций вполне заменяет нитрат калия в составе пороха — то почему не селитра-то? Прежэде всего основывается такое мнение на рецепте пороха, дошедшем до нас из немецкой книги Das Feuerwerkbuch, но не только на ней.
Доказательства не настолько бесспорные, чтобы объявить их истиной в последней инстанции, но заставляющие задуматься.
И т.д.
www.academia.edu/10603252/Calcium_Gunpowder
@темы: история оружия
- ← Предыдущая запись
- Следующая запись →
Этот пост будет безвозвратно удален:
Вы уверены в том, что действительно хотите это сделать?
Да Нет
Зарубка на память — George Rooke — LiveJournal
Помнится, вопрос о селитре когда-то задавал
Для изготовления пороха требовались три компонента: калийная селитра, сера и уголь. Основу пороховой смеси составляла калийная селитра, на ее долю приходилось от 65 до 75 процентов. Природная селитра встречалась в виде залежей в Индии, Персии и Египте.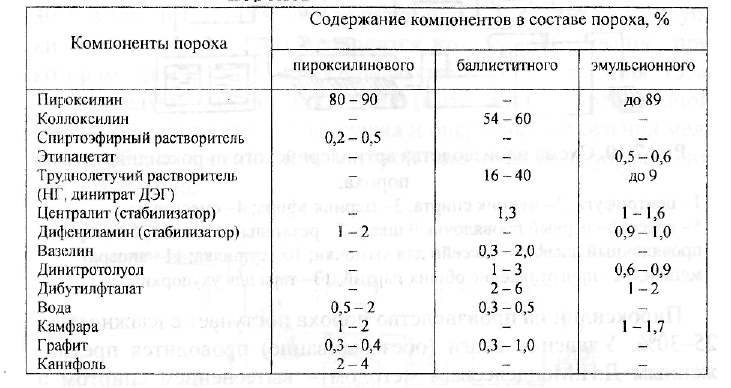 Арабы называли это вещество «китайский снег», византийцы — «индийская соль».
Арабы называли это вещество «китайский снег», византийцы — «индийская соль».
Расход «индийской соли» был настолько велик, а стоимость так высока, что в Европе предпринимались попытки наладить добычу калийной селитры из навоза, фекалий, пищевых отбросов или трупов. Белый кристаллический налет соскабливали со стен пещер, отхожих мест и склепов. Первое сообщение о получении селитры таким способом во Франкфурте относится к 1388 г. {5} Однако длительность процесса образования кристаллов (от 3 до 5 лет) и трудоемкость извлечения готовой селитры, которое требовало до 36 промывок и выпариваний, а главное — ничтожность выхода конечного продукта (около 0,2 %) {6} , заставили алхимиков обратиться к другому способу.
С древних времен алхимики знали, как можно получить «индийскую соль» искусственным путем. Для ее изготовления требовались натриевая (или кальциевая) селитра, квасцы, медный (или железный) купорос и поташ. При нагревании натриевой селитры с медным купоросом и квасцами получали азотную кислоту. Смешивая азотную кислоту и поташ (обычный белый пепел, который остается от сгоревшей древесины), изготавливали калийную селитру.
В Средние века основным источником натриевой и кальциевой селитры являлись соляные промыслы. Селитроносная порода лежит обычно на пласте поваренной соли, ее извлечение производится с помощью кипячения и отстаивания насыщенного соляного раствора. Процесс извлечения натриевой селитры носил название «получение соли из соли» («to make salt upon salt»). Конечный продукт представлял собой белые кристаллы солоноватого вкуса, использовался как для заготовки рыбы или мяса, так и для изготовления калийной селитры.
Принято считать, что итальянские квасцы использовались главным образом в красильном производстве. Однако для протравки тканей требовалось ничтожное количество сырья. Протравочный расствор изготовлялся из расчета 10 грамм квасцов на 1 литр воды {11} . Небольшие залежи квасцов были известны в Италии (Неаполь), Испании (Картахена), Франции (Льеж), Фландрии (Брюгге), Англии (Бристоль). Местная добыча целиком обеспечивала нужды текстильной отрасли. При этом объем ежегодной добычи и продажи итальянских квасцов исчислялся в десятках тысяч кантаров (1 кантар — около 50 кг). То колоссальное количество сырья, которое поставлялось Ватиканом на европейский рынок, свидетельствует, что его основная часть применялась в пороховом деле.
Местная добыча целиком обеспечивала нужды текстильной отрасли. При этом объем ежегодной добычи и продажи итальянских квасцов исчислялся в десятках тысяч кантаров (1 кантар — около 50 кг). То колоссальное количество сырья, которое поставлялось Ватиканом на европейский рынок, свидетельствует, что его основная часть применялась в пороховом деле.
До середины XV в. крупные партии квасцов поступали из Малой Азии, Фракии, Нубии и Аравии через Константинополь, а также с Фокейских рудников, которыми владела Венеция. Расширение производства искусственной калийной селитры позволило поставщикам пороха увеличить объем выхода готового продукта, и к 1410 г. порох подешевел в два раза {12} . Однако искусственная селитра обладала большей гигроскопичностью. Порох слипался в комки, которые приходилось толочь, поэтому природная селитра ценилась выше. Венецианские купцы обманывали покупателей, добавляя искусственную селитру в природный минерал. В 1445 г. в Германии появился трактат с описанием метода, позволявшего определить качество селитры: « Для испытания получаемой из Вененции селитры следует вложить в нее руку, которая по вынутии не должна быть мокра. По вкусу и посредством кристаллизации узнают, есть ли в селитре примесь соли или квасцов».
В то же время, искусственная селитра обладала теми же свойствами, что и природная. Проблему удалось решить после того, как стали применять зернение: в пороховой порошок добавляли небольшое количество вина и протирали полученную тестообразную массу через сито. При этом оказалось, что « два фунта пороха в зернах действуют сильнее, чем три фунта незерненого».К середине XV в. тайна изготовления искусственной калийной селитры из квасцов была разгадана, практически, во всех странах Европы. Порох еще больше подешевел, когда воюющие стороны стали покупать не готовую искусственную калийную селитру, а квасцы и натриевую селитру.
Повышение мощности пороховой смеси и ее удешевление позволило сделать качественный скачок в артиллерии. На полях сражений стали применяться чугунные и свинцовые ядра. Все шире использовалось ручное оружие и «эспаньоли», из которого выстреливали от 5 до 10 пуль, одна за другой. Пушки отливали на специализированных литейных заводах в Германии, Франции и Венгрии.
На полях сражений стали применяться чугунные и свинцовые ядра. Все шире использовалось ручное оружие и «эспаньоли», из которого выстреливали от 5 до 10 пуль, одна за другой. Пушки отливали на специализированных литейных заводах в Германии, Франции и Венгрии.
Угольная шахта с высоким содержанием серы, в которой используются взрывчатые вещества из нитрата аммония — Новости
Угольная шахта с высоким содержанием серы с использованием взрывчатых веществ аммиачной селитры
Угольная шахта с высоким содержанием серы с использованием взрывчатых веществ аммиачной селитры
1. В угольной шахте с высоким содержанием серы с использованием взрывных устройств нитрата аммония концентрацию ионов железа и содержание серы следует измерять до получения порошка сульфидной руды.
2. при содержании серы более 30%, сульфат железа и сульфитный порошок, содержащий железо и концентрацию ионов железа более 0.3% операции в мокрой воде с применением взрывных работ с нитратом аммония, взрывные скважины должны быть очищены порошком; взрывчатое вещество и стенка отверстия не должны находиться в непосредственном контакте с взрывчатыми веществами; если в упаковке не должно быть серных шлаков; заполнение дыры; строго контролируйте время зарядки и количество отверстий.
2. при содержании серы более 30%, сульфата железа и сульфитного порошка, содержащего железо и концентрацию ионов железа более 0,3%, операции перед лицом влажной воды, с использованием взрывного устройства нитрата аммония, взрывное отверстие должно быть очищено порошком; взрывчатое вещество и стенка отверстия не должны находиться в непосредственном контакте с взрывчатыми веществами; если в упаковке не должно быть серных шлаков; заполнение дыры; строго контролируйте время зарядки и количество отверстий.Угольная шахта с высоким содержанием серы с использованием взрывчатых веществ аммиачной селитры
1. В угольной шахте с высоким содержанием серы с использованием взрывных устройств нитрата аммония концентрацию ионов железа и содержание серы следует измерять до получения порошка сульфидной руды.![]()
2. при содержании серы более 30%, сульфата железа и сульфитного порошка, содержащего железо и концентрацию ионов железа более 0,3%, операции перед лицом влажной воды, с использованием взрывного устройства нитрата аммония, взрывное отверстие должно быть очищено порошком; взрывчатое вещество и стенка отверстия не должны находиться в непосредственном контакте с взрывчатыми веществами; если в упаковке не должно быть серных шлаков; заполнение дыры; строго контролируйте время зарядки и количество отверстий.Угольная шахта с высоким содержанием серы с использованием взрывчатых веществ аммиачной селитры
1. В угольной шахте с высоким содержанием серы с использованием взрывных устройств нитрата аммония концентрацию ионов железа и содержание серы следует измерять до получения порошка сульфидной руды.
2. при содержании серы более 30%, сульфата железа и сульфитного порошка, содержащего железо и концентрацию ионов железа более 0,3%, операции перед лицом влажной воды, с использованием взрывного устройства нитрата аммония, взрывное отверстие должно быть очищено порошком; взрывчатое вещество и стенка отверстия не должны находиться в непосредственном контакте с взрывчатыми веществами; если в упаковке не должно быть серных шлаков; заполнение дыры; строго контролируйте время зарядки и количество отверстий.Угольная шахта с высоким содержанием серы с использованием взрывчатых веществ аммиачной селитры
1. В угольной шахте с высоким содержанием серы с использованием взрывных устройств нитрата аммония концентрацию ионов железа и содержание серы следует измерять до получения порошка сульфидной руды.
2. при содержании серы более 30%, сульфата железа и сульфитного порошка, содержащего железо и концентрацию ионов железа более 0,3%, операции перед лицом влажной воды, с использованием взрывного устройства нитрата аммония, взрывное отверстие должно быть очищено порошком; взрывчатое вещество и стенка отверстия не должны находиться в непосредственном контакте с взрывчатыми веществами; если в упаковке не должно быть серных шлаков; заполнение дыры; строго контролируйте время зарядки и количество отверстий.![]()
2. при содержании серы более 30%, сульфата железа и сульфитного порошка, содержащего железо и концентрацию ионов железа более 0,3%, операции перед лицом влажной воды, с использованием взрывного устройства нитрата аммония, взрывное отверстие должно быть очищено порошком; взрывчатое вещество и стенка отверстия не должны находиться в непосредственном контакте с взрывчатыми веществами; если в упаковке не должно быть серных шлаков; заполнение дыры; строго контролируйте время зарядки и количество отверстий. шахта серного угля с использованием взрывчатых веществ нитрата аммония
1.в угольной шахте с высоким содержанием серы, где используются взрывные устройства с нитратом аммония, следует измерять концентрацию ионов железа и содержание серы до порошка сульфидной руды.
2. при содержании серы более 30%, сульфата железа и сульфитного порошка, содержащего железо и концентрацию ионов железа более 0,3%, операции перед лицом влажной воды, с использованием взрывного устройства нитрата аммония, взрывное отверстие должно быть очищено порошком; взрывчатое вещество и стенка отверстия не должны находиться в непосредственном контакте с взрывчатыми веществами; если в упаковке не должно быть серных шлаков; заполнение дыры; строго контролируйте время зарядки и количество отверстий.
ЛУЧШИЕ ТОВАРЫ
Химический чистый нитрат аммония (CPAN)
Нитрат аммония представляет собой белый приллированный кристалл, который имеет сильное влагопоглощение и агломерацию. Он легко взрывается под действием накаливания или детонационного агента. И он легко растворяется в воде, метаноле, ацетате …>
Подробнее >>Пористый приллированный нитрат аммония (PPAN)
При производстве пористого приллированного нитрата аммония (PPAN) используется технология французской компании KT. Продукт характеризуется низким содержанием воды, предотвращением слеживания, высокой прочностью на раздавливание и высоким маслоемкостью a…>
Подробнее >>Мочевина
Мочевина — белое или красное твердое зерно с небольшой щелочью. Он также может подвергаться гидролизу и усадке. Он в основном используется в синтетической смоле, медицине, красителях, красках, продуктах питания, динамите, удобрениях и т. Д.
Он также может подвергаться гидролизу и усадке. Он в основном используется в синтетической смоле, медицине, красителях, красках, продуктах питания, динамите, удобрениях и т. Д.
Нитрат кальция
Нитрат кальция представляет собой бесцветные и прозрачные моноклинальные кристаллы, растворимые в воде, метаноле и этанале и легко впитывающие влагу из воздуха.
Подробнее >>Аммиачная селитра кальция
Это новое азотно-известковое удобрение с характеристиками высокой эффективности и быстрого восполнения азота, применяемое в теплицах и на сельскохозяйственных угодьях большой площади. Улучшает почву и гранулирует почву, делая …>
Подробнее >>Диоксид серы и уголь — Global Energy Monitor
Угольные электростанции являются крупнейшим антропогенным источником диоксида серы, — загрязняющего газа, который способствует образованию кислотных дождей и вызывает серьезные проблемы со здоровьем, особенно из-за его роли в образовании твердых частиц.Уголь естественным образом содержит серу, и при сжигании угля сера соединяется с кислородом с образованием оксидов серы. Хотя естественные процессы, такие как извержения вулканов, биологическое разложение и лесные пожары, также производят диоксид серы, выбросы, вызванные деятельностью человека, намного превышают естественное производство в развитых странах. [1]
По оценкам EPA, более 65%, или более 13 миллионов тонн в год, производства SO 2 в США приходится на электроэнергетические компании, [2] 93 процента из которых производится угольные электростанции. [3] В Китае, крупнейшем в мире потребителе угля, в 2004 году было выброшено около 22,5 миллионов тонн серы, и более 30% территории страны сейчас испытывают кислотные дожди. [4]
Кислотный дождь — это дождь, насыщенный такими химическими веществами, как диоксид серы и оксид азота, который вызывает подкисление озер и ручьев и способствует повреждению деревьев на больших высотах и многих уязвимых лесных почв. Кроме того, кислотные дожди ускоряют разложение строительных материалов и красок, включая незаменимые здания, статуи и скульптуры, которые являются частью культурного наследия нашей страны.Перед падением на землю диоксид серы и оксид азота, а также их производные в виде твердых частиц — сульфаты и нитраты — способствуют ухудшению видимости и наносят вред здоровью населения. [5]
Кроме того, кислотные дожди ускоряют разложение строительных материалов и красок, включая незаменимые здания, статуи и скульптуры, которые являются частью культурного наследия нашей страны.Перед падением на землю диоксид серы и оксид азота, а также их производные в виде твердых частиц — сульфаты и нитраты — способствуют ухудшению видимости и наносят вред здоровью населения. [5]
Воздействие СО на окружающую среду
2Двуокись серы способствует образованию кислотных дождей, которые наносят ущерб лесам, посевам и зданиям, а также подкисляют озера, ручьи и реки, делая их непригодными для водных растений и животных. Продолжительное воздействие SO 2 в течение длительного периода времени может навсегда изменить естественное разнообразие растений и животных в экосистеме. [6] [7] Сульфатные частицы также являются основной причиной смога во многих частях США. [6]
В 2010 году специалисты по растениям, ученые, экологи и владельцы ранчо заявили, что, по их мнению, загрязнение диоксидом серы от угольные электростанции медленно убивают растительность по всему Техасу. Известно, что диоксид серы убивает растительность в других частях страны. В Техасе были зарегистрированы случаи гибели орехов пекан, дубов, вязов и ив. В Центральном Техасе, недалеко от электростанции, находящейся в ведении Управления Нижнего Колорадо, производители орехов пекан говорят, что тысячи деревьев погибли, а производство орехов неуклонно снижается с момента начала работы завода в 1979 году.Посоветовавшись со специалистами, производители считают, что виноваты выбросы диоксида серы. Агентство по охране окружающей среды США посетило некоторые фермы и изучает данные. [8]
Воздействие SO на здоровье
2 Основное воздействие SO2 на здоровье — нарушение функции верхних дыхательных путей. Высокие концентрации диоксида серы могут повлиять на дыхание, вызвать респираторные заболевания и усугубить существующие заболевания сердца и легких. Воздействие в очень низких концентрациях может вызвать раздражение легких и горла и вызвать бронхит. Воздействие низких уровней SO 2 в течение длительного периода снижает способность дыхательной системы защищаться от бактерий и посторонних частиц. [7] К особо чувствительным группам относятся дети, пожилые люди, люди, страдающие астмой, а также люди с заболеваниями сердца или легких. [6]
Воздействие в очень низких концентрациях может вызвать раздражение легких и горла и вызвать бронхит. Воздействие низких уровней SO 2 в течение длительного периода снижает способность дыхательной системы защищаться от бактерий и посторонних частиц. [7] К особо чувствительным группам относятся дети, пожилые люди, люди, страдающие астмой, а также люди с заболеваниями сердца или легких. [6]
Законодательные и нормативные меры США по минимизации выбросов SO
2Закон о чистом воздухе
В 1963 г.Конгресс США принял Закон о чистом воздухе, устанавливающий стандарты для вредных загрязнителей, включая свинец, оксид углерода, озон, диоксид серы, оксид азота и твердые частицы. Законодательство позволило освободить старые электростанции от новых стандартов, поскольку Конгресс предполагал, что эти электростанции будут выведены из эксплуатации. К 1977 году многие штаты не смогли достичь новых целей, и старые заводы продолжали работать, выбрасывая высокие уровни загрязнения. Для решения этих проблем Конгресс принял ряд новых поправок к Закону о чистом воздухе, включая New Source Review (NSR).Это новое законодательство требовало, чтобы старые промышленные предприятия прошли оценку EPA и установили современные технологии контроля загрязнения перед любым расширением. [9]
В 1990 году Конгресс принял дополнительные поправки к Закону о чистом воздухе, включая Раздел IV, в котором решалась проблема кислотных дождей путем ограничения выбросов диоксида серы и оксида азота. Контроль кислотных дождей проводился в два этапа и ограничивал выбросы на несколько лет. [10] В 1990 поправок было спорное положение позволяет компаниям покупать, продавать и торговли загрязнения кредитов, при условии, что они сократить половину их общих выбросов. [11] В 2005 году Агентство по охране окружающей среды США утвердило Межгосударственное правило чистого воздуха, требующее сокращения выбросов диоксида серы на 57 процентов и выбросов оксида азота электростанциями на 61 процент к 2015 году. [12]
[12]
Скрубберы
В результате этих требований многие угольные электростанции установили «скрубберы» дымовых труб, которые улавливают выбросы серы до того, как они попадут в воздух, и превращают их в шлам и твердые отходы. Не только скрубберы дороги, но и отходы побочных продуктов требуют определенных средств удаления.По оценкам Агентства по охране окружающей среды, только 30% этих материалов перерабатывается, чаще всего для производства коммерческих строительных материалов, а остальные 70% вывозятся на свалки. [13] В Огайо, например, Агентство по охране окружающей среды штата недавно одобрило создание полигона для завода FirstEnergy в округе Джефферсон. Ожидается, что на полигоне будет накапливаться от 1,2 млн до 1,6 млн тонн осадка в год. На другую свалку завода AEP в округе Галлия в 2007 году было захоронено 3 миллиона тонн шлама скрубберов и угольной золы. [12]
По данным Управления энергетической информации, следующие доли угольных электростанций мощностью более 100 Компания MW имела в 2005 году скрубберы SO 2 : [14]
| SO 2 Степень удаления | Кол-во растений | Общая вместимость |
|---|---|---|
| Более 90% | 94 | 46 734 МВт |
| 80-89% | 49 | 21 613 МВт |
| 70-79% | 52 | 20,950 МВт |
| 16-69% | 11 | 3825 МВт |
| Нет | 628 | 220 664 МВт |
Возможно, что некоторые угольные электростанции со скрубберами SO 2 не сообщили о своих скрубберах в ОВОС, и, таким образом, приведенная выше таблица завышает количество станций без контроля SO 2 . Однако из 257 угольных электростанций США, выработавших более 2000 ГВтч электроэнергии в 2006 году, 86 имели выбросы SO 2 , превышающие 10 фунтов / МВтч — по сравнению со средним показателем 1 фунт / МВтч для угольных электростанций. с современными скрубберами SO 2 . [15] [16] Мы можем предположить, что эти 86 установок почти наверняка имеют нулевые или крайне минимальные скрубберы SO 2 или имеют скрубберы SO 2 , которые не работали в 2006 году.
Однако из 257 угольных электростанций США, выработавших более 2000 ГВтч электроэнергии в 2006 году, 86 имели выбросы SO 2 , превышающие 10 фунтов / МВтч — по сравнению со средним показателем 1 фунт / МВтч для угольных электростанций. с современными скрубберами SO 2 . [15] [16] Мы можем предположить, что эти 86 установок почти наверняка имеют нулевые или крайне минимальные скрубберы SO 2 или имеют скрубберы SO 2 , которые не работали в 2006 году.
Уголь малосернистый
Альтернативой технологии скруббера является использование угля с низким содержанием серы в качестве топлива для электростанций.По оценкам Министерства энергетики, использование угля с самым низким содержанием серы может привести к сокращению выбросов SO 2 до 85 процентов по сравнению с использованием многих типов угля с более высоким содержанием серы. [17] В США уголь из восточных штатов, включая Огайо, Пенсильванию и Западную Вирджинию, имеет более высокое содержание серы, составляющее от 3 до 10 процентов веса угля; уголь из западных штатов, таких как Вайоминг, Монтана, Юта и Колорадо, может иметь содержание серы менее 1 процента от его веса. [18] Однако уголь с низким содержанием серы значительно дороже угля с более высоким содержанием серы и часто требует дополнительных транспортных расходов. [19] [20] На заводе в Вирджинии Доминион отказался от использования как отечественного угля с низким содержанием серы, так и технологии скрубберов, и вместо этого решил импортировать уголь с низким содержанием серы из Индонезии и Колумбии в качестве менее дорогостоящего способа удовлетворения новых выбросов. стандарты. [21]
Агентство по охране окружающей среды США приближает, что эти меры по соблюдению стандартов выбросов SO 2 обходятся энергетическим компаниям и потребителям от 1 до 2 миллиардов долларов в год, и что эти изменения привели к снижению выбросов SO на 40%. 2 выбросов от уровня 1990 года. [11]
2 выбросов от уровня 1990 года. [11]
Национальные стандарты качества окружающего воздуха
В ноябре 2009 года EPA предложило новые национальные стандарты качества окружающего воздуха для диоксида серы, впервые с 1971 года, когда агентство рекомендовало ужесточить контроль над SO 2 для защиты здоровья населения. Старые пределы измеряли средние значения диоксида серы за 24-часовой и годичный периоды. Новое правило потребует одночасовых измерений, так что всплеск выбросов выше нового предела — от 50 до 100 частей на миллиард за один час — больше не будет приемлемым.По оценкам EPA, если это правило будет введено в действие с самыми строгими ограничениями, рекомендованными агентством, то к 2020 году выгоды будут включать в себя снижение преждевременной смерти на 4700-12000 человек в год и уменьшение количества случаев обострения астмы на 3,6 миллиона. Агентство также подсчитало, что польза для здоровья от новых правил значительно перевесит затраты на 1,8-6,8 миллиардов долларов, связанные с новыми правилами. Общественные слушания запланированы в Атланте на январь 2010 года, а новые правила должны стать окончательными к июню 2010 года. [22]
Новый стандарт был выпущен 3 июня 2010 года. [23]
Транспортное правило
Правило чистого воздушного транспорта — это предлагаемое правило EPA, требующее значительного сокращения выбросов диоксида серы (SO2) и оксидов азота (NOx), которые пересекают границы штата. По оценкам EPA, к 2014 году это правило и другие действия штата и Агентства по охране окружающей среды позволят сократить выбросы SO2 электростанциями на 71 процент по сравнению с уровнями 2005 года, а выбросы NOx — на 52 процента. Предлагаемые правила заменят межгосударственное правило EPA о чистом воздухе 2005 г., которое было отменено в июле 2008 г.C. Окружной суд. Действуя по постановлению федерального суда, администрация Обамы 6 июля 2010 года предложила новые правила качества воздуха для угольных электростанций. Предлагаемое правило потребует сокращения выбросов NOx и SO2 в 2012 году и дополнительных сокращений выбросов SO2 в 2014 году. [24]
Предлагаемое правило потребует сокращения выбросов NOx и SO2 в 2012 году и дополнительных сокращений выбросов SO2 в 2014 году. [24]
21 августа 2012 года федеральный апелляционный суд в Вашингтоне, округ Колумбия, вынес решение 2-1 против Правила транспорта. Суд постановил, что это правило обязывает штаты нести ответственность за загрязнение, которое им не принадлежит, что потенциально делает некоторые штаты ответственными за сокращение загрязнения в других штатах, которое в первую очередь может быть вызвано сторонними государствами.Во-вторых, суд установил, что способ, которым это правило предусматривает обязательства для загрязняющих государств, находится в противоречии с существующими полномочиями в соответствии с Законом о чистом воздухе, поскольку EPA не предоставило штатам первоначальную возможность осуществить необходимые сокращения в пределах своих границ. Двое судей в большинстве были назначены Джорджем Бушем-младшим; раскольник Билла Клинтона. [25]
Стандарты обзора новых источников
16 марта 2011 года Агентство по охране окружающей среды США (EPA) объявило о своих предлагаемых стандартах выбросов, чтобы ограничить ртуть, кислые газы и другие токсичные загрязнения от электростанций. [26]
EPA также предлагает пересмотреть стандарты эффективности New Source Review (NSPS) для электростанций, работающих на ископаемом топливе. В этом документе NSPS будут пересмотрены стандарты, которым должны соответствовать новые угольные и мазутные электростанции в отношении твердых частиц (PM), диоксида серы (SO2) и оксидов азота (NOx). Предлагаемые стандарты должны сократить выбросы ртути от электростанций, сжигающих уголь и нефть, на 91 процент, загрязнение кислого газа на 91 процент, прямые выбросы твердых частиц на 30 процентов и выбросы диоксида серы (SO2) на 53 процента, до 2.1 миллион тонн ежегодных выбросов SO2. [26]
Монетизированная выгода от новых стандартов оценивается в 59–140 миллиардов долларов в год по сравнению с ежегодными расходами на соблюдение требований в размере примерно 10,9 миллиардов долларов. EPA также прогнозирует, что предлагаемые стандарты создадут до 31 000 краткосрочных рабочих мест в строительстве и 9 000 долгосрочных рабочих мест в коммунальных службах. [27]
EPA также прогнозирует, что предлагаемые стандарты создадут до 31 000 краткосрочных рабочих мест в строительстве и 9 000 долгосрочных рабочих мест в коммунальных службах. [27]
Требования новых стандартов включают: [26]
- Для всех существующих и новых работающих на угле и мазуте электрических парогенераторов (EGU) предлагаемые стандарты будут устанавливать количественные пределы выбросов ртути, ТЧ и HCl.
- Для всех существующих и новых EGU, работающих на жидком топливе, предлагаемое правило токсичных веществ будет устанавливать количественные пределы выбросов для общих металлов, HCl и HF.
- Действия, доступные электростанциям для соблюдения пределов выбросов, включают мокрые и сухие скрубберы, системы впрыска сухого сорбента, системы впрыска активированного угля и рукавные фильтры, все это часть технологии максимально достижимого контроля (MACT).
- Предлагаемые стандарты будут устанавливать методы работы вместо численных пределов выбросов для ограничения выбросов органических токсичных веществ в воздух, включая диоксин / фуран, от существующих и новых электростанций, работающих на угле и мазуте.
- Предлагаемые изменения в NSPS будут включать пересмотренные численные пределы выбросов EGU для PM, SO2 и NOX.
Отчеты
В отчете Конгресса от 2011 года Национальной программы оценки кислотных осадков, входящей в состав Министерства внутренних дел США, Геологической службы США, говорится, что по состоянию на 2009 год выбросы SO2 и NOx снизились примерно на две трети по сравнению с уровнями в 1990-е гг. Несмотря на эти сокращения выбросов, в отчете также указывается, что «полное восстановление после кислотных дождей маловероятно для многих уязвимых лесов и водных экосистем.Например, в горах Адирондак в Нью-Йорке, особенно уязвимом регионе, 30 процентов озер в течение 2006-08 гг. Подвергались кислотным дождям, превышающим уровень, необходимый для предотвращения ущерба. Основываясь на моделях, которые анализируют различные сценарии выбросов, в отчете делается вывод о том, что помимо текущих уровней выбросов SO2 и NOx, будущие сокращения выбросов, вероятно, будут способствовать дополнительному и более широкому восстановлению, а также предотвратят дальнейшее подкисление в некоторых регионах США ». [28]
Основываясь на моделях, которые анализируют различные сценарии выбросов, в отчете делается вывод о том, что помимо текущих уровней выбросов SO2 и NOx, будущие сокращения выбросов, вероятно, будут способствовать дополнительному и более широкому восстановлению, а также предотвратят дальнейшее подкисление в некоторых регионах США ». [28]
Гражданин Действие
Фермеры и производители орехов пекана говорят, что углекислый газ убивает растения
В декабре 2010 года эксперты по растениям, ученые, экологи и владельцы ранчо заявили, что, по их мнению, загрязнение диоксидом серы от угольных электростанций медленно убивает растительность в Техасе, в частности, загрязнение от проекта Fayette Power Project в Техасе.
Известно, что диоксид серы убивает растительность в других частях страны. В Техасе были зарегистрированы случаи гибели орехов пекан, дубов, вязов и ив.
В Центральном Техасе, недалеко от завода в Файетте, производители орехов пекана заявили, что тысячи деревьев погибли, а производство орехов неуклонно снижалось с момента начала работы завода в 1979 году. После консультации с научными экспертами производители утверждали, что выбросы диоксида серы от завода были причиной.
У.S. Агентство по охране окружающей среды в настоящее время изучает данные и, как ожидается, в начале 2011 года ответит на свои выводы. [29]
ресурсов
Список литературы
- ↑ Диоксид серы, Tennessee Valley Authority, по состоянию на апрель 2008 г.
- ↑ Диоксид серы — Что это? Откуда это взялось?, EPA, по состоянию на апрель 2008 г.
- ↑ Электроэнергия из угля, Power Scorecard, по состоянию на апрель 2008 г.
- ↑ «Загрязнение китайским углем отбрасывает глобальную тень», New York Times , 11 июня 2006 г.
- ↑ EPA «Effects of Acid Rain», по состоянию на апрель 2010 г.
- ↑ 6,0 6,1 6,2 Двуокись серы: Воздействие SO 2 на здоровье и окружающую среду, EPA, по состоянию на апрель 2008 г.

- ↑ 7,0 7,1 http://www.pca.state.mn.us/air/emissions/so2.html Двуокись серы (SO2) в Миннесоте], Агентство по контролю за загрязнением Миннесоты, декабрь 1997 г.
- ↑ Рамит Плюшник-Масти, «Фермеры и производители орехов пекана говорят, что угольная электростанция убивает растения», Bloomberg, декабрь.28, 2010.
- ↑ Хронология Закона о чистом воздухе, Фонд защиты окружающей среды, по состоянию на апрель 2008 г.
- ↑ Эффекты Раздела IV Поправок к Закону о чистом воздухе 1990 г. на электроэнергетические компании, Управление энергетической информации, март 1997 г.
- ↑ 11,0 11,1 «Модель ограничения и торговли для сокращения выбросов парниковых газов», San Francisco Chronicle , 3 декабря 2007 г.
- ↑ 12,0 12,1 «Коммунальные предприятия собирают свалки: более жесткие воздушные стандарты отправляют в землю тонны растительного ила и угольной золы», Columbus Dispatch , 14 апреля 2008 г.
- ↑ Остатки сгорания угля и контроль ртути, Промежуточный отчет EPA о контроле за выбросами ртути из угольных электрических котлов, апрель 2002 г.
- ↑ Форма базы данных EIA-767, веб-сайт Управления энергетической информации, 2005 г.
- ↑ Dirty Kilowatts 2007 Report Database, Environmental Integrity Project, по состоянию на май 2008 г.
- ↑ Environmental Integrity Project, «Грязные киловатты: самые загрязняющие электростанции Америки», июль 2007 г., стр. 8.
- ↑ Anuual Energy Outlook 2002 с прогнозами до 2020 г., Министерство энергетики США, январь 2002 г.
- ↑ Очистка угля, Министерство энергетики США, по состоянию на апрель 2008 г.
- ↑ «Теннесси: цены на уголь с низким содержанием серы удваиваются, вслед за газом и нефтью», Chattanooga Times , 30 ноября 2004 г.
- ↑ Исследование тарифов на транспортировку в соответствии с Законом об энергетической политике: Заключительный отчет о транспортировке угля, Управление энергетической информации США, октябрь 2000 г.

- ↑ Dominion выбирает импорт угля вместо скрубберов для завода в Чесапике, Энергетика, 8 декабря 2006 г.
- ↑ Рене Шуф, «EPA предлагает ограничения по диоксиду серы впервые с 1971 года», McClatchy Newspapers, 29 ноября 2009 года.
- ↑ Джон Бродер, «E.P.A. ужесточает пределы содержания двуокиси серы», NY Times, 3 июня 2010 г.
- ↑ EPA «Air Transport», по состоянию на февраль 2011 г.
- ↑ «Транспортное правило EPA» «Разрушено судом», American Spectator, 21 августа 2012 г.
- ↑ 26,0 26,1 26,2 «Информационный бюллетень: предлагаемые стандарты по ртути и токсичности воздуха» EPA, по состоянию на март 2011 г.
- ↑ Джон Уолк, «Немного предыстории нового правила Агентства по охране окружающей среды о ртути и токсичных веществах в воздухе» Grist, 16 марта 2011 г.
- ↑ «Исследование кислотных дождей показывает существенное снижение, но требуется больший прогресс», пресс-релиз Геологической службы США, 19 января 2012 г.
- ↑ «Фермеры и производители орехов пекана говорят, что угольная электростанция убивает растения» Рамит Плюшник-Матси, Business Week, 28 декабря 2010 г.
Внешние статьи
- Заявление об общественном здравоохранении: диоксид серы, Агентство по токсическим веществам и регистру заболеваний, по состоянию на апрель 2008 г.
- Как диоксид серы влияет на образ жизни, EPA, по состоянию на апрель 2008 г.
- «Программа кислотных дождей: отчет о ходе работы за 2005 год», EPA.
- Рынки чистого воздуха — данные и карты, EPA
- «Существующие ограничения и режим торговли для выбросов электростанций, которые« будут отменены »» Обнаженный капитализм, 9 июня 2009 г.
- Документ технической поддержки для программного инструмента оценки воздействия силовой установки, подготовленный Abt Associates для Целевой группы по чистому воздуху, июль 2010 г. (данные о смертности и заболеваемости по штатам — Таблица 37, стр.
 97)
97)
Синтетические сорбенты для удаления диоксид серы в камерах сгорания угля с псевдоожиженным слоем.[25 исх.] (Технический отчет)
Снайдер, Р. Б., Уилсон, В. И., Джонсон, И., и Джонке, А. А. Синтетические сорбенты для удаления диоксида серы в камерах сгорания угля с псевдоожиженным слоем. [25 ссылок] . США: Н. П., 1977.
Интернет. DOI: 10,2172 / 7093385.
Снайдер, Р. Б., Уилсон, В. И., Джонсон, И., & Jonke, A. A. Синтетические сорбенты для удаления диоксида серы в камерах сгорания угля с псевдоожиженным слоем. [25 ссылок] . Соединенные Штаты. https://doi.org/10.2172/7093385
Снайдер Р. Б., Уилсон В. И., Джонсон И. и Джонке А. А. Ср.
«Синтетические сорбенты для удаления диоксида серы в камерах сгорания угля с псевдоожиженным слоем. [25 ссылок]». Соединенные Штаты. https: // doi.org / 10.2172 / 7093385. https://www.osti.gov/servlets/purl/7093385.
@article {osti_7093385,
title = {Синтетические сорбенты для удаления диоксида серы в камерах сгорания угля с псевдоожиженным слоем. [25 ссылок]},
author = {Снайдер, Р. Б. и Уилсон, В. И. и Джонсон, И., и Джонке, А. А.},
abstractNote = {Синтетические сорбенты были исследованы на предмет использования вместо известняка для контроля выбросов SO / sub 2 / в камерах сгорания угля с псевдоожиженным слоем.Исследованы сорбенты, полученные пропиткой пористого оксида алюминия оксидами щелочных или щелочноземельных металлов. Наиболее перспективным сорбентом оказался оксид кальция в оксиде алюминия. Однако реакционная способность этого синтетического сорбента SO / sub 2 / была ниже, чем у умеренно реактивного известняка. Следовательно, для соответствия стандартам выбросов SO / sub 2 / потребуется большее количество синтетического сорбента. Устойчивость к истиранию у этого синтетического сорбента выше, чем у натуральных камней; следовательно, можно ожидать большего количества циклов использования.Подсчитано, что использование этого синтетического сорбента уменьшит количество сорбента отходов примерно до одной шестой от количества, ожидаемого при использовании умеренно реактивного прямоточного известняка. Стоимость использования этого синтетического сорбента, по оценкам, примерно в три с половиной раза выше стоимости, ожидаемой при использовании прямоточного известняка. Эта стоимость считается слишком большой ввиду ожидаемого умеренного снижения воздействия на окружающую среду. Синтетические сорбенты, разработанные в этом исследовании, поэтому не считаются жизнеспособной альтернативой известняку в камерах сгорания угля с псевдоожиженным слоем.},
Следовательно, для соответствия стандартам выбросов SO / sub 2 / потребуется большее количество синтетического сорбента. Устойчивость к истиранию у этого синтетического сорбента выше, чем у натуральных камней; следовательно, можно ожидать большего количества циклов использования.Подсчитано, что использование этого синтетического сорбента уменьшит количество сорбента отходов примерно до одной шестой от количества, ожидаемого при использовании умеренно реактивного прямоточного известняка. Стоимость использования этого синтетического сорбента, по оценкам, примерно в три с половиной раза выше стоимости, ожидаемой при использовании прямоточного известняка. Эта стоимость считается слишком большой ввиду ожидаемого умеренного снижения воздействия на окружающую среду. Синтетические сорбенты, разработанные в этом исследовании, поэтому не считаются жизнеспособной альтернативой известняку в камерах сгорания угля с псевдоожиженным слоем.},
doi = {10.2172 / 7093385},
url = {https://www.osti.gov/biblio/7093385},
journal = {},
number =,
объем =,
place = {United States},
год = {1977},
месяц = {6}
}
Взрывчатое вещество | химический продукт | Britannica
История черного пороха
Возможно, никогда не будет достоверно известно, кто изобрел первое взрывчатое вещество, черный порох, который представляет собой смесь селитры (нитрата калия), серы и древесного угля (углерода).По общему мнению, он возник в Китае в 10 веке, но его использовали почти исключительно в фейерверках и сигналах. Возможно, что китайцы также использовали черный порох в бомбах в военных целях, и есть письменные записи, что в середине 13 века они помещали его в бамбуковые трубки для метания каменных снарядов.
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишись сейчас Однако есть некоторые свидетельства того, что арабы изобрели черный порох. Примерно к 1300 году они разработали первое настоящее ружье, бамбуковую трубку, усиленную железом, которая использовала заряд черного пороха для стрельбы.
Примерно к 1300 году они разработали первое настоящее ружье, бамбуковую трубку, усиленную железом, которая использовала заряд черного пороха для стрельбы.
Также можно привести веские доводы в пользу того, что черный порох был обнаружен английским средневековым ученым Роджером Бэконом, который в 1242 году написал подробные инструкции по его приготовлению в странной форме латинской анаграммы, которую трудно расшифровать. Но Бэкон читал по-арабски, и, возможно, он черпал свои знания из арабских источников.
Некоторые ученые приписывают изобретение огнестрельного оружия немецкому монаху начала XIV века по имени Бертольд Шварц.В любом случае они часто упоминаются в рукописях XIV века из многих стран, и есть запись о доставке оружия и пороха из Гента в Англию в 1314 году.
Только в 17 веке черный порох использовался в мирных целях. Существует сомнительное утверждение, что он использовался в горнодобывающих предприятиях в Германии в 1613 году, и достаточно достоверные свидетельства того, что он использовался на рудниках Шемница, Венгрия (современная Банска-Штьявница, Чехословакия), в 1627 году. По разным причинам, таким как высокая стоимость , отсутствие подходящих бурильных орудий и страх обрушения кровли, использование черного пороха в горнодобывающей промышленности не получило быстрого распространения, хотя к 1700 году оно было широко распространено.Первое применение в области гражданского строительства было в туннеле Мальпас на Южном канале во Франции в 1679 году.
В течение 300 лет неизменный состав черного пороха составлял примерно 75 процентов селитры (нитрата калия), 15 процентов древесного угля и 10 процентов серы. Первоначально селитру добывали из компостных куч и отходов животноводства. Месторождения, обнаруженные в Индии, служили источником на многие годы. В 1850-х годах в Чили были обнаружены огромные количества нитрата натрия, и селитра образовалась в результате реакции с хлоридом калия, которого было много.
Чилийский нитрат сначала не считался подходящим для производства черного пороха, поскольку он слишком легко впитывает влагу. Ламмот дю Пон, американский промышленник, решил эту проблему и начал производить порошок нитрата натрия в 1858 году. Он стал популярным за короткое время, потому что, хотя он не давал такого высокого качества взрывчатого вещества, как нитрат калия, он подходил для большинства горнодобывающих и строительных приложений и было намного дешевле. Чтобы различать их, версии нитрата калия и нитрата натрия стали известны как взрывчатые порошки A и B соответственно.Порох A продолжал использоваться для специальных целей, которые требовали его более высокого качества, в основном для огнестрельного оружия, военных устройств и предохранителей.
Ламмот дю Пон, американский промышленник, решил эту проблему и начал производить порошок нитрата натрия в 1858 году. Он стал популярным за короткое время, потому что, хотя он не давал такого высокого качества взрывчатого вещества, как нитрат калия, он подходил для большинства горнодобывающих и строительных приложений и было намного дешевле. Чтобы различать их, версии нитрата калия и нитрата натрия стали известны как взрывчатые порошки A и B соответственно.Порох A продолжал использоваться для специальных целей, которые требовали его более высокого качества, в основном для огнестрельного оружия, военных устройств и предохранителей.
Стандартные методы определения содержания серы в золе угля и кокса (Журнальная статья)
. Стандартные методы определения содержания серы в золе угля и кокса . США: Н. П., 1980.
Интернет.
. Стандартные методы определения содержания серы в золе угля и кокса . Соединенные Штаты.
. Вт.
«Стандартные методы испытаний серы в золе угля и кокса». Соединенные Штаты.
@article {osti_6448990,
title = {Стандартные методы испытаний серы в золе угля и кокса},
author = {},
abstractNote = {Эти методы охватывают три необязательные гравиметрические процедуры для определения серы в угле или коксовой золе, полученной в соответствии с методом D 2795 или D 3174.Содержание серы указывается как SO / sub 3 /. Метод A: модифицированный британский метод, образец подготовленной угольной золы переваривается в кипящем разбавленном растворе соляной кислоты, к которому добавляется бромная вода, чтобы гарантировать, что вся сера окисляется до сульфатной формы. После нейтрализации и осаждения железа гидроксидом аммония смесь фильтруют и сульфат в фильтрате определяют гравиметрически как сульфат бария. Метод B: смесь Eschka, образец подготовленной угольной или коксовой золы и смесь Eschka вместе воспламеняют на воздухе.Сульфаты растворяют в горячей воде и отделяют от нерастворенного остатка золы и оксида магния фильтрованием. Сульфат в фильтрате определяется гравиметрически как сульфат бария. Метод C: метод плавления карбоната натрия, образец подготовленного угля или коксовой золы смешивают с карбонатом натрия и нитратом калия и плавят в платиновом тигле. Смесь охлаждают, переваривают в горячей воде и фильтруют. Сульфат в фильтрате определяется гравиметрически как сульфат бария.},
После нейтрализации и осаждения железа гидроксидом аммония смесь фильтруют и сульфат в фильтрате определяют гравиметрически как сульфат бария. Метод B: смесь Eschka, образец подготовленной угольной или коксовой золы и смесь Eschka вместе воспламеняют на воздухе.Сульфаты растворяют в горячей воде и отделяют от нерастворенного остатка золы и оксида магния фильтрованием. Сульфат в фильтрате определяется гравиметрически как сульфат бария. Метод C: метод плавления карбоната натрия, образец подготовленного угля или коксовой золы смешивают с карбонатом натрия и нитратом калия и плавят в платиновом тигле. Смесь охлаждают, переваривают в горячей воде и фильтруют. Сульфат в фильтрате определяется гравиметрически как сульфат бария.},
doi = {},
url = {https: // www.osti.gov/biblio/6448990},
journal = {Анну. Книга ASTM Stand .; (США)},
number =,
объем = 26,
place = {United States},
год = {1980},
месяц = {1}
}
8,7. Выбросы оксидов азота (NOx)
8.7. Выбросы оксидов азота (NOx)
NOx относится как к оксиду азота (NO), так и к диоксиду азота (NO 2 ).Последствия выброса слишком большого количества NOx в атмосферу для окружающей среды перечислены ниже.
- NOx является основным компонентом образования приземного озона, вызывающего серьезные респираторные проблемы.
- Респираторные проблемы могут возникнуть в результате воздействия NO 2 само по себе, но также вызывает беспокойство реакция NOx с образованием переносимых по воздуху частиц нитрата или кислотных аэрозолей, которые имеют аналогичные эффекты.
- Наряду с оксидами серы (SOx) NOx способствует образованию кислотных дождей и вызывает широкий спектр экологических проблем.
- NOx может ухудшить качество воды из-за перегрузки воды питательными веществами, вызывая переизбыток водорослей.
- Атмосферные азотсодержащие частицы ухудшают видимость.

- NOx может реагировать с образованием закиси азота (N 2 O), которая является парниковым газом и способствует глобальному потеплению.
Уголь обычно содержит от 0,5 до 3 процентов азота в пересчете на сухой вес. Азот, содержащийся в угле, обычно имеет форму ароматических структур, таких как пиридины и пирролы.Гибкость исходного сырья при газификации позволяет варьировать содержание азота в угле в широком диапазоне.
Во время газификации большая часть азота в угле превращается в безвредный газообразный азот (N 2 ), который составляет значительную часть атмосферы. Однако образуются небольшие количества аммиака (NH 3 ) и цианистого водорода (HCN), которые необходимо удалять в процессе охлаждения синтез-газа. Поскольку и NH 3 , и HCN растворимы в воде, это простой процесс.
В процессах, основанных на газификации угля, NOx может образовываться ниже по потоку за счет сжигания синтез-газа с воздухом в газовых турбинах, производящих электричество. Однако известные методы контроля образования NOx сводят эти уровни к минимуму и приводят к выбросам NOx значительно ниже, чем те, которые связаны с другими технологиями производства электроэнергии на угле, как показано на следующем рисунке.
Контроль выбросов NOx
Хотя выбросы NOx от действующих электростанций IGCC довольно низкие, как показано выше, более строгие правила могут потребовать контроля до уровней всего 3 ppm в дымовом газе парогенератора-утилизатора (HRSG).Ниже приводится обзор методов контроля NOx как на основе сжигания, так и после сжигания, используемых для контроля выбросов NOx.
Контроль NOx в турбине
Доступные варианты контроля NOx на основе сжигания для турбин, работающих на синтез-газе, более ограничены, чем для турбин, работающих на природном газе. Так называемая технология Lean-Premix 1 , которая позволяет последней достичь выбросов всего 9 ppm (при 15% O 2 ), не применима к газовым турбинам IGCC. Источником проблемы являются различия между составом синтез-газа и природного газа и характеристиками горения.Синтез-газ, полученный в результате газификации, отличается от природного газа теплотворной способностью, составом газа, характеристиками воспламеняемости и загрязнителями. Установка IGCC с продувкой кислородом и увлеченным потоком обычно производит синтез-газ с теплотворной способностью от 250 до 400 БТЕ / фут 3 (на основе ВТС), что значительно ниже, чем 1000 БТЕ / фут 3 для природного газа. . Это приводит к значительному увеличению расхода по сравнению с природным газом (на ~ 14% больше), что связано с необходимостью поддерживать заданный подвод тепла к камере сгорания.Кроме того, в то время как горючий состав природного газа состоит в основном из метана (CH 4 ), горючими компонентами синтез-газа являются монооксид углерода (CO) и водород (H 2 ), с соотношением H 2 / CO, обычно в диапазоне От 0,6 до 0,8 2 . По сравнению с природным газом компонент синтез-газа H 2 имеет более высокую скорость пламени и более широкие пределы воспламеняемости. Последнее означает, что синтез-газ должен иметь стабильное пламя при более бедных условиях, чем природный газ, в то время как первый указывает на то, что кинетика (скорость химической реакции) горения H 2 намного быстрее, чем у природного газа.Такая очень высокая скорость пламени водородного компонента синтез-газа препятствует использованию технологии обедненного премикса. Наконец, синтез-газ, полученный в результате газификации угля, вероятно, будет содержать более высокие концентрации H 2 S, чем природный газ, что может повлиять на технологии контроля выбросов NOx после сжигания.
Источником проблемы являются различия между составом синтез-газа и природного газа и характеристиками горения.Синтез-газ, полученный в результате газификации, отличается от природного газа теплотворной способностью, составом газа, характеристиками воспламеняемости и загрязнителями. Установка IGCC с продувкой кислородом и увлеченным потоком обычно производит синтез-газ с теплотворной способностью от 250 до 400 БТЕ / фут 3 (на основе ВТС), что значительно ниже, чем 1000 БТЕ / фут 3 для природного газа. . Это приводит к значительному увеличению расхода по сравнению с природным газом (на ~ 14% больше), что связано с необходимостью поддерживать заданный подвод тепла к камере сгорания.Кроме того, в то время как горючий состав природного газа состоит в основном из метана (CH 4 ), горючими компонентами синтез-газа являются монооксид углерода (CO) и водород (H 2 ), с соотношением H 2 / CO, обычно в диапазоне От 0,6 до 0,8 2 . По сравнению с природным газом компонент синтез-газа H 2 имеет более высокую скорость пламени и более широкие пределы воспламеняемости. Последнее означает, что синтез-газ должен иметь стабильное пламя при более бедных условиях, чем природный газ, в то время как первый указывает на то, что кинетика (скорость химической реакции) горения H 2 намного быстрее, чем у природного газа.Такая очень высокая скорость пламени водородного компонента синтез-газа препятствует использованию технологии обедненного премикса. Наконец, синтез-газ, полученный в результате газификации угля, вероятно, будет содержать более высокие концентрации H 2 S, чем природный газ, что может повлиять на технологии контроля выбросов NOx после сжигания.
Использование разбавителя для понижения температуры пламени, такого как азот или пар, в настоящее время является предпочтительным методом минимизации образования NOx из турбины, работающей на синтез-газе. Азот обычно поступает из криогенной установки разделения воздуха, поэтому его можно удобно использовать в процессе IGCC. Этот метод контроля может снизить уровни выбросов NOx от турбин, работающих на синтез-газе, примерно до 15 частей на миллион (при 15% O 2 ). General Electric (GE) в настоящее время нацелена на разработку камер сгорания для надежного достижения уровня NOx ниже 10 ppm с синтез-газом, что было бы сопоставимо с уровнями выбросов NOx, достигаемыми за счет использования технологии обедненного предварительного смешения на газовых турбинах, работающих на природном газе.
Этот метод контроля может снизить уровни выбросов NOx от турбин, работающих на синтез-газе, примерно до 15 частей на миллион (при 15% O 2 ). General Electric (GE) в настоящее время нацелена на разработку камер сгорания для надежного достижения уровня NOx ниже 10 ppm с синтез-газом, что было бы сопоставимо с уровнями выбросов NOx, достигаемыми за счет использования технологии обедненного предварительного смешения на газовых турбинах, работающих на природном газе.
Контроль NOx после сжигания
Единственные доступные в настоящее время методы для достижения однозначных концентраций NOx требуют обработки дымовых газов для снижения NOx до азота.Селективное каталитическое восстановление (СКВ) — это полностью коммерческая технология, которая была применена к турбинам, работающим на природном газе, для минимизации выбросов NOx, в то время как процесс EMx (SCONOx ™) представляет собой новую технологию, не основанную на аммиаке, которая конкурирует с СКВ.
Селективное каталитическое восстановление (SCR)
Технология SCR обычно считается лучшей доступной дополнительной системой контроля NOx для стационарных турбин внутреннего сгорания, работающих на природном газе или мазуте, а также является кандидатом для использования в IGCC. SCR выборочно снижает выбросы NOx, впрыскивая NH 3 в выхлопные газы перед катализатором.NOx реагирует с NH 3 и O 2 с образованием N 2 и H 2 O, в основном в соответствии со следующими уравнениями:
4NH 3 + 4NO + O 2 → 4N 2 + 6H 2 O
4NH 3 + 2NO 2 + O 2 → 3N 2 + 6H 2 O
Активная поверхность катализатора обычно представляет собой благородный металл, оксид основного металла (титана или ванадия) или материал на основе цеолита.Катализаторы на основе металлов обычно наносятся в виде покрытия на металлическую или керамическую подложку, тогда как цеолитные катализаторы обычно представляют собой гомогенный материал, который образует как активную поверхность, так и подложку. Геометрическая конфигурация корпуса катализатора рассчитана на максимальную площадь поверхности и минимальное препятствие на пути потока дымовых газов, чтобы максимизировать эффективность преобразования и минимизировать противодавление на турбину. Самая распространенная конфигурация — монолитная, «сотовая» конструкция. Важным фактором, влияющим на производительность SCR, является рабочая температура.Катализаторы из недрагоценных металлов имеют диапазон рабочих температур для применения в чистом топливе приблизительно от 400 ° до 800 ° F. Верхний диапазон этого температурного окна может быть увеличен с использованием цеолитного катализатора максимум до 1100 ° F. Из-за требуемого диапазона рабочих температур для обычного катализатора СКВ (600-750 ° F) интеграция в ПГРТ обычно требует разделения секции испарителя (или котла) высокого давления для размещения слоя катализатора СКВ и оборудования для впрыска аммиака.
Геометрическая конфигурация корпуса катализатора рассчитана на максимальную площадь поверхности и минимальное препятствие на пути потока дымовых газов, чтобы максимизировать эффективность преобразования и минимизировать противодавление на турбину. Самая распространенная конфигурация — монолитная, «сотовая» конструкция. Важным фактором, влияющим на производительность SCR, является рабочая температура.Катализаторы из недрагоценных металлов имеют диапазон рабочих температур для применения в чистом топливе приблизительно от 400 ° до 800 ° F. Верхний диапазон этого температурного окна может быть увеличен с использованием цеолитного катализатора максимум до 1100 ° F. Из-за требуемого диапазона рабочих температур для обычного катализатора СКВ (600-750 ° F) интеграция в ПГРТ обычно требует разделения секции испарителя (или котла) высокого давления для размещения слоя катализатора СКВ и оборудования для впрыска аммиака.
Решетка для впрыска аммиака, предназначенная для равномерного распределения аммиака в потоке выхлопных газов, расположена перед корпусом катализатора.В типичной системе впрыска аммиака безводный аммиак забирается из резервуара для хранения и испаряется с помощью испарителя с паровым или электрическим подогревом. Пар смешивается с сжатым газом-носителем, чтобы обеспечить как достаточный импульс через форсунки, так и эффективное смешивание аммиака с дымовыми газами. Газ-носитель обычно представляет собой сжатый воздух или пар, а концентрация аммиака в газе-носителе составляет около 5 процентов. Альтернативой безводному аммиаку является использование водного аммиака.Пониженная концентрация аммиака в водном растворе снижает проблемы безопасности, связанные с безводным аммиаком.
Отношение NH 3 : NOx можно изменять для достижения желаемого уровня снижения NOx. Требуется один моль аммиака для восстановления одного моля NO и два моля аммиака для восстановления одного моля NO 2 . Более высокие отношения NH 3 : NOx позволяют добиться более высоких сокращений выбросов NOx, но могут привести к увеличению выбросов непрореагировавшего аммиака в атмосферу. Этот непрореагировавший аммиак известен как проскок аммиака. Катализаторы SCR со временем разлагаются, что изменяет количество проскальзывания NH 3 . Срок службы катализатора обычно составляет от 3 до 10 лет в зависимости от конкретного применения. Применение IGCC с выхлопным газом, который относительно не содержит загрязняющих веществ, должно обеспечить значительно более длительный срок службы катализатора, чем при использовании обычного угольного топлива.
Этот непрореагировавший аммиак известен как проскок аммиака. Катализаторы SCR со временем разлагаются, что изменяет количество проскальзывания NH 3 . Срок службы катализатора обычно составляет от 3 до 10 лет в зависимости от конкретного применения. Применение IGCC с выхлопным газом, который относительно не содержит загрязняющих веществ, должно обеспечить значительно более длительный срок службы катализатора, чем при использовании обычного угольного топлива.
Установка SCR в HRSG IGCC, что равносильно полировке NOx, требует учета воздействия проскока аммиака на окружающую среду.Проскальзывание аммиака обычно ограничивается до менее 5 частей на миллион в большинстве применений СКВ, но может быть выше, когда уровень NOx, поступающего в слой катализатора, очень низок. Такая операция может потребовать больше избытка аммиака, чем обычно используется. Хотя найти компромисс между NOx и аммиаком непросто, с качественной точки зрения они оба очень токсичны; оба способствуют образованию мелких частиц сульфата аммония ((NH 4 ) 2 SO 4 ) и нитрата аммония (NH 4 NO 3 ), кислотному осаждению, эвтрофикации и обогащению наземных экосистем азотом. почвы; и оба они в конечном итоге могут быть преобразованы в закись азота (N 2 O), мощный парниковый газ.Кроме того, NOx (как NO 2 ) является хроническим токсином и важным предшественником образования тропосферного озона. Вклад выбросов NOx или аммиака от одного объекта в любую из этих экологических проблем в первую очередь определяется существующими уровнями NOx и аммиака в районе и концентрацией других загрязнителей в атмосфере, которые вступают в реакцию с NOx или NH 3 . Что касается диапазона воздействия или потенциала для переноса на большие расстояния, азотная кислота или органический нитрат (пероксиацетилнитрат, PAN), полученные из выбросов NOx, и аммиак имеют схожие сроки жизни в атмосфере и, таким образом, аналогичный потенциал для переноса на большие расстояния. Однако ПАН и сульфат аммония более долговечны и могут распространять влияние как NOx, так и аммиака на обширную территорию.
Однако ПАН и сульфат аммония более долговечны и могут распространять влияние как NOx, так и аммиака на обширную территорию.
Утилизация солевых отложений и отработанного катализатора также является потенциальной проблемой для окружающей среды. Катализаторы СКВ обычно содержат оксиды тяжелых металлов, таких как ванадий и / или титан, что создает потенциальный риск для здоровья человека и окружающей среды, связанный с обращением с отработанным катализатором и его утилизацией. Пятиокись ванадия, наиболее часто используемый катализатор СКВ, внесена в список особо опасных материалов Агентства по охране окружающей среды.Количество отходов, связанных с СКВ, довольно велико, хотя фактическое количество активного материала в слое катализатора относительно невелико. Это требует использования лицензированных средств транспортировки и утилизации и соблюдения положений Закона о сохранении и восстановлении ресурсов. Вполне возможно, что предприятия в некоторых штатах могут столкнуться с дополнительными расходами из-за необходимости утилизировать эти материалы за пределами штата из-за отсутствия лицензированных предприятий по удалению этих материалов. Эта ответственность может не лежать на заводе, поскольку поставщики катализаторов часто собирают и рециркулируют отработанный катализатор в рамках своего контракта.
Еще одна экологическая проблема, связанная с SCR, — это безопасность труда. Соискателям разрешений необходимо знать, что безопасность аммиака является проблемой, которая сама по себе может уменьшить преимущества использования СКВ для контроля NOx. EPA характеризует аммиак как чрезвычайно опасное вещество, и пары могут образовывать взрывоопасную смесь с воздухом. Положения Закона о безопасности и гигиене труда требуют, чтобы сотрудники предприятий, где используется аммиак, были обучены безопасному использованию аммиака (согласно 29 CRF 1910.120). Предприятия, которые обрабатывают более 10 000 фунтов безводного аммиака или более 20 000 фунтов аммиака в водном растворе с 20-процентным или более высоким содержанием аммиака, должны подготовить план управления рисками (RMP) и реализовать программу управления рисками для предотвращения случайных выбросов. При оценке технологии необходимо учитывать затраты на обучение, соблюдение соответствующих федеральных, государственных и местных правил техники безопасности, а также подготовку и утверждение RMP и плана готовности к чрезвычайным ситуациям. Все это говорит о том, что аммиак широко используется в различных областях, особенно в сельском хозяйстве, и при соответствующей подготовке его можно безопасно обрабатывать и использовать.
При оценке технологии необходимо учитывать затраты на обучение, соблюдение соответствующих федеральных, государственных и местных правил техники безопасности, а также подготовку и утверждение RMP и плана готовности к чрезвычайным ситуациям. Все это говорит о том, что аммиак широко используется в различных областях, особенно в сельском хозяйстве, и при соответствующей подготовке его можно безопасно обрабатывать и использовать.
Установка системы SCR в HRSG завода IGCC имеет два основных воздействия на эксплуатацию. Во-первых, потеря давления в слое катализатора SCR увеличивает противодавление турбины, тем самым снижая выходную мощность газовой турбины примерно на половину процента. Оборудование для хранения и перекачки аммиака потребляет дополнительную мощность. Во-вторых, нежелательные химические реакции могут отрицательно повлиять на работу установки и помешать ей. Хотя оборудование для очистки топливного газа IGCC эффективно удаляет более 95% компонента серы (как H 2 S), остаточная сера в синтез-газе проходит в турбину внутреннего сгорания, где она окисляется до SO 2 и SO 3. .Промежуточный аммиак из процесса SCR может реагировать с SO 3 , образуя соли аммиака, такие как сульфат аммония или бисульфат аммиака. Бисульфат аммония — это очень едкий и липкий материал, который может закупоривать оборудование для теплопередачи, расположенное ниже по потоку, снижая производительность или даже вызывая остановку завода. Дополнительное противодавление, вызванное засорением, также снижает мощность газовой турбины. Сульфат аммония, если он не осаждается вместе с образовавшимся бисульфатом, выбрасывается в атмосферу в виде мелких твердых частиц (PM2.5), поскольку после ПГРТ обычно не устанавливают контроль твердых частиц. Это проблемное поведение представляет собой еще одно важное различие между электростанцией, работающей на природном газе, и электростанцией IGCC.
Чтобы предотвратить образование солей аммиака, проскок аммиака или SO 3 должен быть в значительной степени сведен к минимуму. Поскольку некоторый проскок аммиака неизбежен, поставщики IGCC рекомендуют разрешить максимальный уровень оксида серы 2 ppm для попадания в HRSG с топливным газом. Установка реактора для полировки оксида цинка или активированного угля перед газовой турбиной является одним из методов контроля остаточного SO 2 (с дополнительным преимуществом в виде некоторого дополнительного контроля за ртутью).К сожалению, это еще больше увеличивает паразитное энергопотребление и увеличивает стоимость установки SCR.
Поскольку некоторый проскок аммиака неизбежен, поставщики IGCC рекомендуют разрешить максимальный уровень оксида серы 2 ppm для попадания в HRSG с топливным газом. Установка реактора для полировки оксида цинка или активированного угля перед газовой турбиной является одним из методов контроля остаточного SO 2 (с дополнительным преимуществом в виде некоторого дополнительного контроля за ртутью).К сожалению, это еще больше увеличивает паразитное энергопотребление и увеличивает стоимость установки SCR.
EMx (SCONOx ™) Цикл окисления / абсорбции
Эта каталитическая система дожигания удаляет NOx и CO из выхлопа газовой турбины за счет использования платинового катализатора. В отличие от SCR, здесь не требуется впрыскивание аммиака, а активным реагентом для удаления NOx является карбонат калия. Выхлопные газы из газовой турбины поступают в реактор и реагируют с карбонатом калия, которым пропитывается поверхность платинового катализатора.СО окисляется до СО 2 платиновым катализатором. NO окисляется до NO 2 , а затем вступает в реакцию с покрытием из карбоната калия на катализаторе с образованием нитритов и нитратов калия на поверхности катализатора. Эти химические реакции, показанные ниже, называются «циклом окисления / абсорбции».
CO + ½O 2 → CO 2
NO + ½O 2 → NO 2
CH 2 O + O 2 → CO 2 + H 2 O
2NO 2 + K 2 CO 3 → CO 2 + KNO 2 + KNO 3
Когда карбонат насыщается NOx, его необходимо регенерировать.Диапазон эффективных рабочих температур составляет 280-750 ° F, при этом 500-700 ° F является оптимальным диапазоном для удаления NOx. Оптимальный температурный диапазон примерно такой же, как у SCR. Регенерация катализатора осуществляется путем пропускания разбавленного газа-восстановителя водорода через поверхность катализатора в отсутствие кислорода. Водород реагирует с нитритами и нитратами с образованием воды и элементарного азота. CO 2 в регенерационном газе реагирует с нитритами и нитратами калия с преобразованием карбоната калия.Этот цикл называется «циклом регенерации», как показано ниже.
Водород реагирует с нитритами и нитратами с образованием воды и элементарного азота. CO 2 в регенерационном газе реагирует с нитритами и нитратами калия с преобразованием карбоната калия.Этот цикл называется «циклом регенерации», как показано ниже.
KNO 2 + KNO 3 + 4H 2 + CO 2 → K 2 CO 3 + 4H 2 O + N 2
Водяной пар и элементарный азот выбрасываются в дымовую трубу вместо NOx, а карбонат калия снова присутствует на поверхности катализатора, позволяя циклу окисления / абсорбции возобновиться.
Поскольку цикл регенерации должен происходить в бескислородной среде, катализатор, подвергающийся регенерации, должен быть изолирован от выхлопных газов.Это достигается с помощью набора жалюзи, одна перед регенерируемой секцией, а другая — после нее. Во время цикла регенерации эти жалюзи закрываются и открывается клапан, пропускающий регенерационный газ в секцию. Типичная система SCONOx ™ имеет от пяти до пятнадцати секций катализатора. В любой момент времени восемьдесят процентов этих секций находятся в цикле окисления / абсорбции, а двадцать процентов — в цикле регенерации. Поскольку в цикле регенерации всегда присутствует одно и то же количество секций, производство газа для регенерации происходит с постоянной скоростью.Цикл регенерации обычно длится от трех до пяти минут, поэтому каждая секция находится в цикле окисления / абсорбции от девяти до пятнадцати минут.
Несколько критических проблем, связанных с использованием этой технологии:
- Катализатор очень чувствителен к сере, включая следовые количества, которые обычно присутствуют в выхлопных газах IGCC;
- Надежность движущихся частей с течением времени является проблемой при эксплуатации и техническом обслуживании;
- Использование водорода для регенерации может быть серьезной проблемой с точки зрения безопасности, поскольку его трудно удерживать;
- Проблемы увеличения масштаба для больших газовых турбин;
- SCONOx ™ имеет примерно вдвое больший перепад давления, чем SCR; и
- Первоначальные капитальные затраты примерно в три раза превышают стоимость SCR, хотя они могут снизиться, когда в эксплуатации будет больше систем.

В 1997 году EPA провело мониторинг применения SCONOx ™ на турбине, работающей на природном газе, на Федеральной когенерационной установке в Лос-Анджелесе, где оно установило стандарт 3,5 ppm (при 15% кислорода на 3-часовом скользящем среднем) для NOx. Система управления SCONOx ™ обычно обеспечивает средний уровень выбросов NOx примерно 2 ppmv. Это привело к достижению LAER (наименьшего достижимого уровня выбросов) на уровне 3,5 ppmv, что установило стандарт для будущих технологий контроля для аналогичных объектов в соответствии с Разделом 173 (a) (2) Закона о чистом воздухе.
Район управления качеством воздуха Южного побережья назвал SCONOx ™ лучшей доступной технологией контроля (BACT) для газотурбинных двигателей. Дальнейшее улучшение снижения было подтверждено в 1998 году, когда EPA обнаружило, что показатель LAER для SCONOx ™ составил 2,5 ppmv.
Снижение выбросов NOx после сжигания на объектах IGCC в США
Информация из заявок на получение разрешений / разрешений по недавним проектам IGCC включает уровни выбросов NOx, как показано на сопроводительном рисунке.Обратите внимание, что не все проекты IGCC, в том числе совсем недавно выполненная электростанция на базе Duke Edwardsport IGCC и IGCC округа Кемпер штата Миссисипи Пауэр, требовали внедрения контроля NOx после сжигания, хотя другие, такие как HECA в Калифорнии, планируют это сделать. с SCR, что коррелирует со снижением выбросов NOx. Edwardsport может выбрать применение SCR, что снизит выбросы NOx примерно на две трети от количества, указанного на рисунке.
[Источник: Экологические характеристики электростанций IGCC, Стив Дженкинс (Ch3M HILL, Inc.) И Джордж Борас (Институт исследований в области электроэнергетики), 4-я Международная конференция во Фрайберге по технологиям IGCC и XtL, 3 мая 2010 г.]
Наконец, интересно увидеть влияние внедрения СКВ на NOx и другие виды загрязняющих веществ в контексте завод IGCC. На следующей диаграмме показаны выбросы основных регулируемых загрязняющих веществ для завода Duke Energy Edwardsport IGCC, как без, так и с работающей системой SCR, в сравнении с лимитами, указанными в разрешении NSPS класса V.Очевидно, что выброс NOx значительно снижается с помощью СКВ, и это незначительно влияет на другие загрязнители. Однако в любом случае выбросы всех регулируемых загрязняющих веществ значительно ниже установленных в разрешении пределов.
На следующей диаграмме показаны выбросы основных регулируемых загрязняющих веществ для завода Duke Energy Edwardsport IGCC, как без, так и с работающей системой SCR, в сравнении с лимитами, указанными в разрешении NSPS класса V.Очевидно, что выброс NOx значительно снижается с помощью СКВ, и это незначительно влияет на другие загрязнители. Однако в любом случае выбросы всех регулируемых загрязняющих веществ значительно ниже установленных в разрешении пределов.
| Выбросы турбины внутреннего сгорания завода Edwardsport IGCC, фунт / час | |||
| Сжигание синтез-газа, нагрузка 100% (59 ° F), SCR выключен | Сжигание синтез-газа, нагрузка 100% (59 ° F), SCR включен | Разрешенный предел | |
| NOx | 169.0 | 57,0 | 633 |
| CO | 92,5 | 93,0 | 194 |
| SO 2 | 28,9 | 29,0 | 633 |
| ЛОС | 3,3 | 3,3 | 8,4 |
| PM / PM 10 / PM 2,5 | 36.0 | 39,1 | 80,1 |
| H 2 SO 4 * | 3,2 | 6,4 | НЕТ |
1. Процесс сжигания обедненного премикса имеет множество названий, в том числе процесс сухого низкого уровня выбросов NOx (DLN) компании General Electric, процесс сухого низкого уровня выбросов (DLE) компании Rolls-Royce / Allison, и процесс SoLoNOx компании CATERPILLAR / Solar Turbines. Большинство имеющихся в продаже систем гарантированно сокращают выбросы NOx до диапазона от 9 до 25 частей на миллион, в зависимости от производителя, конкретной модели турбины и области применения. Некоторые производители гарантируют выбросы NOx в диапазоне 9 ppm (например, GE). По мере снижения уровня выбросов NOx некоторые производители столкнулись с проблемами, связанными с вибрацией сгорания (колебания динамического давления) и преждевременным выходом из строя камеры сгорания. Эти технологии могут привести к увеличению содержания CO и несгоревших углеводородов на целых 50 частей на миллион.
Некоторые производители гарантируют выбросы NOx в диапазоне 9 ppm (например, GE). По мере снижения уровня выбросов NOx некоторые производители столкнулись с проблемами, связанными с вибрацией сгорания (колебания динамического давления) и преждевременным выходом из строя камеры сгорания. Эти технологии могут привести к увеличению содержания CO и несгоревших углеводородов на целых 50 частей на миллион.
2. Тодд Д. и Баттиста Р., «Новые разработки в области сжигания синтез-газа LCV / опыт IGCC», технический доклад General Electric, 2001 г.
Мощность
Сжигание ископаемого топлива
Сжигание ископаемого топлива| Дроссман / Вейрс EV112 Блок 5, 2002 г. | ЭНЕРГИЯ |
На этом уроке мы изучим два основных источника загрязнения воздуха:
загрязнение от электростанций, работающих на угле и природном газе
и загрязнение от автомобилей. Основные загрязнители из всех
эти источники включают NOx, CO, углеводороды и твердые частицы.Установки, работающие на угле, содержат дополнительные загрязнители, в том числе SO2,
радиоактивные соединения, тяжелые металлы и твердые вещества, такие как летучая зола. Мы
кратко рассмотрим загрязняющие вещества, характерные для угольной энергетики
растений, а затем перейти к изучению химии NOx, CO и
углеводороды подробнее.
Загрязнение от производства электроэнергии (уголь) (1)
Электричество можно производить разными способами. Ключевой момент заключается в том, что другие формы энергии должны быть преобразованы в электричество. В США большая часть электроэнергии вырабатывается при сжигании ископаемых. топливо.Этот процесс преобразования никогда не бывает полностью чистым; к напротив, это обычно основной источник экологических проблем.
В целом влияние электроэнергии на окружающую среду зависит от
о технологиях и первичных источниках энергии, используемых для производства электроэнергии. Самый распространенный источник энергии для производства электроэнергии в США.
Штаты — уголь, который обеспечивал 52 процента всей электроэнергии в
1997 г. (USDOE, 1998a). Следующим по важности источником энергии является
уран, используемый атомными электростанциями, обеспечивая 18 процентов
U.С. электричество. Остальные 30 процентов делят натуральные
газ (14 процентов), гидроэлектроэнергия (10 процентов), нефть (3 процента),
и различные возобновляемые источники (3 процента), состоящие из
геотермальная энергия, биомасса, твердые бытовые отходы (включая свалки
газ), ветровая и солнечная энергия. На рисунке ниже показаны исторические
Тенденция в структуре энергетики США для выработки электроэнергии в США
Самый распространенный источник энергии для производства электроэнергии в США.
Штаты — уголь, который обеспечивал 52 процента всей электроэнергии в
1997 г. (USDOE, 1998a). Следующим по важности источником энергии является
уран, используемый атомными электростанциями, обеспечивая 18 процентов
U.С. электричество. Остальные 30 процентов делят натуральные
газ (14 процентов), гидроэлектроэнергия (10 процентов), нефть (3 процента),
и различные возобновляемые источники (3 процента), состоящие из
геотермальная энергия, биомасса, твердые бытовые отходы (включая свалки
газ), ветровая и солнечная энергия. На рисунке ниже показаны исторические
Тенденция в структуре энергетики США для выработки электроэнергии в США
Экологические проблемы, связанные с электростанциями, работающими на ископаемом топливе сегодня сосредоточены в первую очередь вокруг выбросов углекислого газа в атмосферу (CO2), диоксид серы (SO2), оксиды азота (NOx) и твердые частицы дело (ПМ).В таблице ниже показано количество этих выбросов. высвобождается на киловатт-час электроэнергии, произведенной в США Состояния по разным типам электростанций. Обратите внимание, что эти выбросы ставки отражают текущие различия в эффективности производства электроэнергии с использованием различных видов топлива и технологий.
Из-за потенциального воздействия этих загрязнителей на человека здоровье и окружающая среда, федеральные и государственные нормы ограничивают суммы, которые могут быть высвобождены из любого конкретного объекта.В целом, федеральные лимиты выбросов применяются к вновь построенным заводов, в то время как государственные и местные правила охватывают существующую мощность растения. Исключение составляют федеральные правила по кислотным дождям. контроль, который распространяется на все объекты. Примеры федеральных Пределы выбросов приведены в таблице ниже.
Природный газ выделяет на 42 процента меньше CO2, чем уголь, при поставке
такое же количество энергии. Различные топливные композиции дадут
немного разные результаты, но во всех случаях природный газ выделяет
значительно меньше CO2, чем уголь на единицу поставляемой энергии,
при условии, что эффективность преобразования одинакова. Эта экологическая
выгода является одной из причин того, что природный газ становится все более
привлекательно в качестве топлива для выработки электроэнергии.
Эта экологическая
выгода является одной из причин того, что природный газ становится все более
привлекательно в качестве топлива для выработки электроэнергии.
Одной из самых важных примесей в ископаемом топливе является сера. Сера встречается в минеральной форме в виде пирита (соединение железа и сера, также известная как «золото дураков» из-за ее ярко-желтого цвета), а также в органической форме внутри молекулярной состав угля. Нефть и природный газ также содержат соединения серы. при извлечении из земли.Однако большинство этих примесей удаляются на нефтеперерабатывающих и газоперерабатывающих заводах, которые очищать и очищать неочищенное топливо перед его распределением для использования. С другой стороны, уголь практически не обрабатывается. удаление серы перед сжиганием. Таким образом, самые высокие уровни примеси серы обычно присутствуют в угле. Когда уголь горит, небольшое количество серы, обычно от 2 до 5 процентов всего (в зависимости от типа угля) остается в твердых частицах золы. Большая часть серы (95 процентов и более) окисляется до газообразного состояния. диоксид серы SO2:
S + O2 -> SO2
Этот SO2 является основным источником кислотных дождей и источником неблагоприятных
последствия для здоровья.Очень небольшое количество (менее 1 процента)
SO2, образующийся при сгорании, может быть дополнительно окислен до SO3, который
реагирует с водяным паром в дымовых газах с образованием газообразного
серная кислота (h3SO4). При попадании в атмосферу этот газ
конденсируется в мелкие капли жидкости, которые остаются взвешенными в
воздух. Этот кислотный аэрозоль — еще один источник экологического
воздействия, связанные с примесями серы в ископаемом топливе.
Другой крупной примесью ископаемого топлива является минеральное вещество, обычно
называется ясень .Этот твердый негорючий материал включает:
соединения железа, кремния и других обычных элементов земных
корочка. Действительно, большинство природных элементов, включая токсичные тяжелые металлы, могут
можно найти в золе ископаемого топлива, особенно угля. Потому что
нефть и природный газ очищаются перед использованием, они содержат мало
или без золы при сгорании. Уголь, с другой стороны, относительно
с высоким содержанием золы, включая камни и минеральные вещества, оторванные от земли
в процессе майнинга. Часть этого материала отделена от
уголь перед сжиганием.Тем не менее, примерно 10 процентов угля
на электростанциях сжигается негорючий материал (сродни
остатки серой золы, оставшиеся в угольном гриле). Если не профилактический
приняты меры, выбросы угля в атмосферу
большие количества этой золы (также известной как зола , , потому что
он «вылетает» из дымохода). Все современные электростанции,
тем не менее, иметь системы контроля окружающей среды, которые удаляют почти
все частицы золы, захваченные потоком продуктов сгорания.
Ускользнувшие твердые частицы могут представлять опасность для окружающей среды.Такие выбросы твердых частиц относятся к числу загрязнителей воздуха.
Потому что
нефть и природный газ очищаются перед использованием, они содержат мало
или без золы при сгорании. Уголь, с другой стороны, относительно
с высоким содержанием золы, включая камни и минеральные вещества, оторванные от земли
в процессе майнинга. Часть этого материала отделена от
уголь перед сжиганием.Тем не менее, примерно 10 процентов угля
на электростанциях сжигается негорючий материал (сродни
остатки серой золы, оставшиеся в угольном гриле). Если не профилактический
приняты меры, выбросы угля в атмосферу
большие количества этой золы (также известной как зола , , потому что
он «вылетает» из дымохода). Все современные электростанции,
тем не менее, иметь системы контроля окружающей среды, которые удаляют почти
все частицы золы, захваченные потоком продуктов сгорания.
Ускользнувшие твердые частицы могут представлять опасность для окружающей среды.Такие выбросы твердых частиц относятся к числу загрязнителей воздуха.
Другой основной класс загрязнителей воздуха от сжигания ископаемого топлива оксиды азота (NOx). NOx состоит в основном из оксида азота. (NO) и диоксид азота (NO2), образующиеся в результате высокотемпературных реакций между кислородом и азотом. NOx может образовываться исключительно из молекулярный азот и кислород воздуха, а также атомарный примеси азота и кислорода в топливе. Потому что его образование во время процесса горения очень сложно, количество NOx обычно необходимо определять экспериментально.Для нефти и угля NOx выбросы на единицу топливной энергии обычно выше, чем на сжигание природного газа. Более высокие уровни NOx в основном связаны с наличие связанного с топливом азота, который легко превращается НЕТ при сгорании топлива. Количество топлива, связанного с NOx »обычно в два-три раза больше, чем« термический NOx «образуется только в результате реакций между N2 и O2 в воздух. Хотя NOx составляет лишь небольшую долю от общего продукты горения, тем не менее, их воздействие на окружающую среду существенный.
Доступны три основных подхода к снижению воздействия на окружающую среду. удары электростанций. Первый предполагает технологические меры
контролировать или удалять загрязнитель до того, как он попадет в
среда.
удары электростанций. Первый предполагает технологические меры
контролировать или удалять загрязнитель до того, как он попадет в
среда.
Второй подход — это применение «зеленого дизайна». принципы повышения эффективности производства электроэнергии. Более высокая эффективность означает, что для производства требуется меньше первичной энергии. желаемое количество электроэнергии; воздействие на окружающую среду снижено пропорционально.Такой подход наиболее плодотворен при проектировании новые объекты, хотя часто можно встречается на многих существующих заводах. Зеленый дизайн также включает загрязнение подходы к предотвращению, такие как инновации, которые производят полезные побочные продукты, а не твердые отходы.
Третий подход к борьбе с загрязнением включает выбор и
использование более чистых источников энергии и альтернативных технологий
с меньшим воздействием на окружающую среду. По концепции похож на зеленый
дизайн, этот вариант применяется в ситуациях, когда более одного
технология может выполнять заданную работу — в данном случае производить заданную
количество электричества.
Загрязнение от автомобилей (сжигание бензина) (2)
При сгорании бензина, как и при любой другой химической реакции, выделяется товары. При полном сгорании углеводорода выделяется только вода. и диоксид углерода. Вода, конечно, довольно безопасная вещь, и углекислый газ, способствуя потеплению парниковых газов и глобальному изменение климата, по крайней мере, нетоксично для дыхания. Но из-за неполного горение, побочные реакции с компонентами атмосферы, кроме кислород и реакции примесей в бензине, выхлопная труба также выделяет некоторые другие вещества, которые не столь безвредны.
В этом уроке вы узнаете, что это за вещества, что
часть процесса сгорания порождает их, и как они
регулируется. Вы узнаете о влиянии этих загрязнителей на здоровье.
и начнем рассматривать потенциальную роль кислородсодержащих добавок
в изменении загрязнения от автомобилей.
Источники загрязнителей воздуха
Как известно, два основных продукта горения автомобиля
топливо — CO2 и h3O. Жизнь на этой планете, какой мы ее знаем, будет
было бы невозможно, если бы у нас не было достаточно этих двух молекул.Однако слишком много хорошего не всегда может быть полезным.
поскольку оба являются парниковыми газами. В этом модуле вы сосредоточитесь
на соединениях, которые выделяются в гораздо меньших количествах, но имеют
известные последствия для здоровья человека. Эти соединения включают азота
оксиды , углеводородов и оксид углерода . Эти
соединения имеют собственное воздействие на здоровье, а также могут сочетаться
в атмосфере с образованием других опасных газов, таких как озон
(O3), компонент неприятной смеси загрязняющих веществ, известной как
смог.Как только вы поймете, как сжигается топливо в автомобилях
производит эти соединения и компромиссы, связанные с уменьшением
выбросы каждого, вы оцените, есть ли кислородсодержащее топливо
следует использовать для улучшения качества воздуха.
Хотя в этом уроке основное внимание уделяется загрязнителям, попадающим в атмосферу автомобилями, основными источниками каждого из этих загрязнителей воздуха на самом деле естественны. Углеводороды естественным образом производятся многими источники. Например, метан образуется при анаэробном распаде. органических материалов в таких областях, как заболоченные земли и рисовые поля, а терпены выделяются деревьями и зерновыми культурами.Монооксид углерода в основном образуется в результате естественного атмосферного окисления метана. Оксиды азота образуются в результате бактериального воздействия почвенных микробов. и последующие атмосферные реакции этих соединений. Цифры 1A-C представляют собой среднемировые количества каждого загрязняющего вещества. испускается из всех источников.
Рисунок 1A : Источники глобальных выбросов углеводородов
Рисунок 1B : Источники глобальных выбросов окиси углерода.
Рисунок 1C : Источники глобальных выбросов оксидов азота.
Бывший президент Рональд Рейган однажды заметил, что наибольшее загрязнение воздуха вызвано деревьями. Хотя он был не совсем прав, как вы можете Судя по рисункам, подобные его замечания заставили многих задуматься почему мы должны беспокоиться о антропогенных или созданных человеком, источники. Хотя источники антропогенного загрязнения меньше по количеству они вызывают серьезную озабоченность из-за их локальной концентрации. Природные загрязнители часто образуются на более обширных территориях и имеют тенденцию относительно равномерно распределяться за счет атмосферной циркуляции и смешивание.Однако антропогенные загрязнители, как правило, выбрасываются. в сконцентрированном пространстве и времени, и, таким образом, может испускаться во многих более высокие чистые ставки, чем естественные загрязнители в конкретном месте. Выбросы загрязняющих веществ в атмосферу от автомобилей сосредоточены в высокая населенность и плотность движения. Не хватает времени чтобы загрязнители рассеялись до того, как будет добавлено больше загрязнителей ежедневно, поддерживая высокий средний уровень в местной атмосфере.
Например, более 95% оксида углерода в атмосфере мегаполисов является результатом деятельности человека.Местные концентрации может быть в 50–100 раз больше, чем в среднем в мире концентрации. Это может подавить возможности естественных механизмов. чтобы очистить воздух. Рисунок 1D иллюстрирует этот эффект путем сравнения среднечасовые концентрации CO с учетом трафика в в центре Нью-Йорка. Эти концентрации CO представляют собой уровни выше фона естественных выбросов (рис. 1D).
Рисунок 1D: Концентрации окиси углерода и схемы движения в Нью-Йорке.Рисунок от Johnson, K. L .; Dworetzky, L.H .; Хеллер, А. Н. Наука 1968 , 160 , 67.
Производство, воздействие на здоровье и контроль над угарным газом
Окись углерода (CO) образуется в выхлопных газах транспортных средств при наличии
либо недостаточно времени для реакции, либо недостаток кислорода
для полного сгорания бензина в двигателе. Вы будете исследовать
Подробнее об этой ситуации позже в ваших исследованиях. При высоких концентрациях
выше 100 ppm (частей на миллион), окись углерода смертельна.При более низких концентрациях вредное воздействие на здоровье человека меньше.
хорошо задокументировано, но все же серьезно. Окись углерода связывается с
гемоглобин в крови очень эффективно, тем самым подавляя связывание
кислорода. Пониженная способность крови к кислороду приводит к острой
последствия воздействия CO, такие как головная боль, усталость и головокружение1.
Тем не менее, большой класс граждан добровольно вдыхает
концентрации CO несколько раз в день. Вы можете догадаться, кто
они могут быть?
Вы будете исследовать
Подробнее об этой ситуации позже в ваших исследованиях. При высоких концентрациях
выше 100 ppm (частей на миллион), окись углерода смертельна.При более низких концентрациях вредное воздействие на здоровье человека меньше.
хорошо задокументировано, но все же серьезно. Окись углерода связывается с
гемоглобин в крови очень эффективно, тем самым подавляя связывание
кислорода. Пониженная способность крови к кислороду приводит к острой
последствия воздействия CO, такие как головная боль, усталость и головокружение1.
Тем не менее, большой класс граждан добровольно вдыхает
концентрации CO несколько раз в день. Вы можете догадаться, кто
они могут быть?
Закон о чистом воздухе 1970 г. требовал от производителей автомобилей уменьшить количество загрязняющих веществ в результате сгорания топлива.Поздние поправки к Закону дополнительно снизили допустимые концентрации (см. Таблица 1B-1). Один очень эффективный ответ на эти требования было внедрение каталитических нейтрализаторов . В Основная функция автомобильных каталитических нейтрализаторов — преобразование СО в СО2 в присутствии воздуха и металлического катализатора. Поскольку каталитический преобразователи были впервые установлены в автомобилях США в 1975 году. количество автомобилей в США увеличилось вдвое, но концентрация CO в атмосфере снизились на 40% 2 — замечательное достижение химии и автомобильная техника.
Производство, воздействие на здоровье и контроль оксидов азота
Окислы азота образуются в двигателях как побочный эффект
горение топлива, реакция при высокой температуре азота
и кислород, естественно присутствующий в воздухе, необходимый для сгорания
топливо. Поскольку воздух необходим для реакции самого топлива, там
невозможно избежать этой дополнительной реакции, проблема, которую вы
подробнее рассмотрим позже в этом модуле. Транспортные счета
примерно для половины общих антропогенных выбросов NOx,
установки и другие стационарные источники горения следующие основные
источник.
Для химика оксиды азота включают NO, NO2 и N2O. Атмосферный ученых, однако, больше всего беспокоят токсичные и чрезвычайно реакционноспособные соединения NO и NO2, и обозначают их вместе как «NOx», то есть x может быть равно 1 или 2. Эти два соединения могут быть сгруппированы, потому что они быстро взаимопревращаются в атмосферы и, таким образом, играют совместную роль в образовании смога. Азотный оксид (NO) — основная форма, образующаяся непосредственно при сгорании, но NO2 более распространен в атмосфере.Закись азота (N2O, веселящий газ) классифицируется отдельно, потому что он намного меньше химически активен и не участвует в химии образования смога.
Оксиды азота влияют на качество воздуха по разным причинам. Атмосферный окисление NO приводит к образованию более высоких оксидов азота и, в конечном итоге, азотная кислота, значительный источник кислотных дождей, уступающий только оксиды серы. Катализируемая солнечным светом реакция в атмосфере между несгоревшими молекулами углеводородов и NOx приводит к фотохимическому смог, коричневая дымка, которую часто можно увидеть над большими городами.Один продукт из этих реакций — озон, загрязнитель в нижних слоях атмосферы. это раздражитель дыхательных путей. Парадоксально, что антропогенные выбросы ответственны как за избыток озона в тропосфере (нижняя атмосфера) и истощение озонового слоя в стратосфере (средняя атмосфера).
По сравнению со значительным прогрессом, достигнутым в снижении выбросов CO, попытки
по снижению уровня NOx оказались менее успешными. Новый каталитический
конвертеры содержат катализатор для восстановления NO до N2 и
O2, но этот восстановительный химический состав затрудняет присутствие
катализатора окисления, необходимого для удаления CO.Однако даже если
количество автомобилей увеличилось вдвое с 1975 года, уровни NOx
оставался практически неизменным в течение последних 15 лет. Содействие
факторы включают улучшенные каталитические нейтрализаторы, лучшую конструкцию двигателя,
и улучшенные составы бензина. Несмотря на эти достижения, сокращение
Выбросы NOx и смог по-прежнему представляют собой серьезную проблему для автомобилей.
производители и агентства по контролю за загрязнением.
Несмотря на эти достижения, сокращение
Выбросы NOx и смог по-прежнему представляют собой серьезную проблему для автомобилей.
производители и агентства по контролю за загрязнением.
Производство, воздействие на здоровье и контроль углеводородов
Углеводороды — это большой класс соединений, образованных из углерода
и водород, и поэтому иногда их вместе обозначают «CHx».В контексте загрязнения воздуха в эту категорию входят несгоревшие
и частично сгоревшие компоненты бензина, выпущенные при
выхлопная труба в результате неполного сгорания или испарения топлива
резервуары, заправочные станции и нефтеперерабатывающие заводы. Транспортные счета
примерно на половину общих выбросов углеводородов. Термин «летучие»
органические соединения »или ЛОС. часто используются как взаимозаменяемые.
Этот термин является более широким и учитывает тот факт, что частично сгоревшие
углеводороды, строго говоря, не являются углеводородами, потому что
они включают немного кислорода в свои структуры.Примеры
к этой группе относятся формальдегид (HCHO) и ацетальдегид (Ch4CHO).
Атмосферные углеводороды на текущих уровнях окружающей среды (т. Е.
количества, присутствующие в воздухе, которым мы дышим) представляют опасность для здоровья
меньше из-за их собственных опасностей, чем из-за их роли в
образование других, более опасных соединений. Исследования показывают, что
даже при гораздо более высоких концентрациях, алифатических или линейно-цепочечных,
углеводороды не оказывают вредного воздействия на здоровье. Тем не мение, ароматические или циклические углеводороды представляют большую опасность.Простейший ароматический углеводород, бензол, содержится в бензине,
и является известным канцерогеном. Ароматические пары также являются раздражителями
при вдыхании. Более того, многие соединения, образующиеся при атмосферном окислении
углеводородов, включая альдегиды и раздражающие компоненты смога
такие как пероксиацетилнитрат (PAN) и озон, проявляют свои собственные
неблагоприятные последствия для здоровья.
Для производства озона в тропосфере требуется солнечный свет, NOx
и ЛОС. Таким образом, и NOx, и летучие органические соединения контролируются экологическими
агентства.Новые каталитические нейтрализаторы включают катализатор для окисления.
частично сгорели углеводороды полностью до СО2, вместе с
CO. Плотно прилегающие крышки топливных баков, устройства для улавливания паров на топливных насосах,
и осмотр и обслуживание топливопроводов и баков — это меры
что может помочь снизить выбросы углеводородов в результате испарения. В
Закон о чистом воздухе потребует дальнейших сокращений, если высокий процент
сильно загрязненных городов остается дымным.
Последняя опасность, связанная с ЛОС, особенно более полярными соединениями
такие как альдегиды, их тенденция слипаться в
Атмосфера образует крошечные жидкие частицы, называемые аэрозолями .Аэрозоли также будут содержать кислотные вещества из NOx.
Эти частицы, а также сажа и другие частицы напрямую
испускаемые транспортными средствами, несут ответственность за снижение видимости
или «дымка», которая является одним из характерных эффектов смога. Они
представляют опасность для органов дыхания, особенно мелкие частицы меньше
более 10 микрон, которые с меньшей вероятностью будут захвачены волосками в носу
и слизистые оболочки перед попаданием в легкие.
Выбросы твердых частиц привлекают все большее внимание со стороны исследователи атмосферы, токсикологи и регуляторы загрязнения.Потому что сложная химия и физика их образования еще не очень хорошо изучены, вы не станете подробно изучать частицы в этом модуле. Однако вам следует сохранить этот дополнительный загрязнитель. имея в виду, когда вы рассматриваете более широкие проблемы загрязнения воздуха от автомобили.
Таблица 1E : Нормы выбросов выхлопных газов автомобилей в граммах за милю для легковых автомобилей США (за исключением Калифорнии, которая имеет свои стандарты) (3)
Восстановление CO с помощью оксигенатов
Кислородсодержащие присадки к топливу являются горючими соединениями
которые содержат кислород в своей молекулярной структуре. Примеры
Наиболее распространенные кислородсодержащие присадки к топливу приведены в Таблице 1Е.
Продолжаются дискуссии о том, помогают ли такие добавки снизить
загрязнение воздуха, дискуссия, о которой вы узнаете больше в процессе работы
через этот урок.
Примеры
Наиболее распространенные кислородсодержащие присадки к топливу приведены в Таблице 1Е.
Продолжаются дискуссии о том, помогают ли такие добавки снизить
загрязнение воздуха, дискуссия, о которой вы узнаете больше в процессе работы
через этот урок.
Большинство кислородсодержащих присадок к топливу также являются усилителями октанового числа, обеспечивая более высокое октановое число при смешивании с бензином. Оксигенированные были впервые представлены в США как усилители октанового числа и как отечественные заменители нефти во время арабского нефтяного эмбарго в начале 1970-х годов.Октановые числа бензиновых смесей, используемых в США обычно составляет от 85 до 94. Доступный диапазон октанового числа зависит от географического региона и производителя. Вы можете предположить что более высокие цены на топливо с более высоким октановым числом коррелируют либо с большей топливной экономичностью, либо с большей топливной эффективностью. Однако это не всегда так.
EPA требует, чтобы кислородсодержащие бензины включали не менее 2,7% кислорода по массе в топливе, продаваемом при недостижении окиси углерода области.Область недостижения — это та, которая в настоящее время не встречается Стандарты EPA для конкретного рассматриваемого загрязнителя. Требование для кислородсодержащего топлива в областях недостижения CO известен как Программа Wintertime Oxy-Fuel, потому что окись углерода имеет тенденцию к накапливаются, когда воздух плохо перемешивается. Это происходит чаще зимой, когда возможны температурные инверсии, отлов застойный слой воздуха у поверхности. Эти погодные условия также более распространены в западных городах, особенно в приграничных горами, которые, как правило, помогают улавливать инверсии.В озоне области недостижения, EPA требует не менее 2,0% кислорода для масса. Эта программа известна как Летний реформулированный бензин. (RFG) программа. Исходя из того, что вы уже знаете об образовании смога, как вы думаете, зачем нужна эта программа летом?
Таблица 1E: Кислородные топливные добавки и необходимые количества Соответствует стандарту EPA на 2,7% O по массе для областей, недоступных для CO
| Название добавки | Химическая формула | Плотность (г / мл) | Массов. % Кислорода в чистой присадке % Кислорода в чистой присадке | % (мас.%) (Мас.% Присадки в топливной смеси) |
| этанол | Ч4Ч3ОН | 0.794 | ||
| метанол | Ch4OH | 0,791 | 50% | 5,4% |
| МТБЭ | (Ч4) 3СОЧ4 | 0,740 | ||
| ETBE | (Ч4) 3СОЧ3Ч4 | 0,742 | ||
| TAME | (Ч4) 3ЦЧ3ОЧ4 | 0.770 | ||
| TBA | (Ch4) 3COH | 0,775 |
Источники «большой тройки» первичных загрязнителей воздуха (4)
Тропосферный озон
Озон (O3) — химически активный газ, состоящий из трех атомов кислорода. атомов, в отличие от нормального молекулярного кислорода (O2). Большинство из атмосферный озон Земли (8590 процентов) находится в стратосфера — часть атмосферы между примерно 10 и 45 километров (км) над уровнем моря.В стратосфере озон играет решающую роль в поглощении испускаемого ультрафиолетового излучения солнцем. Остальные 1015 процентов атмосферного озона находится в тропосфере — нижняя часть атмосферы простирается от поверхности земли до высоты примерно 10 км.
Озон — это следы атмосферного газа с естественной концентрацией в
чистая тропосфера примерно 3040 частей на миллиард
(ч / млрд). Если бы весь объем атмосферного озона сжался до
при давлении в одну атмосферу он образовал бы слой всего 3 мм.
толстый.Поскольку озон существует в таких малых концентрациях в
атмосферы, человеческая деятельность более склонна вызывать изменения в
его концентрация.
Были зафиксированы высокие концентрации озона, превышающие примерно 100 частей на миллиард.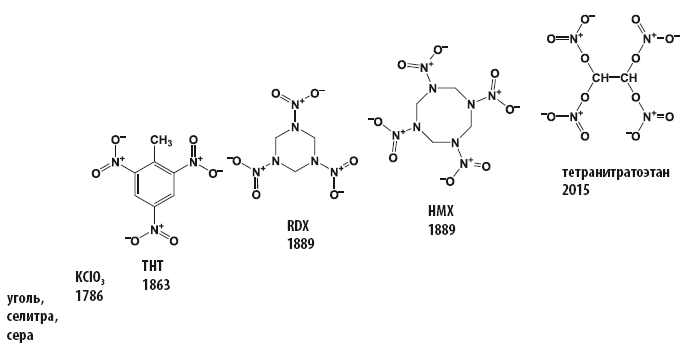 показано, что связано с неблагоприятным воздействием на дыхательные пути человека.
система. Эффекты более значительны для людей, которые занимаются спортом.
Острые эффекты, такие как изменение емкости и функции легких,
наблюдались у некоторых людей после воздействия менее чем
час. В некоторых случаях эффекты сохраняются в течение многих часов или дней.Высокие концентрации озона также могут повредить деревья и сельскохозяйственные угодья.
посевы, а также повредить определенные материалы.
показано, что связано с неблагоприятным воздействием на дыхательные пути человека.
система. Эффекты более значительны для людей, которые занимаются спортом.
Острые эффекты, такие как изменение емкости и функции легких,
наблюдались у некоторых людей после воздействия менее чем
час. В некоторых случаях эффекты сохраняются в течение многих часов или дней.Высокие концентрации озона также могут повредить деревья и сельскохозяйственные угодья.
посевы, а также повредить определенные материалы.
Интенсивность углерода
Выражение содержания углерода в топливе по отношению к содержание энергии в топливе дает прямую связь между потреблением энергии и выбросы углерода. Отношение содержания углерода в топливе к его энергоемкость определяет углеродоемкость :
Интенсивность углерода = Масса углерода в топливе / энергия топливаСравнение значений нагрева топлива
| Топливо | Энергосодержание кДж / л | Бензиновый эквивалент, * л / л-бензин |
| Бензин | 31 850 | 1 |
| Легкий дизель | 33 170 | 0.96 |
| Тяжелый дизель | 35 800 | 0,89 |
| LPG (сжиженный углеводородный газ, в основном пропан) | 23 410 | 1,36 |
| Этанол | 29 420 | 1,08 |
| Метанол | 18 210 | 1,75 |
| CNG (Сжатый природный газ, преимущественно метан, при 200 атм.) | 8 080 | 3.94 |
| СПГ (сжиженный природный газ, в основном метан) | 20 490 | 1,55 |

После определения теплотворной способности топлива (на основе
HHV или LHV) рассчитывается соответствующая углеродная интенсивность
как:
Доля углерода в топливе может быть указана на любой массе
основание или молярное основание, в соответствии с единицами измерения, используемыми для обогрева
ценить.
| Источник энергии | Содержание углерода (мас.% C) | Теплотворная способность * (кДж / г) | Интенсивность углерода (гКл / МДж) |
| Природный газ | 74 | 54,4 | 13,7 |
| Сырая нефть | 85 | 44.3 | 19,2 |
| Уголь ** | 59 | 24,2 | 24,4 |
* На основе HHV
** значения различаются на ~ 30% для разных типов угля
Источник: USDOE и IPCC
Список литературы
1) По материалам Rubin, Engineering и окружающая среда, Глава 5.
2) Взято из Дроссмана, Лаурсена. и Тикканен, модуль загрязнения воздуха, ChemLinks
3) По материалам Rubin, Engineering и окружающая среда, Глава 3.
4) Схемы от Рубина, Инжиниринг и окружающая среда, главы 3 и 5.
.




 97)
97)
